Manejo de la infertilidad
Introducción
La endometriosis es una enfermedad inflamatoria, crónica, progresiva, sistémica, dependiente de estrógenos y resistente a la progesterona. Se define como la presencia de tejido endometrial (glándulas y estroma) fuera de la cavidad uterina (1). Se estima que afecta entre el 2% y el 10% de las mujeres en edad reproductiva. Entre el 25 y 50% de las mujeres con endometriosis son subfértiles. Actualmente al menos 190 millones de mujeres en edad reproductiva están afectadas por la enfermedad, y en algunos casos persiste durante la menopausia (2). La endometriosis conlleva un considerable costo económico para la sociedad, con gastos médicos directos e indirectos comparables a los de otras enfermedades crónicas. A pesar de esto, existe un retraso significativo de 4 a 11 años desde el inicio de los síntomas hasta el diagnóstico definitivo de la enfermedad (3), lo que puede atribuirse a una falta de conciencia sobre la endometriosis entre los profesionales de la salud, así como a la complejidad y variabilidad sus manifestaciones clínicas, lo que dificulta su identificación y abordaje temprano. Este retraso en el diagnóstico puede tener repercusiones adversas en la calidad de vida de las pacientes, subrayando la necesidad imperante de mejorar la educación y concientización sobre la endometriosis tanto entre los profesionales de la salud como en la población en general. Los síntomas más frecuentes incluyen dismenorrea, dispareunia y dolor pelviano acíclico o crónico, aunque también puede ser asintomática o ser sospechada debido a dificultades para lograr embarazo. A pesar de que existe una asociación establecida entre endometriosis e infertilidad, los mecanismos implicados aún no se comprenden completamente, pero se reconoce que es una enfermedad multifactorial.
El propósito de esta revisión es examinar los mecanismos biológicos relacionados con la infertilidad asociada a la endometriosis y su tratamiento, fundamentados en la medicina basada en la evidencia científica.
Mecanismos biológicos de la infertilidad asociada a la endometriosis
La tasa de fecundidad en parejas sanas se sitúa entre el 15 al 20% por ciclo menstrual, disminuyendo con la edad de la mujer. Por otro lado, la tasa de fecundidad de mujeres con endometriosis oscila entre el 2 y el 10%. Se han propuesto varios mecanismos que podrían contribuir a la infertilidad asociada a la endometriosis.
Factor coital
El dolor experimentado durante las relaciones sexuales puede estar vinculado con la infertilidad asociada a la endometriosis, incluyendo la dispareunia superficial que interfiere con el inicio del coito como la dispareunia profunda, que dificulta su mantenimiento (4). Además, el dolor pelviano crónico asociado a la endometriosis puede influir en la disminución del deseo sexual, lo que a su vez puede tener repercusiones en las relaciones de pareja y en la calidad de vida.
Distorsión anatómica de la cavidad peritoneal
La endometriosis en una enfermedad inflamatoria crónica. Varios estudios (5) han demostrado una alta concentración de prostaglandinas, proteasas y citoquinas en el medio ambiente peritoneal de estas pacientes como IL-1, IL-6, TNFa, IL-8 y VEGF producidos principalmente por los macrófagos. Ese medio proinflamatorio ejerce efectos adversos en la calidad del ovocito resultando en una disminución de su capacidad para completar la maduración y fertilización, debido a la des- regulación de la esteroidogénesis (disminución del estradiol) y las alteraciones del microambiente intrafolicular (disminución de la eficacia reproductiva). Asimismo, el medio inflamatorio afecta la función de los espermatozoides y afecta el desarrollo embrionario6, lo que resulta en la detención del desarrollo embrionario y una diminución del potencial de implantación. Además este medio inflamatorio puede provocar la formación de adherencias en la cavidad peritoneal lo que dificulta la interacción entre las fimbrias y el cúmulus, obstaculizando así la captación ovocitaria, y la ovulación.
Reserva ovárica
La Sociedad Americana de Medicina Reproductiva (ASRM) define como reserva ovárica a la cantidad de ovocitos presen- tes en el ovario, representada por el número de ovocitos. Es importante distinguir este concepto de la calidad ovocitaria, que se refiere al potencial de un ovocito fertilizado para dar lugar a un recién nacido vivo. Hay varias causas responsables de la disminución de la reserva ovárica en pacientes con endometriosis; entre las más importantes se encuentran (7):
- Cirugía: la quistectomía puede provocar daño en el tejido ovárico circundante con pérdida de la masa folicular. Este daño es más pronunciado en los casos de endometriomas bilaterales y puede estar relacionado con el uso de electro- coagulación y la inflamación local asociada al procedimiento quirúrgico. Además, la disminución de la vascularización ovárica puede ocurrir en casos de adhesiolisis extensa, incluso en ausencia de intervención quirúrgica directa en los ovarios.
- Endometrioma: pueden ejercer un efecto de masa ocupante en el tejido ovárico circundante y su contenido (hierro libre, citoquinas, enzimas proteolíticas) puede inducir estrés oxidativo y daño en el tejido sano adyacente. El tejido que rodea el pseudoquiste endometriósico presenta alteraciones morfológicas como fibrosis, disminución del estroma específico de la corteza, metaplasia de células de músculo liso, disminución de la vascularización y menor densidad folicular. Estas alteraciones no se observan en otros quistes benignos ni en el ovario contralateral que no presenta endometrioma. La proporción de folículos primordiales se ve significativamente reducida, junto con un aumento del reclutamiento folicular, lo que conduce a una activación folicular persistente (efecto burn out) y disminución precoz de la reserva ovárica.
- Medio ambiente peritoneal tóxico: se ha observado una disminución de la reserva ovárica en pacientes con endometrio- sis peritoneal mínima o moderada, incluso en ausencia de endometriomas.
Receptividad endometrial
La endometriosis se asocia a disminución de la decidualización y receptividad endometrial atribuida a la resistencia a la progesterona, caracterizada por una reducción de la expresión de sus receptores A y B en el endometrio. Este fenómeno es inducido por la producción local de estrógenos con inflamación y aumento de la proliferación celular (5). La resistencia a la progesterona conduce a una disminución de la expresión de genes claves en la implantación (HOXA 10, la integrina B3). Un estudio retrospectivo (8) que compara tasas de nacido vivo en pacientes con endometriosis receptoras de ovocitos versus receptoras sin endometriosis no encontró diferencias significativas en los resultados reproductivos. Esto podría explicarse, ya que, en general, las pacientes receptoras con endometriosis tienden a ser de mayor edad que las pacientes que utilizan sus propios óvulos, lo que sugiere una función ovárica disminuida o ausente con mayor remisión de la enfermedad (9).
Manejo de la infertilidad asociada a la endometriosis
El abordaje clínico de la infertilidad asociada a la endometriosis representa un gran desafío para los profesionales de la salud dada la diversidad de fenotipos presentes en las pacientes infértiles con esta condición. En la era de la medicina personalizada, se recalca la necesidad de un tratamiento individualizado que tome en consideración diversos factores, como la edad de la paciente, la reserva ovárica, la duración de la infertilidad, el factor masculino, el estadio de la enferme- dad, antecedentes de cirugías previas y la presencia de dolor concurrente. La toma de decisiones y la elección del trata- miento deben ser consensuados entre el médico y la paciente, teniendo en cuenta tanto la situación clínica y los deseos personales de la paciente.
Tratamiento médico
El tratamiento médico es efectivo en el alivio del dolor asociado a la endometriosis. Sin embargo, su aplicación previa a la búsqueda de embarazo no demuestra un aumento significativo en las tasas de concepción espontánea después de su suspensión, por lo que no se recomienda su uso para mejorar las tasas de embarazo natural (2). Además, la mayoría de los tratamientos médicos tienen efectos inhibidores de la ovulación, lo que puede resultar en un retraso en la búsqueda de embarazo. El tratamiento médico sólo se justificaría en situaciones donde la paciente haya sido sometida a cirugía y no tenga intención de buscar embarazo inmediatamente tras el procedimiento, con el propósito de prevenir la recurrencia de la enfermedad y manejar el dolor asociado a la endometriosis.
Tratamiento quirúrgico
La decisión de realizar tratamiento quirúrgico en las pacien- tes con infertilidad asociada a la endometriosis debe basarse en una evaluación integral de diversos factores (edad de la paciente, reserva ovárica, presencia de dolor, antecedentes de cirugías previas, estadio de la enfermedad). La endome- triosis mínima y moderada (estadios I y II de ASRM) pueden manifestarse con dolor, aunque no se evidencien hallazgos en el examen físico o en las imágenes. Algunos metaanálisis sugieren que la laparoscopía quirúrgica puede mejorar las ta- sas de embarazo espontáneo y de nacidos vivos. Las guías de la ASRM y la Sociedad Europea de Reproducción Humana y Endocrinología (ESHRE) recomiendan considerar la laparos- copía en estadios tempranos de la enfermedad, especialmen- te cuando se indica por otros motivos, como la presencia de dolor. En pacientes jóvenes (menores de 30 años) puede ser beneficiosa para mejorar las tasas de embarazo espontáneo (2, 9). En pacientes asintomáticas no se recomienda realizar laparoscopía previa a los tratamientos de reproducción asisti- da con el único objetivo de mejorar las tasas de embarazo, ya que los beneficios potenciales no están completamente claros y los tratamientos de reproducción asistida tienen buenos re- sultados, principalmente en mujeres menores de 35 años y en aquellas de mayor edad cuando se realizan transferencias de embriones euploides (2, 10). En casos de endometriosis es- tadios III y IV, la decisión quirúrgica es más compleja debido a la falta de evidencia científica de alta calidad que respalde beneficios en los resultados, así como al riesgo de complica- ciones quirúrgicas. La indicación quirúrgica es clara en casos de dolor, grandes endometriomas, sospecha de malignidad, o alteraciones funcionales de otros órganos pelvianos (obstruc- ción intestinal, ureteral, compresión nerviosa). En pacientes asintomáticas con endometriomas, la cirugía debe ser reco- mendada para mejorar el acceso a los folículos o prevenir ruptura con contaminación ovocitaria o infección durante la aspiración folicular (2). Sin embargo, la quistectomía no está indicada únicamente para mejorar los resultados de los trata- mientos de reproducción asistida, ya que puede comprometer la reserva ovárica sin aportar beneficios significativos.
Tratamientos de reproducción asistida (TRA)
Es fundamental proporcionar asesoramiento objetivo a las pacientes que desean embarazo, tanto antes como después de someterse a la cirugía, considerando detalladamente su histo- ria clínica, la de su pareja y sus posibilidades reales de lograr un nacido vivo con o sin cirugía y/o TRA. En caso de optar por la cirugía el Índice de Fertilidad de Endometriosis (IFE) emer- ge como un sistema de puntuación validado que estadifica la enfermedad y facilita la predicción de la probabilidad de embarazo espontáneo o con TRA de baja complejidad. El IFE
considera factores clínicos (edad, antecedentes obstétricos, duración de la infertilidad) y quirúrgicos (función tubárica y ovárica, presencia lesiones endometriósicas, estadio de la en- fermedad, entre otros).
TRA de baja complejidad
Hay una limitada cantidad de estudios que evalúan la efec- tividad de la inseminación intrauterina (IIU) con o sin esti- mulación ovárica en pacientes con endometriosis. Un estudio controlado aleatorizado comparando pacientes con endome- triosis mínima/ moderada sometidas a estimulación ovárica + IIU versus manejo expectante concluyó que el primer grupo presentó tasas de nacidos significativamente mayores (11). En cuanto a los estadios III y IV, la eficacia de la IIU en las pacientes con trompas permeables no es clara. En presencia de otros factores de riesgo como baja reserva ovárica, edad mater- na avanzada o dolor, los tratamientos de reproducción asistida de alta complejidad muestran mejores resultados (2, 11).
TRA de alta complejidad
A pesar de la amplia implementación de los TRA de alta complejidad, persiste un debate sobre la influencia de la en- dometriosis en la efectividad de estos tratamientos en mujeres con esta condición. Las indicaciones principales para los TRA incluyen la edad reproductiva avanzada, los estadios III y IV de la enfermedad, la alteración tubárica, el factor masculino, el EFI bajo y el fracaso de otros tratamientos. No existen estu- dios aleatorizados y controlados que evalúen la eficacia de los TRA en comparación con ausencia de intervención en mujeres con endometriosis. Hasta la fecha los protocolos de induc- ción de la ovulación con agonistas o antagonistas del GnRH han demostrado una eficacia similar, y su elección debe ba- sarse en las preferencias del médico y la paciente. Pirtea10 en una revisión describe que el efecto toxico resultante de la inflamación en la cavidad peritoneal de las pacientes con endometriosis altera la calidad de los gametos y el desarrollo embrionario en caso de concepción natural o de la IIU con estimulación ovárica. Este efecto podría prevenirse con los TRA de alta complejidad al evitar el contacto de los gametos y el embrión con el medio peritoneal tóxico. Además, existe una disminución de la receptividad endometrial en el endo- metrio eutópico debido a la producción local de estrógenos y a la resistencia a la progesterona, efectos que desaparecen en caso de supresión ovárica. Pirtea (12) proporciona datos que indican que esta neutralización del efecto de la inflamación también se observa después de la supresión ovárica utilizando los regímenes de estrógeno y progesterona en transferencias de embriones congelados. Por lo tanto, concluye que estas pacientes se beneficiarían con criopreservación total de em- briones y la transferencia embrionaria diferida.
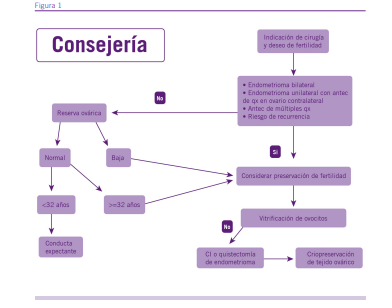
Preservación de la fertilidad
Las pacientes con endometriosis enfrentan un mayor riesgo de compromiso de la reserva ovárica, por la propia enferme- dad y por causas iatrogénicas. Existen niveles reducidos de Hormona Antimülleriana en pacientes con endometriomas in- cluso antes de someterse a intervenciones quirúrgicas. Esta enfermedad podría justificar la consideración de estrategias de preservación de la fertilidad. Un diagnóstico precoz y un tratamiento médico oportuno para frenar la evolución de la en- fermedad y prevenir recurrencias y la cirugía conservadora son métodos altamente costo-efectivos para preservar la fertilidad de las pacientes. Entre las estrategias de preservación de la fertilidad se incluyen la vitrificación de ovocitos, embriones y la criopreservación de tejido ovárico. Un estudio publicado por Cobo y colaboradores (13) propone la vitrificación de ovo- citos como una herramienta eficaz para mejorar las chances reproductivas de las pacientes, la cual debería considerarse antes de la cirugía si está indicada. Este estudio reveló los resultados de la vitrificación y desvitrificación de ovocitos en 485 pacientes con endometriomas de por lo menos 1 cm y recuento de folículos antrales > 3, obteniendo en una tasa de sobrevida a la desvitrificación del 83,2% y una tasa acumu- lada de nacido vivo del 46,4%. En situaciones en las cuales la estimulación ovárica no es posible, y en el contexto de una cirugía por endometrioma uni o bilateral, de rápido crecimien- to o recidivante se puede considerar la criopreservación de tejido ovárico (14, 15). En todos estos escenarios es impera- tivo discutir con la paciente los beneficios y los riesgos de las
técnicas de preservación de fertilidad, brindándole la información necesaria para que pueda tomar una decisión informada y alineada con sus necesidades preferencias personales.
Conclusiones
La endometriosis es una enfermedad multifactorial que afecta la calidad de vida de las mujeres y conlleva un importante impacto económico en la sociedad.
Existe un retraso en el diagnóstico de la endometriosis, lo que subraya la necesidad de mejorar la concientización sobre esta enfermedad.
Los mecanismos biológicos que contribuyen a la infertilidad asociada a la endometriosis incluyen el factor coital, la distor- sión anatómica de la cavidad peritoneal, la disminución de la reserva ovárica y la alteración de la receptividad endometrial. El abordaje clínico debe ser individualizado y considerar factores, como la edad de la paciente, la reserva ovárica, la duración de la infertilidad y el estadio de la enfermedad. Los TRA de baja y de alta complejidad, son opciones viables para las pacientes con endometriosis y pueden mejorar las tasas
de embarazo.
En resumen, un enfoque integral y personalizado que combine diferentes modalidades de tratamiento, incluyendo la educación sobre la enfermedad, el manejo del dolor, la preservación de la fertilidad y los tratamientos de reproducción asistida es esencial para mejorar los resultados reproductivos y la calidad de vida de las mujeres con endometriosis.
Referencias bibliográficas
- 1. Tomasetti C, et al. International working group of AAGL ESGE ESHRE and WES.2021. Facts Views Vis Obgyn. 2021;13(4):295- 304.
- 2. Becker CM, el al.ESHRE Endometriosis Guideline Group, ESHRE guideline: endome- triosis. Human Reproduction Open. 2022; 2.
- 3. Agarwal SK, et al. Clinical diagnosis of endometriosis: A call to action. Am J Obstet Gynecol. 2019; 220:354.e1–354.e12.
- 4.Wahl KJ, et al. Deep Dyspareunia, Su- perficial Dyspareunia, and Infertility Con- cerns Among Women Wiith Endometrio- sis: A Cross-Sectional Study. Sex Med. 2020;8(2):274-281.
- 5. García-Gómez E, et al. Regulation of Inflammation Pathways and Inflammasome by Sex Steroid Hormones in Endometriosis. Front. Endocrinol. 2020;10:935.
- 6. Simopoulou M, et al. Getting to Know
Endometriosis-Related Infertility Better: A Review on How Endometriosis Affects Oocyte Quality and Embryo Development. Biomedici- nes. 2021; 9(3):273.
- 7. Sanchez AM, et al. The distinguishing cellular and molecular features of the endo- metriotic ovarian cyst: from pathophysiolo- gy to the potential endometrioma-mediated damage to the ovary. Hum Reprod Update. 2014;20(2):217–30.
- 8. Kamath MS. Endometriosis and oocyte quality: an analysis of 13614 donor oocyte recipient and autologous IVF cycles. Hum Re- prod Open. 2022; 10.
- 9. Bonavina G and Taylor HS. Endometrio- sis-associated infertility: From pathophysio- logy to tailored treatment. Front. Endocrinol. 2022; 13:1020827.
- 10. Pirtea P, et al. Fertility workups: identifying endometriosis. Fertil Steril. 2022;118:29–33
- 11. Skorupskaite K, et al. Evidence based management of patients with endometriosis undergoing assisted conception: British ferti- lity society policy and practice recommenda- tions. Human Fertility. 2024; 27:1.
- 12. De Ziegler D. Fertility worksups: the times they are a-changin´. Fertil Ste- ril.2022;118:5–7.
- 13. Cobo A, et al. Oocyte vitrification for fertility preservation in women with endome- triosis: an observational study. Fertil Steril. 2020;113:836e44.
- 14. Dolmanz MM, Donez J. Fertility preser- vation in women for medical and social rea- sons: Oocytes vs ovarian tissue. Best Practice & Research Clinical Obstetrics and Gynaeco- logy. 2021;70:63e80.
- 15. Anderson R. ESHRE Guideline Group: Female Fertility Preservation. Hum Reprod Open. 2020; 14:4.







No comments! Be the first commenter?