Revisión sistemática de la asociación entre enfermedad mental, sobrepeso, obesidad y su tratamiento. Segunda parte
Resumen
Introducción: Pese a que existen algunos fármacos con probada eficacia antiobesidad, con mecanismos de acción heterogéneos (disminuyendo el apetito, alterando el metabolismo o inhibiendo la absorción calórica), los mismos exhiben en numerosas ocasiones severos efectos adversos y colaterales, que han obligado incluso a su retiro del mercado. Ejemplos de estos últimos son la sibutramina y el rimonabant. En consecuencia existen pocos fármacos aceptados. En los últimos años se han realizado progresos en dilucidar los mecanismos que controlan la obesidad, incluyendo el sistema digestivo y neural, además de las sustancias que intervienen en los mecanismos regulatorios como péptidos y hormonas.
Objetivo: revisar las nuevas actualizaciones en el tratamiento de la obesidad, teniendo en cuenta las asociaciones con los trastornos mentales. Se tomaron en cuenta las principales guías de consenso. Se señala el rol desempeñado por el hipotálamo como homeostato de los ciclos alimentarios y del peso corporal. Se analizan los fármacos que se encuentran aprobados y otros en fase de investigación para su uso terapéutico.
Material y métodos: se efectuó una búsqueda en bases de datos electrónicas PubMed, Ebsco, Host y OvidSP, utilizando como palabras clave los términos sobrepeso, obesidad, enfermedad mental, adultos, pacientes, comorbilidad, trastorno psiquiátrico, tratamiento. Se les dio prioridad a los trabajos que presentaban una estricta metodología científica; sobre todo, ensayos doble ciego aleatorizados controlados con placebo o metaanálisis, y que hubieran sido publicados en la última década, así como en- sayos abiertos o reportes de casos considerados relevantes por consenso de expertos.
Resultado: se analizan las principales opciones terapéuticas, incluyendo el papel de los fármacos, así como las limitaciones en su uso agudo y crónico.
Palabras clave
Obesidad – Farmacoterapia – Mecanismos de acción.
Tratamiento de la obesidad
En vista de la alta prevalencia de obesidad entre pacientes con distintas enfermedades psiquiátricas, los psiquiatras fre- cuentemente enfrentan la necesidad de encarar simultánea- mente el tratamiento para ambas patologías. Hay suficiente evidencia de que los psiquiatras no siempre cuentan con la suficiente preparación para el manejo de sus pacientes obe- sos (1, 8).
Por otra parte, es sumamente frecuente que el psiquiatra en su práctica diaria aborde el tratamiento conjunto de los dos problemas, el trastorno psiquiátrico de base y la obesidad, ya sea por obesidad primaria o secundaria al uso de psicofármacos. Las guías internacionales para el manejo de la obesidad recomiendan los siguientes criterios (9, 12).
Reducción y el mantenimiento del peso corporal
El tratamiento integral para adelgazar (y para mantener el peso corporal) debe incluir la combinación de alimentación baja en calorías, aumento de la actividad física y terapia conductual (13, 17). La reducción de la ingesta alimentaria para producir un balance energético negativo constituye el com- ponente fundamental del tratamiento del sobrepeso y la obesidad. Con dietas bajas en calorías se busca la creación de un balance energético negativo para reducir el excedente de triglicéridos existente en el tejido adiposo. Sin embargo, la disminución exclusiva de la grasa alimentaria sin disminuir la ingestión de energía no es suficiente para producir adelgaza- miento. La reducción de la grasa junto con los hidratos de car- bono en la dieta puede facilitar la disminución de la energía alimentaria (18, 20). Una dieta planificada individualmente para ayudar a crear un déficit diario de 500 a 1 000 kcal deberá ser parte integrante de cualquier programa dirigido a conseguir un adelgazamiento de 0,5-1 kg de peso semanal. Se recomienda que la actividad física forme parte del trata- miento global para la reducción y el mantenimiento de peso porque:
1) contribuye a la disminución de peso en los adultos con sobrepeso y obesidad;
2) puede reducir la grasa abdominal;
3) aumenta la competencia cardiorrespiratoria, y
4) puede ayudar en el mantenimiento del peso perdido.
Inicialmente debe animarse al paciente para realizar actividad física durante 30 a 45 minutos, de 3 a 5 días semanales. A largo plazo todos los adultos deberían establecer el objetivo de acumular 30 minutos o más de actividad física de moderada intensidad la mayoría de los días de la semana, incluso preferiblemente todos los días. Se recomienda la combinación de una dieta baja en calorías y un aumento de actividad física porque la reducción de peso que producen puede acompañarse, además, de disminución de la grasa abdominal y de aumento de la competencia cardiorrespiratoria.
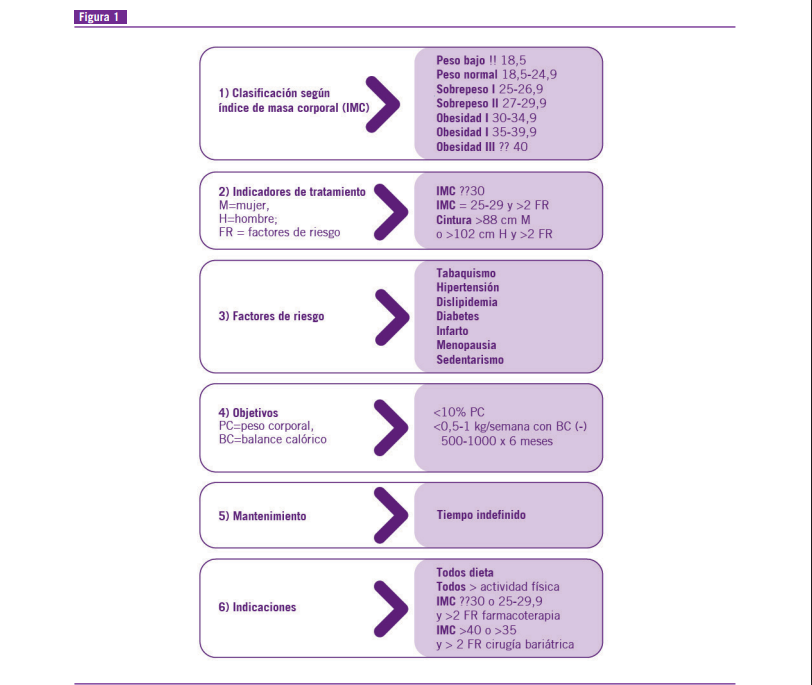
La terapia conductual constituye un complemento útil cuando se incorpora al tratamiento para la reducción y el mantenimiento del peso. Con objeto de tomar las medidas apropiadas para motivar al paciente es necesario que el médico valore su disposición para incorporarse al tratamiento y para ejecutar el plan. Los tratamientos cognitivos comportamentales generalmente incluyen 3 componentes: cambio en la dieta, aumento de la actividad física y técnicas de terapia cognitiva comporta- mental, tales como fijación de metas, automonitoreo y control de estímulos. Además de la pérdida de peso, el objetivo de las intervenciones es introducir cambios en el comportamiento y estilos de vida que aumenten la probabilidad de perder peso y mantenerlo. Un programa estándar de pérdida de peso incluye 12 a 16 sesiones que cubren estrategias específicas, como registro diario de alimentos y consumo de calorías, evitar desencadenantes para comida no saludable, aumento de la actividad física, obtener apoyos social y familiar y modificación de pensamientos y emociones que se contraponen a la pérdida de peso. Las intervenciones sobre el comportamiento generalmente reducen el peso entre 8% y 10% del peso inicial. Las anteriores medidas para la obesidad deben contemplarse cuando se tienen valores de IMC = 27 kg/m2, mientras que la farmacoterapia debería añadirse con un IMC = 30 kg/ m2 y otras comorbilidades; en tanto que con un IMC ≥ 35 kg/ m2 con comorbilidades o un IMC absoluto ≥ 40 kg/m2 debería contemplarse la posibilidad de una cirugía bariátrica, además de las técnicas de modificación de conducta para reducir la ingesta calórica y aumentar la actividad física, cuando esto fuera posible.
Fármacos y obesidad
Antidepresivos
Los antidepresivos varían considerablemente con respecto a su potencial de aumento de peso a largo plazo. En un reciente metaanálisis Serretti y Mandelli evaluaron el riesgo relativo de aumento de peso asociado a cada uno de los principa- les antidepresivos (21). La paroxetina es considerada como el ISRS que produce el mayor incremento a largo plazo en el peso corporal, en tanto que la amitriptilina es el más potente inductor de ganancia de peso entre los antidepresivos tricícli- cos y mirtazapina es el antidepresivo dual serotoninérgico y noradrenérgico que se asocia con el mayor aumento de peso a largo plazo. Otro antidepresivo tricíclico que se ha asociado con aumento de peso incluye la nortriptilina, mientras que el efecto de la imipramina parece ser neutral. Los ISRS como fluoxetina y sertralina se han asociado con pérdida de peso durante el tratamiento agudo (4-12 semanas) y con efecto neutro sobre el peso en la fase de mantenimiento (>4 meses). Para el citalopram y escitalopram no se pudo observar ningún efecto significativo en el peso corporal. Entre los duales inhibidores de la recaptación de serotonina y norepinefrina, la venlafaxina y la duloxetina aumentan ligeramente el peso corporal en el tratamiento a largo plazo, aunque los datos para la venlafaxina son escasos. El bupropión inhibe selectivamente la recaptación de la dopamina y, en menor medida, de la noradrenalina. Es el único antidepresivo que regularmente causa pérdida de peso. Originalmente, fue aprobado para tratar la depresión y para inducir el cese del tabaquismo. Durante los ensayos clínicos, se observó que suprimía el apetito y el antojo por alimentos, junto con lo cual disminuyó significativamente el peso corporal (22). En una revisión sistemática reciente solo se pudo demostrar aumento de peso con amitriptilina (1,8 kg) y mirtazapina (1,5 kg), en tanto que se observó pér- dida de peso con bupropión (-1.3 kg) y con fluoxetina (-1.3 kg). La evidencia de cambios en el peso asociada con los otros antidepresivos fue de baja calidad.
Antipsicóticos
Aunque son mejor tolerados que los antipsicóticos más antiguos, muchos de los nuevos agentes antipsicóticos atípicos tienen como efecto colateral frecuente el aumento de peso. Este aumento de peso resulta de interés clínico porque inter- fiere con el cumplimiento del paciente y tiene consecuencias perjudiciales para la salud en los pacientes que a menudo padecen sobrepeso u obesidad (23). El efecto diferencial de los antipsicóticos atípicos sobre los receptores de histamina (H1), los efectos anticolinérgicos y los efectos antagonistas sobre los receptores de serotonina tipo 2C pueden explicar las diferencias en ganancia de peso entre los diferentes antipsicóticos. Henderson et al. demostraron que la ganancia de peso asociada con la clozapina se prolongó durante 46 meses y se acompañó por un aumento significativo en los niveles de tri- glicéridos y un aumento de 37% en la incidencia de diabetes mellitus tipo 2 durante un período de 5 años de observación
(24). En un ensayo aleatorizado investigando la efectividad de cinco antipsicóticos se encontró que el aumento de peso > 7% desde el inicio de tratamiento se produjo en el 30% de los que tomaban olanzapina, en 16% de los que tomaban quetiapina, en el 14% de los que tomaban risperidona, en el 12% de los que tomaban perfenazina y en el 7% de las personas que tomaban ziprasidone (25). Los pacientes perdieron peso cuando se pasó de la olanzapina a ziprasidona, y esta pérdida de peso se asoció con mejorías en su tolerancia a la glucosa y en el perfil de lípidos. En un ensayo de 6 semanas, doble ciego, los pacientes fueron asignados aleatoriamente para recibir ziprasidona (n=136) u olanzapina (n=133). El peso corporal aumentó significativamente en aquellos que tomaron olanzapina (3,6 kg) en comparación con aquellos que toma- ron ziprasidona (1,0 kg) (26). Una revisión de nueve ensayos aleatorizados que comparaban ziprasidona con amisulprida, clozapina, olanzapina, quetiapina y risperidona demostró que ziprasidona produce menos aumento de peso que la olanzapina (5 ensayos controlados aleatorizados; n = 1659; con una diferencia media estimada de -3.82, IC 95% -4.69 a -2.96), quetiapina (2 ensayos controlados aleatorizados; n=754; con un riesgo relativo de 0,45; IC 95% 0,28 a 0.74), o risperidona (3 ensayos controlados aleatorizados; n = 1063; riesgo relativo 0.49; IC 95% 0.33 a 0,74). La ziprasidona también se asoció con menos aumento del colesterol que la olanzapina, quetiapina y risperidona (27). Finalmente, una revisión de 34 estudios clínicos de antipsicóticos en jóvenes con psicosis y trastorno bipolar encontró que el aumento de peso varió de 3.8 a 16,2 kg con olanzapina, 0.9 a 9.5 kg con clozapina, 1,9 a 7,2 kg con risperidona, 2.3 a 6.1 kg con quetiapina y 0 a 4,4 kg con aripiprazol. A pesar del efecto variable en la ganancia de peso entre los agentes antipsicóticos, el efecto prodiabético puede ser similar para todos los antipsicóticos a través de mecanismos independientes del peso.
Antirecurrenciales (AR)
Los AR asociados con pérdida de peso son el felbamato, topiramato y zonisamida, en tanto que los AR asociados con aumento de peso son gabapentina, pregabalina, ácido valproico, vigabatrina y carbamazepina. Los AR neutros para el aumento de peso son lamotrigina, levetiracetam y fenitoína. En la práctica clínica, es fundamental pesar a los pacientes con regularidad y la selección de AR debe basarse en el per- fil de cada paciente sin sacrificar la eficacia terapéutica. El ácido valproico ha demostrado causar aumento de peso en adultos y niños. Un estudio retrospectivo a largo plazo sobre aumento de peso en pacientes epilépticos adultos en mono o politerapia con ácido valproico demostró un aumento de peso de leve a moderado (5 a 10% del peso inicial) en el 24% de los pacientes, mientras que un aumento de peso marcado (> 10% ganancia del peso inicial) fue demostrado en el 47% de los pacientes (27,28). En un estudio sobre pacientes que tomaron gabapentina durante 12 meses o más se mostró que de los 44 pacientes, 57% ganó más del 5% del peso corporal basal; de estos, 10 pacientes (23%) obtuvo más del 10% de su peso inicial. En una revisión sistemática se documentó un aumento de peso con gabapentina de 2,2 kg después de 1.5 meses de uso, y para divalproex un riesgo relativo de aumento de peso de 2.8 (IC 95%: 1.30 a 6.02) (29). Carbamazepina es uno de los AR más antiguos y también se ha asociado con aumento de peso, aunque no tan importante como el ácido valproico o gabapentina. En un estudio de 66 pacientes que tomaron AR se demostró que 66.7% de los que tomaron car- bamazepina tuvo una media de aumento de peso de 1,5 kg a lo largo de un seguimiento de 6 a 8 meses (30).
Miscelánea
Hay una gran variedad de otras clases de drogas aprobadas para usos específicos que se han utilizado, sin embargo, para promover pérdida de peso en pacientes obesos. Las categorías de estas drogas incluyen a los anticonvulsivos como topira- mato y zonisamida. Zonisamida en un estudio aleatorizado doble ciego de 1 año sobre 225 pacientes zonisamida 200 g redujo –4.4 kg (–3.9%) y zonisamida 400 mg redujo –7.3 kg
(–6.8%) comparado con –4.0 kg (–3.7%) para placebo (31).
El topiramato ha sido comercializado para el tratamiento de epilepsia y profilaxis de migraña, en tanto para reducción de peso en pacientes obesos con o sin diabetes 2 e hipertensión arterial. En un ensayo aleatorizado de 56 semanas, se compa- raron dosis de 7.5 mg fentermina/46 mg topiramato y 15 mg fentermina/92 mg topiramato. A las 56 semanas, el cambio en peso fue –1.4 kg (–1.2%), –8.1 kg (–7.8%) y –10.2 kg (–9.8%) respectivamente para placebo, fentermina 7.5/topiramato 46 mg y fentermina 15 mg/topiramato 92 mg, con un descenso de >10% de peso para el 7%, 37% y 48% de los participantes en cada uno de los 3 grupos. Los efectos adversos fueron sequedad bucal, parestesias, constipación, insomnio y mareos, además de disgeusia, y ansiedad (32). Los hipoglucemiantes como la metformina (33), agonistas de GLP-1, exenatida y liraglutida (34), antidepresivos como bupropión (35), además de fármacos empelados para el trastorno por déficit de atención e hiperactividad como el metilfenidato (36) y, finalmente, las hormonas tiroideas (37) junto con betahistina (agonista H1/antagonista H3) especialmente controlando los efectos obesogénicos de los antipsicóticos atípicos (38). Los tratamientos combinando una o más de estas drogas no siempre cuentan con evidencia de alto nivel respaldando su uso, aunque su beneficio se ha documentado en reportes de caso. Si se decide prescribir un medicamento para la pérdida de peso que no esté aprobado para esta indicación por la FDA o no esté aprobaron para su administración crónica, se debe- ría advertir a los pacientes que este tratamiento no ha sido evaluado para seguridad y eficacia y no está aprobado por la FDA. Esta intervención y los detalles de los riesgos y beneficios de la estrategia sugerida de tratamiento deben documentarse en el expediente médico. El proveedor debe seleccionar en primer lugar medicamentos aprobados para bajar de peso y en caso de optar por otra estrategia se debería discutir los pro y contra junto con el paciente y justificar el por qué un medicamento fuera de aprobación fue el elegido. Las prácticas de venta de medicamentos para pérdida de peso de manera privada deberían evitarse porque podría interpretarse como un conflicto de intereses para el proveedor.
Mecanismo de acción de los agentes farmacológicos
De acuerdo con un reciente artículo sobre obesidad y su manejo farmacológico, los nuevos tratamientos antiobesidad deben apuntar hacia diferentes factores. Se requiere identi- ficar fármacos que puedan selectivamente afectar el deseo y disfrute de comer, la plenitud y satisfacción. Las intervencio- nes diseñadas específicamente para modular estos procesos podrían ayudar a reducir la experiencia aversiva de la dieta y maximizar la capacidad de privilegiar la pérdida de peso por sobre el apetito. Se sabe muy poco sobre los efectos comportamentales de los fármacos antiobesidad en desarrollo, y existen pocas certezas sobre la eficacia de los nuevos tratamientos para tratar las causas subyacentes de la obesidad (39). Los fármacos para el tratamiento de la obesidad se clasifican, de acuerdo con sus mecanismos de acción, en 3 grandes categorías:
a) reducción de la ingesta calórica;
b) modificación del metabolismo intermediario y
c) aumento del gasto calórico.
Agentes noradrenérgicos
Norepinefrina (NE): puede incrementar o disminuir la ingesta calórica dependiendo del sitio de acción. La acción de NE sobre receptores adrenérgicos tipo 1 localizados en neuronas del núcleo ventro-medial del hipotálamo disminuye la ingesta de alimentos. Los antagonistas de receptores adrenérgicos 1 y agonistas de 2 aumentan el peso, como terazozin. Los agonistas de receptores 2-adrenérgicos en el área perifornical, en cambio, disminuye la ingesta calórica y tiene un reducido efecto termogénico, como terbutalina, clembuterol y salbutamol. Los agonistas de receptores adrenérgicos 3 reducen la ingesta calórica a nivel central y periférico y estimulan débilmente la termogénesis. Los fármacos noradrenégicos, con excepción de mazindol, se derivan de la -feniletilamina, cuya estructura química es similar a los neurotransmisores dopamina, epinefrina y norepinefrina. El fármaco prototipo de este grupo es la anfetamina. La modificación de la estructura de -feniletilamina permite la obtención de una amplia gama de compuestos con diversas respuestas farmacológicas incluyendo la liberación de NE y dopamina de las vesículas presinápticas (benzfetamina, fendimetrazina, fentermina, y dietilpropión), la inhibición de la recaptación de NE (mazin-dol) (40) o la acción agonista sobre receptores adrenérgicos (fenilpropanolamina). Estos agentes reducen el peso corporal entre un 3 a 8% comparado con placebo y más del 5 % del peso corporal inicial, sin embargo, la posibilidad de desarrollar adicción, tolerancia y múltiples efectos adversos como xerostomía, constipación, insomnio, euforia, palpitaciones, arritmias, hipertensión arterial, isquemia miocárdica y valvulopatías los convierte en poco confiables y de uso limitado para el tratamiento crónico de la obesidad.
Fenilpropanolamina (1R, 2S)-2-amino-1-fenil-propan-1-ol): es agonista de los receptores alfa- y beta-adrenérgicos y agonista parcial de los receptores dopaminérgicos D1. Fue retira- da del mercado por aumentar el riesgo de ictus hemorrágico en mujeres jóvenes (41).
Fentermina (1,1-Dimetil-2-Fenietliamina): es un derivado-fenil-amínico con perfil simpaticomimético que actúa en el núcleo para ventricular del hipotálamo a través de la interacción con 2 tipos de receptores 1 y 2. Es agonista de receptores noradrenérgicos y dopaminérgicos y suprime las señales de hambre y apetito. La fentermina fue aprobada para el tratamiento de la obesidad en el corto plazo, pero no en forma crónica, lo cual representa un obstáculo para los clínicos dado que es probable que ocurra una ganancia de peso luego de su suspensión. Para ello se lo puede emplear en forma intermitente lo que funciona mejor si el paciente está expuesto a factores ambientales circunstanciales que promueven ganancia de peso. Es, actualmente, el fármaco más prescripto para reducir el peso, asociado a su bajo costo comparativo (42). No hay datos fiables sobre seguridad a largo plazo aunque algunos datos recientes sobre 269 pacientes tratados sugieren un bajo potencial adictivo (43). Una dosis de 15 mg diaria es ca- paz de reducir > 7% el peso a los 6 meses. La dosis de inicio es de 7.5 mg que puede aumentarse progresivamente hasta
15 mg/d o más si no se obtienen beneficios significativos. Se sugiere un seguimiento mensual durante la escalada de dosis y luego cada 3 meses durante la fase de mantenimiento. Se prescribe con frecuencia fuera de indicación (off-label) por periodos largos de tiempo (6-12 meses) (44). Se administra a la dosis de 37,5 mg por la mañana (antes o 1-2 horas después del desayuno, pero no a última hora de la tarde). Hay pocos ensayos clínicos controlados en monoterapia con una duración ≥6 meses y los que describen sus efectos a largo plazo sobre los factores de peso cardiovascular incluyen muy pocos pacientes. En un ensayo doble ciego de 36 semanas de duración, la fentermina producía una pérdida de peso de 12,2 kg (4,8 kg el placebo) (45) y en un metaanálisis de 6 estudios de entre 2 y 24 semanas de duración, la fentermina (15-30 mg/d) producía una pérdida de peso adicional en relación a placebo de 3,6 kg, siendo la pérdida media del peso total de 6,3 kg (46). En otro ensayo controlado con placebo realizado en mujeres obesas tratadas con 30 mg de fentermina diaria- mente o de forma intermitente (en meses alternos) durante 36 semanas, la reducción del peso era similar con ambas pautas de tratamiento (12,2 y 13,0 kg, respectivamente, vs 4,8 kg con placebo). Cerca del 51% de los pacientes abandonaron el tratamiento (8% en el grupo placebo) debido a reacciones adversas centrales (47). Además, fentermina produce taquicardia y aumenta la presión arterial, estando contraindicado su uso en pacientes con enfermedades cardiovasculares o con glaucoma. Los efectos secundarios comprometen el sis- tema nervioso central (estimulación, inquietud, nerviosismo, insomnio, temblores, mareos y cefaleas, raramente euforia seguida por fatiga y depresión, los episodios psicóticos y alucinaciones), el aparato cardiovascular (disnea de esfuerzo, taquicardia, palpitaciones, hipertensión, dolor precordial, ac- cidentes cerebrovasculares, hipertensión pulmonar primaria, angina, infarto de miocardio, insuficiencia cardiaca y paro cardiaco), aparato gastrointestinal (náuseas, vómitos, boca seca, dolores abdominales, gusto desagradable, diarrea, constipación), trastornos en la micción, rash, impotencia, cambios de la libido, edema facial. Las contraindicaciones para su uso están dadas por la presencia de hipertensión arterial pulmonar, hipertensión arterial, enfermedad cerebrovascular, hipertiroidismo, manía o depresión, glaucoma, uso concomitante de IMAO.
Dietilpropión (±)-2-(dietil-amino)-1-fenilpropan-1-ona): su mecanismo de acción es similar al de los otros supresores del apetito, pero sus efectos son más débiles que la dextro-anfetamina, la cual es de hecho 6 a 11 veces más fuerte que el dietilpropión cuando se administra por vía oral, y 10 a 20 veces más fuerte cuando se administra por inyección subcutánea. El dietilpropión (a través de la elevación de catecolaminas) eleva indirectamente los niveles de leptina e inhibe al neuropéptido Y (orexígeno). Tiene un bajo potencial adictivo dado que su actuación principal es a nivel hipotalámico. Se emplea habitualmente como complemento de restricción calórica en el tratamiento a corto plazo (6 semanas) de la obesidad exógena y con IMC inicial ≥ 30 kg/m2 que no han
respondido a la dieta y/o ejercicio. Se administra a corto plazo en monoterapia para obesidad, y también se lo ha empleado para reducir el craving por cocaína y aliviar el dolor de artritis de rodilla. La dosis habitual es de 25 mg tres veces al día; 75 mg al día de una formulación de liberación controlada) con una eficacia y seguridad similar a la de la fentermina. En un estudio aleatorizado los participantes obesos que recibieron un dosis de 75 mg de dietilpropión durante 6 meses tuvieron una reducción del peso corporal del 9,8 % y del 10,6% y al cabo de 6 y 12 meses de tratamiento, respectivamente en comparación con el 3,2% del grupo placebo. En un metaanálisis de 9 estudios con un reducido número de pacientes y un seguimiento de entre 6 y 52 semanas, dietilpropión (75 mg/d) producía una pérdida media de peso de 6,5 kg (3 kg con placebo) (48). Tanto fentermina y dietilpropión también producen una reducción de peso significativa cuando se utilizan de forma intermitente (en meses alternos). Sus efectos adversos incluyen aumento (leve) de la frecuencia cardiaca o la presión arterial y, por ello, es una buena opción para los pacientes con presión arterial alta. Otros efectos adversos incluyen mareos, sequedad de boca y estreñimiento. Otros como euforia, temblores musculares o dificultad para dormir se observaron en un 3%. Como efectos adversos mayores se mencionan accidente cerebrovascular y ataques isquémicos transitorios, ginecomastia y en algunos casos se desarrolla psicosis de tipo orgánico. Debido a su potencial adictivo no debe prescribirse a personas con antecedentes de abuso de drogas, especialmente debido al desarrollo de tolerancia a las acciones estimulantes de la droga. El dietilpropión no está recomendado para uso en niños menores de 12 años. Al interactuar con alcohol aumenta las sensaciones de estimulación, con IMAO está contraindicada, dado que puede producir crisis hipertensivas graves, además la administración posterior o previa a un IMAO debe hacerse mínimo con 14 días de intervalo entre ambos fármacos. Con bloqueadores beta puede estimular receptores a-adrenérgicos y amplificar los efectos colaterales asociados a su estimulación. Con antidepresivos tricíclicos se pueden presentar arritmias cardiacas, retención urinaria, constipación. Con fenotiazinas atenúan o anulan sus efectos. Con digital causa arritmias. No debe administrarse durante el embarazo ni lactancia.
Benzafetamina (N-Benzil-N, a-dimetilobenzenoetanamina):
se transforma en el organismo en anfetamina y metanfetami- na, por lo que presenta el riesgo de abuso (pertenece al grupo III del U.S. Controlled Substance Act). Se administra en dosis de 25 y 50 mg 1-3 veces al día, en dos estudios de 12 semanas de duración producía una pérdida de peso similar al de la fentermina (35). La fendimetrazina (35 mg 2-3 veces al día; 105 mg por la mañana de una formulación de liberación retardada) presenta una eficacia y seguridad similares a las de fentermina. Al igual que la benzafetamina pertenece al grupo III del U.S. Controlled Substance Act y ambos fármacos están contraindicados durante el embarazo.
Agentes serotoninérgicos
Dexfenfluramina y fenfluramina (N-etil-1-[3-(trifluorometi- l)-fenil] propan-2-amina): tienen actividad agonista de receptores serotoninérgicos (d-norfenfluramina y clorofenilpiperazina). Los receptores 5-HT1 y 5-HT2 están involucrados de modo principal en la regulación del balance energético. La estimulación de receptores tipo 5-HT1A del núcleo del rafe dorsal estimula la ingesta de alimentos en tanto que los agonistas de receptores 5-HT1B/2C disminuyen los niveles de neuropéptido Y (NPY) y, por tanto, reducen la ingestión calórica. Al igual que los agentes noradrenérgicos, los fármacos serotoninérgicos tienen acciones agonista y de bloqueo de la recaptación, pero carecen de efectos estimulantes y adictivos. La fenfluramina es una mezcla racémica y dexfenfluramina su dextroisómero. Estas drogas producen disminución de 6 al 10% del peso corporal después de 1 año con mejora de las comorbilidades asociadas a la obesidad, tales como insuli- no-resistencia e intolerancia a la glucosa, que fueron independientes de la pérdida de peso. Sin embargo, el desarrollo de tolerancia después de los 6 meses (efecto meseta) y otros efectos adversos como exacerbación de la manía, pérdida de la memoria e hipertensión pulmonar y valvulopatías promovieron su retiro del mercado (49, 50).
Lorcaserina: es un agente serotoninérgico agonista de los receptores 5-HT2c que en el hipotálamo modulan la ingesta de alimentos mediante la activación del sistema de la propio- melanocortina, induciendo una reducción del apetito. Al igual que fenfluramina y dexfenfluramina, lorcaserina actúa sobre los receptores 5-HT2b, pero con menor afinidad. En diversos estudios preclínicos y clínicos, la lorcaserina, en dosis de 10 y 15 mg una vez por día y 10 mg dos veces por día, redujo el peso corporal > 5% del peso basal a las 4 y 12 semanas de duración (51). Su seguridad y eficacia se evaluaron en tres estudios aleatorizados, controlados con placebo que incluyeron a casi 8.000 pacientes obesos y con sobrepeso, con y sin diabetes tipo 2. En comparación con el placebo, el tratamiento durante un año estuvo asociado con una reducción promedio del peso del 3% al 3,7%. Hubo un 23% de pacientes que perdió el 10% de su peso inicial.
Agentes histaminérgicos
Betahistina: betahistina [N-metil-2-(piridina-2-il)-etanamina] es un agonista parcial H1 y antagonista de receptores H2 y H3 pre-sinápticos produciendo su regulación decreciente. Dado que el receptor H1 post sináptico se encuentra en el núcleo periventricular y el hipotálamo ventromedial y H3 es un autoreceptor inhibitorio y regula la secreción de histamina y otros neurotransmisores, betahistina puede inhibir la ingesta alimentaria actuando sobre dichos receptores. Se absorbe rápidamente por vía oral y se metaboliza a ácido 2-piridilacé- tico (2-PAA) (sin actividad farmacológica), alcanzando su pico máximo 1 hora después de la ingesta, con una vida media de
3.7 horas y una unión a proteínas plasmáticas menor a 5%. Tiene una farmacocinética lineal sin saturación metabólica. Se emplea habitualmente en el tratamiento de la enfermedad de Meniere y en algunos estudios ha reducido la ganancia de peso asociada con olanzapina. Es una molécula bien tolerada y no se asocia habitualmente con abandonos de tratamiento por efectos colaterales. Puede ser una estrategia segura y relativamente económica para el manejo del aumento de peso especialmente en pacientes tratados con quetiapina (52).
Agentes duales (noradrenérgicos/serotoninérgicos)
Sibutramina: fue sintetizada en 1980 para ser empleada como antidepresivo, pero se encontró que reduce la inges- ta de alimento en animales de experimentación incremen- tando la termogénesis. Sibutramina es una amina terciaria (N-[1-[-(4-clorofenil) ciclobutil]-3-metilbutil)-n, n-dimetila- mina-monhidrato-clorhidrato) que se desdobla en 2 compues- tos farmacológicamente activos (aminas secundarias) y se me- taboliza en el hígado por desmetilación. In vitro es un potente inhibidor selectivo de la recaptación de noradrenalina (NE), serotonina (5-HT) y Dopamina (DA). Sin embargo, estos efec- tos son indirectos, porque in vivo, sibutramina se comporta como un débil inhibidor de la recaptación de monoaminas comparado con desipramina, imipramina, nomifensina y amitriptilina. La sibutramina y sus metabolitos activos no estimulan la liberación de NE, 5-HT o DA, lo cual la diferencia de dexfenfluramina y D-anfetamina; carece de actividad sobre la enzima MAO y presenta afinidad por una amplia variedad de receptores: 1, 2, 3 adrenérgicos, receptores de serotonina 5-HT1A, 5-HT1B, 5-HT2A, 5-HT2B, 5-HT2C, receptores de dopamina D1, D2, receptores muscarínicos, histaminérgicos tipo H1 y de benzodiazepinas (53). El principal mecanismo de acción farmacológico de sibutramina es como inhibidor de la recaptación y agonista de receptores adrenérgicos y sobre todo serotoninérgicos tipo 5-HT2B y 5-HT2C situados en el núcleo arcuato del hipotálamo. Como resultado inhibe la liberación
del neuropéptido Y (NPY) y disminuye la ingesta de alimentos. A diferencia de los compuestos anfetamínicos que reducen el apetito, sibutramina reduce la ingesta de alimentos prolongando la saciedad. La dosis oscila entre 10 y 15 mg diarios una vez al día generalmente en la mañana. En caso de buena respuesta (pérdida ponderal > 2 kg en 4 semanas) se continuará con la misma dosis. En caso de respuesta insuficiente (pérdida ponderal < 2 kg en 4 semanas) se puede incrementar la dosis a 15 mg/d, siempre que haya habido buena tolerancia a la dosis anterior. En caso de respuesta insuficiente a 15 mg/d de sibutramina (pérdida ponderal <2 kg en 4 semanas) se suspenderá el tratamiento. La continuidad del tratamiento corresponde solamente para los pacientes que reduzcan > 5% del peso corporal inicial en 3 meses de tratamiento farmacológico y en los que mantengan en adelante pérdidas > 5% de su peso inicial. Duración del tratamiento: hasta un máximo de un año, y no deben existir contraindicaciones clínicas o psicológicas. El tratamiento con sibutramina debe suspenderse cuando la disminución de peso sea < 5 Kg en 3 meses o se recuperen >3 Kg después de haber adelgazado o tras un año de tratamiento continuo. La eficacia del tratamiento con sibutramina se basa en una reducción de 6-10% con respecto al peso corporal inicial, con recuperación de peso después de 18 meses en menor porcentaje con respecto al placebo; además mejora el perfil metabólico por disminución de glicemia basal, insulina, péptido C, HbA1c, ácido úrico, triacilglicéridos y VLDLc, sin disminución de LDLc ni aumento de HDLc. Los efectos secundarios son leves a moderados en las primeras 4 semanas de tratamiento. Los más frecuentes son boca seca, náuseas, mareos, constipación, insomnio y cefalea. Dentro de los efectos adversos sobre el sistema cardiovascular se encuentran aumento de la presión arterial sistólica y diastólica (+/- 2 mmHg dosis de 10-15 mg) taquicardia y palpitaciones por el aumento del gasto cardiaco (6-13 latidos por minu- to), sin asociarse a infarto miocárdico o accidente cerebro- vascular, por lo cual, la presión arterial y el pulso deben ser cuidadosamente monitoreados en los pacientes obesos con hipertensión que inician la farmacoterapia con sibutramina pues en las primeras 8 semanas de tratamiento se reportan elevaciones de estos parámetros. No se han descrito efectos adversos como hipertensión pulmonar, valvulopatía, adicción y/o síndrome de abstinencia; si se ha descripto en algunos pacientes el desarrollo de amnesia. No debe considerase la utilización de sibutramina en pacientes con historia de enfermedad cardiovascular, hipertensión, enfermedad cerebrovascular, trastorno bipolar, insuficiencia renal o hepática; ni en pacientes en tratamiento con fármacos inhibidores de la MAO, o que sean metabolizados por citocromo p450, como ketoconazol, eritromicina y cimetidina, entre otras. La sibutramina ha sido retirada del mercado a partir del 2010 debido a sus efectos perjudiciales sobre el aparato cardiovascular.
Modificación del metabolismo intermediario
Orlistat (tetrahidrolipstatina): es el único inhibidor de la absorción intestinal de grasa aprobado por la FDA, para el tratamiento de la obesidad. Se trata de un derivado hidrogenado (liptastina) producido por streptococcus toxutricini. Este componente altamente lipofílico, actúa como un potente inhi- bidor de la mayoría, sino todas, las lipasas de mamíferos. Se administra a una dosis de 120 mg tres veces con las comidas. Orlistat actúa en la cavidad gástrica y en la luz del intestino delgado formando un enlace covalente con el sitio activo de las lipasas gástrica y pancreática, inhibiendo la escisión de los triacilglicéridos en ácidos grasos libres y monogliceroles absorbibles, de tal manera que 30% de las grasas ingeridas se eliminan junto a las materias fecales, resultando en un déficit calórico, que promueve la pérdida de peso. En estudios aleatorizados doble ciego controlados con placebo, los pacientes tratados con orlistat, mostraron una reducción de peso entre 8,5 y 10,2 % con respecto al peso corporal inicial, durante el primer año (grupo placebo 5,5- 6,6%). En el segundo año, la pérdida de peso con Orlistat se mantuvo superior al 5% (7,6 y 7%), en contraste al grupo placebo (4,5-7,6%); demostrándose una reducción gradual y mantenida durante el primer año, y una ganancia ponderal de rebote más lenta (53). A diferencia de sibutramina, orlistat disminuye los niveles de LDL en un 4-11% además del colesterol total, triacilglicéridos
y cifras tensionales. Muestra además mejoras en los niveles de glicemia basal y pospandrial, HbA1c e insulina, contribuyendo al control de los pacientes diabéticos obesos. Debido a su alta liposolubilidad, la absorción de orlistat es mínima (1%), siendo su principal vía de eliminación la excreción fecal. La porción absorbida sufre metabolismo gastrointestinal, que origina 2 metabolitos (M1 y M3) farmacológicamente inactivos, los cuales se excretan por vía biliar. Debido a su mecanismo de acción, disminuye la absorción de vitaminas liposolubles y análogos (A, D, E, y K), por lo cual deben administrarse suplementos de estos, 2 horas antes o después del empleo del fármaco (54). En virtud de su mínima absorción, orlistat no afecta las propiedades farmacocinéticas de digoxina, fenitoína, warfarina, gliburide, anticonceptivos orales, alcohol ni tampoco de antihipertensivos como furosemida, captopril, atenolol y nifedipino. Sin embargo, se debe tener cuidado al administrar orlistat conjuntamente con pravastatina y cliclosporina porque aumenta la disponibilidad de las mismas así como sus efectos farmacológicos. Sus principales efectos secundarios son gastrointestinales y se manifiestan durante las primeras 6 semanas de tratamiento, después de las cuales desaparecen o son bien tolerados. Estos incluyen: dolor abdominal, aumento de la frecuencia de defecaciones (11%), flatulencia (24%) manchas oleosas (27%) urgencia
fecal (22%) esteatorrea (20%) e incontinencia fecal (8%);todos los cuales aumentan con el mayor consumo de lípidos en las comidas.
Metformina: este agente derivado de las biguanidas produ- ce pérdida de peso por múltiples mecanismos entre los cuales se cuenta un cambio fenotípico inducido por la proteinqui- nasa de nicotinamida activada sobre la fosforibosil-transfera- sa-sirtuina-1, la cual media los cambios en el metabolismo y la reducción de peso. En el programa de prevención de Dia- betes la metformina (850 mg 2 x día) produjo una reducción de peso de 2.1 kg comparado con 0.1 kg en el grupo placebo. Otro estudio reciente comparando sitagliptina más metfor- mina con pioglitazona en pacientes con DM2 mostró que la combinación sitagliptina-metformina redujo el peso (>1.4 kg) mientras que pioglitazona aumentó el peso (3.0 kg) (55,56). Exenatida y liraglutida: estos agentes son agonistas de GLP-1 y promueven una pérdida moderada de peso. Un análisis re- trospectivo de exenatida (n = 6280), sitagliptina (n = 5861), e insulina (n = 3398) indicó que el grupo exenatida perdió un promedio de 3.0 kg, el grupo sitagliptina perdió 1.1 kg, y el grupo insulina ganó peso (0.6 kg). Todos los agonistas GLP-1 también reducen el nivel de HbA1c cerca del 1%. En un ensayo de un año comparando dos dosis de liraglutida (1.2 y 1.8 mg) con glimepirida 8 mg, los sujetos perdieron 2.05 y 2.45 kg en los grupos de liraglutida de 1.2- y 1.8-mg, respectivamente, comparados con 1.12-kg de ganancia de peso en el grupo glimepirida. La hemoglobina glicosilada (HbA1c) disminuyó 0.84% con liraglutida 1.2 mg (P = .0014) y 1.14% con liraglutida 1.8 mg (P = .0001) comparadas con 0.51% con glimepirida. Un análisis de 17 ensayos controlados alea- torizados doble ciego mostró que todos los agonistas GLP-1 redujeron los niveles de HbA1c cerca de 1% (57).
Pramlintida: este es un análogo de amilina que reduce el peso aumentando la saciedad y disminuyendo la ingesta ca- lórica. Indicada como adjunto a la insulina puede ayudar a la pérdida de peso. Un metaanálisis demostró una pérdida de peso de -2.57 kg para el grupo pramlintida vs el grupo control (58).
Acarbosa y miglitol: son inhibidores de glucosidasa y tienen efectos mínimos o neutros sobre el peso (59, 60).
Sitagliptina y vildagliptina: son inhibidores de DPP-4 y ade- más de reducir la ingesta y el peso, también lo hacen con la HbA1c. En un metaanálisis de 25 estudios sitagliptina y vil- dagliptina redujeron la HbA1c aproximadamente 0.7 y 0.6%, respectivamente, en comparación con placebo (61). En una revisión reciente de comparaciones directas entre agentes hipoglucemiantes los inhibidores DPP-4 redujeron la HbA1c discretamente menos que metformina (aproximadamente 0.28%) y tuvieron similares efectos hipoglucemiantes que las tiazolidinadionas (62). Los inhibidores DPP-4 tienen mejor tolerancia gastrointestinal que la metformina y tienen un efec- to neutral sobre el peso (63). Otro metaanálisis encontró un aumento del peso corporal (1.8 a 3.0 kg) con la mayoría de las terapias de segunda línea con la excepción de los inhibi- dores DPP-4, inhibidores de la -glucosidasa, y los análogos de GLP-1 (+0.6 a -1.8 kg) (51).
Dapagliflozina y canagliflozina: los inhibidores de SGLT-2 son una nueva clase de hipoglucemiantes que reducen la re- absorción renal de glucosa en el túbulo contorneado proximal y aumentan la excreción urinaria de glucosa. En un reciente metaanálisis evaluó los efectos de estos medicamentos en la glicemia y en el peso corporal comparados con placebo. El porcentaje medio de cambio en el peso corporal desde la línea de base en 8 estudios de > 12 semanas comparando los inhibidores de SGLT-2 con placebo fue -2.37% (IC 95% -2.73 a -2.02). Canagliflozina produce ligeramente más pérdida de peso debido a que 3 estudios con dapagliflozina vs placebo mostraron una pérdida media de peso de -2.06% (IC 95 % -2.38 a -1.74), y 5 estudios de canagliflozina vs placebo mostraron una pérdida media de peso de -2.61% (IC 95% -3.09 a -2.13); sin embargo, no fue una diferencia estadísticamente significativa (64). Estos análisis podrían haber subestimado los efectos sobre la pérdida de peso de estas drogas dado que los estudios incluidos fueron de 12 semanas (65). En obser- vaciones de 52 semanas no hubo ganancia de peso después de la pérdida máxima a las 24 semanas. Además, debido a que las medicaciones para reducir el peso no producen hipo- glicemia de manera independiente, tienen un menor potencial para complicar un programa de ejercicios.
El ajuste de la intensidad de ejercicio solamente se requiere para insulina y medicamentos que pueden promover la secre- ción endógena de insulina a pesar de que la glicemia este baja, tal como es el caso para las sulfonilureas y agentes de- rivados de glinidas. De lo anterior surge que priorizar el uso de metformina, medicamentos derivados de incretina y SGLT- 2 como agentes terapéuticos pueden reducir la hipoglicemia potencial por ejercicio y aumentar la seguridad y eficacia del ejercicio en pacientes con diabetes, reforzando las estrategias de pérdida de peso.
Aumento del gasto calórico
Rimonabant (N-(Piperidin-1-il)-5-(4-clorofenyi) -1-(2,4-di- clorofenyi) -4-metil-1H-pirazol-3-carboxamida): fue descubierto en 1994 para el tratamiento de la obesidad debido a su efecto antagonista selectivo del receptor CB1; evitando o revirtiendo los efectos inducidos por su estimulación in vivo e in vitro. Tiene una afinidad para CB1 1000 veces mayor que para CB2. Inicialmente, se pensó que dichos efectos eran debidos al antagonismo de los cannabinoides endógenos como la anandamida (localizada en sistema nervioso central, adipocito e intestino), pero recientemente se descubrió que rimonabant posee actividad agonista inversa. Sus efectos centrales son mediados por endo cannabinoides agonistas de CB1; otras funciones son periféricas e incluyen: (a) regulación de la ingesta, actuando en centros hipotalámicos ya sea en forma directa o a través de CCK, CRH, NPY, oxitocina o leptina; (b) control endócrino activando la secreción de ACTH y glucorticoides, e inhibiendo la liberación de gonadotropinas, GH, prolactina y TSH; (c) regulación de la microcirculación a través de sus acciones sobre la hematopoyesis. La administración de rimonabant durante 7 días demostró reducir la ingesta alimentaria, la sensación de hambre y el peso corporal en hombres con sobrepeso y obesos. Sin embargo, el efecto específico de rimonabant sobre el apetito (reduciendo el valor hedónico de los alimentos y su palatabilidad, o aumentando la sensación de saciedad) no ha sido aún completamente es- clarecido. Por otra parte, en pacientes obesos de alto riesgo o pacientes con sobrepeso más dislipidemias, se demostró que incrementa significativamente las HDL, la sensibilidad a la insulina y disminuye los niveles plasmáticos de triacilglicéridos y aumenta significantemente los niveles de adiponectina. Un estudio reciente demostró que rimonabant es capaz de inhibir la proliferación y retrasar la maduración de preadipocitos de ratón en cultivo; esta pudiese ser una propiedad adicional de rimonabant como compuesto anti obesidad, particularmente asociado al efecto reductor de masa corporal grasa. Rimonabant ejerce un efecto directo en el consumo de energía asociado a un aumento en la producción de calor (termogénesis). Rimonabant fue retirado del mercado en 2008, luego que el Comité para Productos Médicos de Uso Humano (CHMP) de la Agencia Europea de Medicamentos concluyó que los riesgos de su consumo superaban a sus beneficios potenciales, principalmente por haberse detectado un aumento significativo de casos notificados de trastornos psiquiátricos severos, depresión, incremento de pensamientos suicidas y suicidio consumados.
En la tabla 1 se muestran los principales fármacos emplea- dos para el tratamiento de la obesidad en pacientes psiquiátricos (Tabla 1).
DOSIS
Para las medicaciones aprobadas para uso crónico en obesidad se recomiendan las siguientes dosis:
- Orlistat: 120 mg 3 veces por día;
- Fentermina: 30 mg por día (37.5 mg como resina)
- Fentermina / topiramato: 7.5 mg/46 mg por día comen- zando con 3.75 mg/23 mg una vez por día durante 2 semanas. Si se tolera adecuadamente se incrementa a 7.5 mg/46 mg y se aumenta en caso de que no haya repuesta como descenso de >3% del peso a las 12 semanas hasta 11.25 mg/69 mg, y luego hasta 15 mg/92 mg. Para la suspensión del medica- mento se aconseja una supresión gradual durante una semana ya que la suspensión brusca de topiramato puede producir convulsiones especialmente en pacientes con epilepsia;
- Lorcaserina: 10 mg 2 veces por día, aunque en algunos ensayos clínicos la dosis de 10 mg una vez por día produjo casi tanto descenso de peso como una dosis de 2 por día.
- Naltrexona / bupropión: 8 mg/90 mg, 2 veces por día. Se debe comenzar con una tableta a la mañana y en 1 semana se agrega una tableta antes de la cena. Si se tolera se puede aumentar la dosis a 2 tabletas en la mañana en la tercera se- mana y 2 tabletas antes de la cena en la cuarta semana hasta un máximo de 2 tabletas 2 veces por día. Si se desarrollan efectos adversos como náuseas durante la escalada de dosis se debe aumentar más gradualmente. Si el paciente no ha perdido > 5% del peso a las 12 semanas se debe suspender.
- Liraglutida: 3.0 mg SC una vez por día. Se debe comen- zar con una dosis de 0.6 mg por día en inyección subcutánea. Se puede aumentar gradualmente 0.6 mg por semana has- ta un máximo de 3.0 mg. Si se desarrollan efectos adversos como náuseas durante la administración se debe aumentar la dosis más gradualmente.
Implementación de la farmacoterapia en situaciones clínicas y dosis
Si tenemos un paciente con antecedentes cardiacos, hiper- tensivos o convulsiones no convendría usar fentermina o die- tilpropión, ya que ambos se asocian con hipertensión arterial y taquicardia o convulsiones. Un agonista de receptor sero- toninérgico HT2c y HT2b como lorcaserina sería una mejor opción para un paciente cardiaco. Un paciente con obesidad y depresión que estuviera tomando IRSS (inhibidores selectivos de recaptación de serotonina) o IRSN (inhibidores selectivos de recaptación de serotonina y noradrenalina duales) la lor- caserina no sería la mejor opción debido a la posibilidad de un síndrome serotoninérgico. Sería mejor emplear fentermina o fentermina/topiramato. Orlistat es más seguro en todas las circunstancias debido a su mecanismo de acción junto con la dieta y la modificación del comportamiento. Para los pacien- tes con obesidad y diabetes tipo 2 que requieren insulina se sugiere agregar al menos uno de los dos siguientes: metformi- na, pramlintida o agonistas GLP-1, aunque también pueden funcionar inhibidores DPP-4 o la sitagliptina para mitigar la ganancia de peso debida a la insulina. La insulina preferida en estos casos es la insulina glargina o detemir. De acuerdo con las guías de las distintas asociaciones para el manejo del sobrepeso/obesidad, los mejores resultados se obtienen con
Tabla 1
Principales fármacos antiobesidad
Drogas Dosis Acción Efectos Estado Efectos adversos Contraindicaciones
FENTERMINA
(37.5 mg),
37.5 mg/d
Agonista NE
3% 1año Corto plazo Cefalea, HTA, taqui- cardia,
insomnio, boca seca, constipa- ción, ansiedad, temblores, diarrea,
impotencia. Psicosis, infarto, hipertensión arterial, glaucoma, convul- siones, uso IMAOS, embarazo, lactancia, hipertiroidismo, abuso
drogas.
DIETILPROPIÓN 75 mg/d Agonista NE 3% 1 año Corto
plazo Ídem fentermina. Ídem fentermina.
ORLISTAT
120 mg 3xd
Inhibidor lipasa pancreática y gástrica
5% 1 año
Uso crónico Disminución absor- ción vitaminas lipo- solubles (A,D,E,K), esteatorrea, Ciclosporina, mala absorción, embarazo, lactancia, colestasis, l-tiroxina, warfarina,
antiepilépticos.
LORCASERINA
10 mg 2xd
Agonista receptor 5HT2c
5% 1 año
Uso crónico Cefalea, náuseas, boca seca, mareos, constipación, Embarazo, lactancia, ISRS, ISRSN, IMAO,
bupropión, triptanos, dextrometorfano, hi-
dromorfona, codeína.
FENTERMINA/ TOPIRAMATO(F/T)
F=3.75 mg (15)+ T=23
Mg (92) 2xd
(T) Modula receptor GABA (F) agonista NA
6-10% 1 año
Uso crónico Insomnio, boca seca, constipación, parestesias, mareos,
disgeusia. Embarazo lactancia, hipertiroidismo, glau- coma, IMAO, aminas
simpaticomiméticas.
NALTREXONA/ BUPROPIÓN(N/B)
32/360 2xd
(B)Inhibe captación D/NE (N) antagoniza opioide
5% 1 año
Uso crónico
Náuseas, consti- pación, cefalea, vómitos, mareos. Hipertensión no con- trolada, convulsiones, anorexia nerviosa o bulimia, uso alcohol,
IMAO.
LIRAGLUTIDA
3.0 inyectable s.c.
Agonista GLP-1
5% 1 año
Uso crónico
Náuseas, vómitos, pancreatitis. Historia Cáncer medular tiroides, neoplasias endócrinas
múltiples.
BETAHISTINA
8-16 mg
Bloqueo H1, agonista H3
7% 6 meses
Corto plazo
Náuseas, cefaleas Feocromocitoma, embarazo, lactancia, úlcera, asma, porfiria.
ZONISAMIDA Bloqueo canal cálcico T 5% 6 meses Corto plazo
Tratamientos quirúrgicos para índice de masa corporal igual o mayor a cuarenta (40) kg/m2
Acceden al tratamiento quirúrgico pacientes con los siguientes criterios de inclusión: La información recabada en criterios de inclusión debe ser volcada en historia clínica que avale aptitud para la cirugía firmado y sellado por: cirujano de cirugía bariátrica, médico especializado en obesidad, médico nutricionista, psicólogo y/o psiquiatra
- Edad de 21 a 65.
- Índice de Masa Corporal (IMC) > 40 kg/m2.
- Más de 5 años de obesidad no reductible demostrada por evaluacio- nes en los últimos 5 años.
- Riesgo quirúrgico aceptable sin comorbilidades antes de la cirugía según escala ASA (American Society of Anesthesiologists Physical Status Scale).
- Fracaso de otros métodos no quirúrgicos para control de obesidad bajo supervisión médica al menos 1 vez por mes por 24 meses en forma ininterrumpida.
- Aceptación del procedimiento evaluado por equipo multidisciplinario y compromiso para sostener los cambios de estilo de vida asociados al by pass.
- No adicción a drogas ni alcohol evaluado por equipo multidisciplinario.
- Estabilidad psicológica.
- Comprensión clara del tratamiento y visión positiva del mismo.
- Consentimiento informado.
- Disposición para seguir las instrucciones del grupo multidisciplinario tratante.
- Buena relación médico-paciente. – En caso de comorbilidad endócrina o psiquiátrica, el especialista debe firmar junto al equipo antes citado el pedido de cirugía, confir- mando la estabilidad del paciente.
- Procedimientos quirúrgicos.
- Banda gástrica ajustable (BGA).
- By pass gástrico.
- Contraindicaciones para la cirugía.
- Adicción a drogas o alcoholismo.
- Pacientes embarazadas, en lactancia.
- Insuficiencias de órganos o sistemas incompatible con el riesgo anestesiológicos descrito con anterioridad.
- Depresión severa, patología psiquiátrica con comportamiento auto- destructivo.
- Obesidad secundaria a otra patología ejemplo síndrome de Cushing, acromegaglia, hipogonadismo, enfermedad hipotalámica.
- Riesgo quirúrgico elevado.
- No entender o no estar dispuesto a seguir correctamente el trata- miento.
- No aceptar firmar el consentimiento escrito de la cirugía.
visitas regulares hasta un total de 16 visitas por año en en- cuentros cara a cara. Si la medicación es eficaz determinado por una reducción de > 5 % del peso corporal a los 3 meses y no hay problemas de seguridad se recomienda continuar la medicación, pero si es ineficaz con <5% pérdida de peso en los 3 meses se recomienda cambiar el esquema. Tener presente que los medicamentos no son capaces de alterar por sí solos la fisiología subyacente a la obesidad de mane-
ra permanente, sino solo en la medida en que están siendo consumidos y no se pueden mantener los efectos solamente sobre la base de una modificación del comportamiento ya que no hay evidencia que apoye esta visión del mismo modo que ocurre con otros medicamentos como los anti-hipertensivos. Hay que tener en cuenta que la regulación corporal es un sistema complejo de sistemas de retroalimentación múltiples sobrepuestos.
Referencias bibliográficas
• 1. Patte KA, Davis CA, Levitan RD, Kaplan AS, Carter-Major J & Kennedy JL. A Behavioral Genetic Model of the Mechanisms Underlying the Link between Obesity and Symptoms of ADHD. J Atten Disord. 2016, 21. pii: 1087054715618793. [Epub ahead of print].
• 2. Rashid NA, Lim J, Lam M, Chong SA, Keefe RS & Lee J. Unraveling the relationship between obesity, schizophrenia and cognition. Schizophrenia research 2013, 151(1).
• 3. American Diabetes Association. (2004). Consensus development conference on antipsychotic drugs and obesity and diabetes. Diabetes care, 27(2), 596-601.
• 4. National Institutes of Health. National Heart, Lung, and Blood Institute. Clinical guidelines on the identification, evaluation, and treatment of overweight and obesity in adults. The evidence report. Bethesda: National Heart, Lung, and Blood Institute, 1998: p. i-228. Disponible en: http://www. nhlbi.nih.gov/nhlbi/nhlbi.htm.
• 5. The National Heart, Lung, and Blood Institute Expert Panel on the Identification, Evaluation, and Treatment of Overweight and Obesity in Adults. Executive summary of the clinical guidelines on the identification, evaluation, and treatment of overweight and obesity in adults. Arch Intern Med 1998; 158:1855-67.
• 6. Scottish Intercollegiate Guidelines Network. SIGN 50: a guideline developers’ handbook. Edinburgh: SIGN, 2001. Disponible en: www.sign.ac.uk/ guidelines/fulltext/50/index.html.
• 7. National Institutes of Health, National Heart, Lung, and Blood Institute, North American Association for the Study of Obesity. The Practical Guide: identification, evaluation, and treatment of overweight and obesity in adults. Bethesda: National Institutes of Health, National Heart, Lung, and Blood Institute, North American Association for the Study of Obesity, NIH Publication n.o 00-4048, 2000; p. 1-77. Disponible en: http://www. nhlbi.nih.gov/ guidelines/obesity/practgde.htm.
• 8. Serretti A, Mandelli L. Antidepressants and body weight: a comprehensive review and meta-analysis. J Clin Psychiatry. 2010;71: 1259–127.
• 9. Yanovski SZ & Yanovski JA. Naltrexone extended-release plus bupropion extended-release for treatment of obesity. JAMA 2015, 313(12), 1213-1214.
• 10. Himmerich H, Schuld A, Pollmächer T. Weight gain during treatment with antipsychotics: clinical relevance, pathophysiology, and therapeutical strategies. Psychiatr Prax. 2004; 31 Suppl 2:S233-7.
• 11. Nemani, K. L., Greene, M. C., Ulloa, M., Vincenzi, B., Copeland, P. M., Al-Khadari S & Henderson DC. Clozapine, Diabetes Mellitus, Cardiovascular Risk and Mortality: Results of a 21-year Naturalistic Study in Patients with Schizophrenia and Schizoaffective Disorder. Clinical schizophrenia & related psychoses 2017, doi:10.3371/CSRP.KNMG.111717. [Epub ahead of print] PubMed PMID: 29164928.
• 12. Samara MT, Dold M, Gianatsi M, Nikolakopoulou A, Helfer B, Salanti G & Leucht S. Efficacy, acceptability, and tolerability of antipsychotics in treatment-resistant schizophrenia: a network meta-analysis. JAMA psychiatry 2016, 73(3), 199-210.
• 13. Allison DB, Casey DE. Antipsychotic-induced weight gain: a review of the literature. J Clin Psychiatry. 2001; 62 (suppl 7):22–31.
• 14. Rummel-Kluge C, Komossa K, Schwarz S, Hunger H, Schmid F, Lobos CA & Leucht S. Head-to-head comparisons of metabolic side effects of second generation antipsychotics in the treatment of schizophrenia: a systematic review and meta-analysis. Schizophrenia research 2010, 123(2), 225-233.
• 15. Fraguas D, Correll CU, Merchán-Naranjo J, Rapado-Castro M, Parellada M, Moreno C & Arango C. Efficacy and safety of second-generation antipsy- chotics in children and adolescents with psychotic and bipolar spectrum disorders: comprehensive review of prospective head-to-head and placebo-con- trolled comparisons. European Neuropsychopharmacology 2011, 21(8), 621-645.
• 16. Verrotti A, D’Egidio C, Mohn A, Coppola G, Chiarelli F. Weight gain following treatment with valproic acid: pathogenetic mechanisms and clinical implications. Obes Rev. 2011; 12: e32–e43.
• 17. Gaspari CN, Guerreiro CA. Modification in body weight associated with antiepileptic drugs. Arq Neuropsiquiatr. 2010; 68:277–281.
• 18. DeToledo JC, Toledo C, DeCerce J, Ramsay RE. Changes in body weight with chronic, high-dose gabapentin therapy. Ther Drug Monit. 1997; 19:394–396.
• 19. Ben-Menachem E. Weight issues for people with epilepsy–a review. Epilepsia. 2007; 48 (suppl 9):42– 45.
• 20. Rakitin A, Kõks S & Haldre S. Metabolic syndrome and anticonvulsants: A comparative study of valproic acid and carbamazepine. Seizure 2016, 38, 11-16.
• 21. Gadde KM, Kopping MF, Wagner HR, Yonish GM, Allison DB & Bray GA. Zonisamide for Weight Reduction in Obese Adults A 1-Year Randomized Controlled Trial. Archives of Internal Medicine 2012, 172(20), 1557–1564.
• 22. Apovian CM & Aronne LJ. Zonisamide for weight reduction in obese adults. JAMA 2013, 310(6), 637-638.
• 23. Gadde KM, Allison DB, Ryan DH, Peterson CA, Troupin B, Schwiers ML & Day WW. Effects of low-dose, controlled-release, phentermine plus topiramate combination on weight and associated comorbidities in overweight and obese adults (CONQUER): a randomised, placebo-controlled, phase 3 trial. Lancet 2011, 377, 1341-52.
• 24. McDonagh MS, Selph S, Ozpinar A & Foley C. Systematic review of the benefits and risks of metformin in treating obesity in children aged 18 years and younger. JAMA pediatrics 2014, 168(2), 178-184.
• 25. Hegedüs L, Moses AC, Zdravkovic M, Le Thi T & Daniels GH. GLP-1 and calcitonin concentration in humans: lack of evidence of calcitonin release from sequential screening in over 5000 subjects with type 2 diabetes or nondiabetic obese subjects treated with the human GLP-1 analog, liraglutide. The Journal of Clinical Endocrinology & Metabolism 2011, 96(3), 853-860.
• 26. Gadde KM, Parker CB, Maner LG, Wagner HR, Logue EJ, Drezner MK & Krishnan KR. Bupropion for weight loss: an investigation of efficacy and
tolerability in overweight and obese women. Obesity Research 2001, 9(9), 544-551.
• 27. Volkow ND, Wang GJ, Fowler JS, Logan J, Jayne M, Franceschi D & Pappas N. “Nonhedonic” food motivation in humans involves dopamine in the dorsal striatum and methylphenidate amplifies this effect. Synapse 2002, 44(3), 175-180.
• 28. Krude H, Biebermann H, Schnabel D, Tansek MZ, Theunissen P, Mullis PE & Grüters A. Obesity due to proopiomelanocortin deficiency: three new cases and treatment trials with thyroid hormone and ACTH4–10. The Journal of Clinical Endocrinology & Metabolism 2003, 88(10), 4633-4640.
• 29. Barak N. Betahistine: what’s new on the agenda? Expert opinion on investigational drugs 2008, 17(5), 795-804.
• 30. Halford JC, Boyland EJ, Blundell JE, Kirkham TC & Harrold JA. Pharmacological management of appetite expression in obesity. Nature Reviews Endocrinology 2010, 6(5), 255.
• 31. Aotani D, Son C, Shimizu Y, Nomura H, Hikida T, Kusakabe T & Nakao K. Reevaluation of anti-obesity action of mazindol and elucidation of its effect on the reward system. Neuroscience Letters 2016, 633, 141-145.
• 32. Kernan WN, Viscoli CM, Brass LM, et al. Phenylpropanolamine and the risk of hemorrhagic stroke. N Engl J Med 2000; 343: 1826-32.
• 33. Shin JH & Gadde KM. Clinical utility of phentermine/topiramate (Qsymia) combination for the treatment of obesity. Diabetes Metab Syndr Obes 2013, 6, 131-139.
• 34. Hendricks EJ, Srisurapanont M, Schmidt SL, et al. Addiction potential of phentermine prescribed during long-term treatment of obesity. Int J Obes (Lond). 2014; 38:292–298.
• 35. Hampp C, Kang EM, Borders-Hemphill V. Use of prescription antiobesity drugs in the United States. Pharmacotherapy 2013; 33: 1299-1307.
• 36. Cercato C, Roizenblatt VA, Leança CC, et al. A randomized double-blind placebo controlled study of the long-term efficacy and safety of diethyl- propion in the treatment of obese subjects. Int J Obes (London) 2009; 33: 857-65.
• 37. Haddock CK, Poston WS, Dill PL, Foreyt JP, Ericsson M. Pharmacotherapy for obesity: a quantitative analysis of four decades of published rando- mized clinical trials. Int J Obes Relat Metab Disord 2002; 26: 262-73.
• 38. Cosentino, G., Conrad, A. O., & Uwaifo, G. I. (2013). Phentermine and topiramate for the management of obesity: a review. Drug design, develo- pment and therapy, 7, 267.
• 39. Haddock CK, Poston WS, Dill PL, Foreyt JP, Ericsson M. Pharmacotherapy for obesity: a quantitative analysis of four decades of published rando- mized clinical trials. Int J Obes Relat Metab Disord 2002; 26: 262-73.
• 40. Schulz, L.O.; Bennett, P.H.; Ravussin, E.; Kidd, J.R.; Kidd, K.K.; Esparza, J.; Valencia, M.E. Effects of traditional and western environments on prevalence of type 2 diabetes in Pima Indians in Mexico and the U.S. Diabetes Care, 2006, 29, 1866-71.
• 41. Fidler MC, Sanchez M, Raether B, et al. A one-year randomized trial of lorcaserin for weight loss in obese and overweight adults: the BLOSSOM trial. J Clin Endocrinol Metab. 2011; 96:3067–3077.
• 42. Smith SR, Weissman NJ, Anderson CM, et al. Multicenter, placebo- controlled trial of lorcaserin for weight management. N Engl J Med. 2010; 363:245–256.
• 43. O’Neil PM, Smith SR, Weissman NJ, et al. Randomized placebocontrolled clinical trial of lorcaserin for weight loss in type 2 diabetes mellitus: the BLOOM-DM study. Obesity 2012; 20:1426–1436.
• 44. Serrani D. Efecto de betahistina sobre aumento de peso inducido por quetiapina. Revista psicofarmacología 2016 98:11.
• 45. Fanghänel G, Cortinas L, Sánchez-Reyes L, Berber A. Second phase of a double-blind study clinical trial on Sibutramine for the treatment of pa- tients suffering essential obesity: 6 months after treatment cross-over. Int J Obes Relat Metab Disord. 2001; 25;741–747.
• 46. Anderson JW, Schwartz SM, Hauptman J, et al. Low-dose orlistat effects on body weight of mildly to moderately overweight individuals: a 16 week, double-blind, placebo-controlled trial. Ann Pharmacother. 2006; 40:1717–1723.
• 47. Xenical (orlistat) [prescribing information]. South San Francisco, CA: Genentech USA Inc. http://www.gene.com/download/pdf/xenical_prescribing. pdf. Consultado Mayo 2, 2016.
• 48. Alli (orlistat) [label]. Moon Township, PA: GlaxoSmithKline. http://www.accessdata.fda.gov/drugsatfda_docs/label/2007/021887lbl.pdf. Consulta- do Mayo 2, 2016.
• 49. Malin SK, Kashyap SR. Effects of metformin on weight loss: potential mechanisms. Curr Opin Endocrinol Diabetes Obes. 2014; 21(5):323–329.
• 50. Caton PW, Kieswich J, Yaqoob MM, Holness MJ, Sugden MC. Metformin opposes impaired AMPK and SIRT1 function and deleterious changes in core clock protein expression in white adipose tissue of genetically-obese db/db mice. Diabetes Obes Metab 2011; 13 (12):1097–1104.
• 51. Hollander P, Raslova K, Skjøth TV, Råstam J, Liutkus JF. Efficacy and safety of insulin detemir once daily in combination with sitagliptina and metformin: the TRANSITION randomized controlled trial. Diabetes Obes Metab. 2011; 13:268–275.
• 52. McIntosh B, Cameron C, Singh SR, et al. Second-line therapy in patients with type 2 diabetes inadequately controlled with metformin monotherapy: a systematic review and mixed-treatment comparison meta-analysis. Open Med. 2011; 5:e35–e48.
• 53. Wu D, Li L, Liu C. Efficacy and safety of dipeptidyl peptidase-4 inhibitors and metformin as initial combination therapy and as monotherapy in patients with type 2 diabetes mellitus: a meta-analysis. Diabetes Obes Metab. 2014; 16(1):30–37.
• 54. Wainstein J, Katz L, Engel SS, et al. Initial therapy with the fixeddose combination of sitagliptin and metformin results in greater improvement in glycaemic control compared with pioglitazone monotherapy in patients with type 2 diabetes. Diabetes Obes Metab. 2012; 14(5):409–418.
• 55. Bolinder J, Ljunggren Ö, Kullberg J, et al. Effects of dapagliflozina on body weight, total fat mass, and regional adipose tissue distribution in pa- tients with type 2 diabetes mellitus with inadequate glycemic control on metformin. J Clin Endocrinol Metab. 2012; 97:1020–1031.
• 56. Buse JB, Bergenstal RM, Glass LC, et al. Use of twice-daily exenatida in basal insulin-treated patients with type 2 diabetes: a randomized, contro- lled trial. Ann Intern Med. 2011; 154:103–112.
• 57. Aronne L, Fujioka K, Aroda V, Chen K, Halseth A, Kesty NC & Weyer C. Progressive reduction in body weight after treatment with the amylin analog pramlintide in obese subjects: a phase 2, randomized, placebo-controlled, dose-escalation study. The Journal of Clinical Endocrinology & Metabolism 2007, 92(8), 2977-2983.
• 58. van de Laar FA, Lucassen PL, Akkermans RP. Alpha-glucosidase inhibitors for patients with type 2 diabetes: results from a Cochrane systematic review and meta-analysis. Diabetes Care. 2005; 28 (1):154–163.
• 59. Lee A, Patrick P, Wishart J, Horowitz M, Morley JE. The effects of miglitol on glucagon-like peptide-1 secretion and appetite sensations in obese type 2 diabetics. Diabetes Obes Metab. 202; 4(5): 329–335.
• 60. Wu D, Li L, Liu C. Efficacy and safety of dipeptidyl peptidase-4 inhibitors and metformin as initial combination therapy and as monotherapy in patients with type 2 diabetes mellitus: a meta-analysis. Diabetes Obes Metab. 2014; 16 (1): 30–37.
• 61. Wainstein J, Katz L, Engel SS, et al. Initial therapy with the fixed dose combination of sitagliptin and metformin results in greater improvement in glycaemic control compared with pioglitazone monotherapy in patients with type 2 diabetes. Diabetes Obes Metab. 2012; 14(5):409–418.
• 62. Richter B, Bandeira-Echtler E, Bergerhoff K, Lerch CL. Dipeptidyl peptidase-4 (DPP-4) inhibitors for type 2 diabetes mellitus. Cochrane Database Syst Rev. 2008; 2:CD006739.
• 63. Scheen AJ. DPP-4 inhibitors in the management of type 2 diabetes: a critical review of head-to-head trials. Diabetes Metab. 2012; 38: 89–101.
• 64. Bolinder J, Ljunggren Ö, Kullberg J, et al. Effects of dapagliflozina on body weight, total fat mass, and regional adipose tissue distribution in pa- tients with type 2 diabetes mellitus with inadequate glycemic control on metformin. J Clin Endocrinol Metab 2012; 97: 1020–1031.
• 65. Grandy S, Hashemi M, Langkilde AM, Parikh S, Sjöström CD. Changes in weight loss-related quality of life among type 2 diabetes mellitus patients treated with dapagliflozin. Diabetes Obes Metab 2014; 16: 645–650.






