Conducta maternal y apego: consideraciones clínicas y epigenéticas Mecanismos epigenéticos de los fármacos
Resumen
La interrupción temprana del vínculo de apego madre hijo –attachment– produce efectos negativos en la neuroplasticidad y puede predisponer a manifestaciones psicopatológicas futuras. El apego contribuye a la supervivencia física y psíquica del sujeto generando seguridad y facilitando el conocimiento del mundo.
Gracias a diferentes investigaciones, se sabe que las conductas de aseo y cuidado de las crías (licking-grooming, LG) alteran la función del eje hipotalámico-pituitario-adrenal, y regulan la expresión del gen del receptor de glucocorticoides (GR) en el hipocampo a través de la acetilación de las histonas y la metilación del ADN (Moriceau et al., 2009).
La epigenética –cambios heredables en la estructura y organización del ADN y de las histonas, que no implican alteraciones en la secuencia de nucleótidos– genera modificaciones que afectan la actividad transcripcional de los genes que son relativa- mente estables en las generaciones futuras.
Algunos psicofármacos pueden producir modificaciones epigenéticas; entre otros, los antidepresivos tendrían la capacidad de restablecer la funcionalidad del circuito involucrado en la depresión.
Vemos entonces que se abren nuevas perspectivas y posibles abordajes en los conceptos de salud y enfermedad, que abarcan la compleja red de interacción de nuestro bagaje genético con el medio ambiente.
Palabras clave
Apego – Conducta Maternal – Epigenética – Neuroplasticidad – Salud Mental.
Dahan Miriam P. “Conducta maternal y apego: consideraciones clínicas y epigenéticas. Mecanismos epigenéticos de los fármacos”. Psicofarmacología 2018;111:12-30. Puede consultar otros artículos publicados por los autores en la revista Psicofarmacología en sciens.com.ar
Introducción
Allí donde el arte de la medicina es cultivado, también se ama a la humanidad. Hipócrates, Siglo V a. C.
sistematizarla para una detección temprana de gran impacto preventivo. La unidad de evaluación diagnóstica y terapéutica es la díada madre-bebé; consideración basada en el supuesto de la interdependencia del funcionamiento psíquico de ambos.
Un bebé requiere un adecuado ambiente que estimule su desarrollo y maduración. Los factores del medio en fases tem- pranas del desarrollo infantil están centrados, constituidos, en su mayor parte por los cuidados maternos. En un sentido amplio se sabe que los cuidados que brindan los padres a los hijos desde el mismo momento de la gestación tienen un sig- nificado muy especial en el futuro de su salud mental.
La psicopatología del bebé constituye un objeto de obser- vación y reflexión definida entre el nacimiento y el tercer año de vida. Esta distinción se justifica dada la originalidad de la semiología y clínica psiquiátrica del bebé y la posibilidad de
Los estudios neurobiológicos avalan la idea que el desarrollo madurativo en el hombre sienta sus bases en los primeros dos meses de la gestación; en relación al sistema nervioso central, la morfología global de los hemisferios cerebrales ya está constituida en ese tiempo gestacional. El “empuje” de crecimiento del cerebro humano, comienza a partir del último trimestre del embarazo y continúa hasta los dieciocho/veinticuatro (18-24) meses de vida posnatal; por su parte, la mielinización del cerebro es tan rápida y amplia que al final del primer año de vida ya tiene un aspecto similar al del adulto.
Las investigaciones en neurociencias indican que el crecimiento acelerado de la estructura cerebral en el período posnatal parece depender de una adecuada interacción con el medio ambiente. La maduración posnatal de los circuitos límbicos del sistema autónomo es influida significativamente por las características de las experiencias sociales y afectivas que le proporciona el cuidador principal del niño.
Varias investigaciones comprobaron que la interrupción temprana de la relación de apego madre-hijo tiene un efecto negativo en la plasticidad del cerebro y predispone a patologías psicológicas futuras. Investigaciones sobre las capacidades sensoriales e interactivas del recién nacido revolucionaron las primeras concepciones sobre el tema y se pasó a considerar al bebé como un ser complejo que interactúa desde el principio con los adultos que lo rodean.
Los conceptos de vínculo y apego neonatal nos permiten profundizar lo señalado, remarcando la importancia conferida hace muchos años por John Bowlby y Mary D. S. Ainsworth, entre otros autores, al período comprendido entre el nacimiento y los primeros años de vida (Oiberman, 2011). Bowlby basó sus trabajos en la observación de los conocimientos entonces existentes sobre Biología, particularmente en dos: la teoría de la evolución de Charles Darwin (1809-1882) y el aprendizaje programado o impronta (imprinting) de Konrad Lorenz (1903- 1989), Premio Nobel de Fisiología-Medicina en 1973.
En las bases neurobiológicas de las conductas de vinculación de madres y bebés una línea de investigación se basa en la epigenética, más específicamente en los genes tempranos de adaptación a estímulos medioambientales, que implican cambios heredables en el ADN e histonas sin alteraciones en la secuencia de nucleótidos, sino sobre la estructura de la cromatina, que modifican su estructura y condensación, afectando así la expresión génica y el fenotipo (Morgan, Whitelaw, 2003). Las conductas de vinculación de madres y bebés están radicadas en el programa genético, es decir en los genes tempranos de adaptación a estímulos medioambientales que proveen la base molecular de las conductas de adaptación. Estudios de investigación en modelos animales postulan que una alta conducta maternante, esto es, el cuidado materno neonatal temprano medido en conductas de aseo y cuidado de las crías (licking-grooming o LG), estimula la acetilación de histonas en el promotor del gen del receptor a glucocorticoides (GR), aumentando su transcripción y facilitando el frenado del eje hipotálamo pituitario adrenal (HPA), lo que genera crías que poseen una menor respuesta al estrés cuando son adultas.
A su vez, el fenotipo biológico se revierte cuando se entrecruzan las crías de madres con baja conducta de LG a alta conducta de LG: al revertirse los niveles del receptor GR, se eliminan las influencias de las experiencias ambientales tempranas sobre las respuestas del eje HPA al estrés (Weaver and Meaney, 2006).
Así como el entorno puede producir marcas epigenéticas, algunos fármacos ejercen cambios epigenéticos que serán señalados en este trabajo. Los mecanismos de acción a nivel molecular, que los antidepresivos producen en mayor preponderancia a nivel presináptico, llevan a la activación sostenida de los receptores postsinápticos, que desencadenan “accio- nes” neuroplásticas a mediano y largo plazo (Alvano, 2010). La conducta materna entonces –o de quien o quienes ejerzan esta función– tendría un claro impacto en la salud del individuo, en la de su descendencia y en la evolución de la especie humana.
Hipótesis
- La conducta maternante en las primeras etapas del desa- rrollo puede ejercer cambios neurobiológicos y generar conse- cuencias en la salud mental.
Objetivos generales
- Describir las posibles implicancias clínicas y epigenéticas, de acuerdo con las características de la conducta maternante.
Objetivos específicos
- Desarrollar los conceptos centrales de la Teoría del apego neonatal.
- Considerar las variables neurobiológicas en las conductas de apego.
- Analizar las características de la conducta maternante.
- Exponer las implicancias clínicas y epigenéticas.
- Mecanismos epigenéticos de los fármacos.
Materiales y métodos
- Recopilación de material bibliográfico proveniente de in- formación científica actualizada.
- Datos clínicos elaborados en la práctica profesional.
- Investigación de característica descriptiva.
Desarrollo
Los cuidados proporcionados por los padres o cuidadores a sus hijos, desde el mismo momento de la gestación, tienen un significado muy importante en el futuro de su salud mental. Un bebé requiere un adecuado ambiente que estimule su de- sarrollo y maduración.
Los factores del medio en fases tempranas del desarrollo infantil están centrados, constituidos en su mayor parte por los cuidados maternos.
El padre representa un papel esencial, ya que protege la díada madre-bebé, consolida la posibilidad para el niño de vivir en un entorno “nutriente” y separa a la madre y al bebé cuando llegue el momento justo para que el mundo del bebé pueda extenderse más allá de los límites de la díada.
La psicopatología del bebé, como ya fue señalado, constituye un objeto de observación y reflexión definida, que puede sistematizarse en una semiología precisa, para una detección temprana de carácter preventivo. La unidad de observación diagnóstica y terapéutica es la díada madre-bebé en su interacción diádica; por lo tanto el rol y el significado del síntoma y el carácter transdisciplinario de intervención posible, se plantea como eje ya que las variables psicopatológicas y neurobiológicas ocupan un área común.
Diversos autores han profundizado estos aspectos.
La definición de apego acorde con la Real Academia Espa- ñola es: “Afición o inclinación hacia alguien o algo”.
Para el diccionario libre (The Free Dictionary) es: “El de- sarrollo de fuertes lazos afectivos entre un bebé y su madre, padre, hermano, cuidador”.
La teoría psicológica del apego, formulada originalmente por John Bowlby en la segunda década del Siglo XX (1950), ha permitido profundizar el conocimiento del vínculo ma- dre-bebé, identificar sus patologías y evaluar su influencia en las relaciones afectivas adultas. Desde esta perspectiva, el apego contribuye a la supervivencia física y psíquica del sujeto generando seguridad y facilitando el conocimiento del mundo, en la medida en que el niño va conformando modelos de representación internos que estructuran su vínculo con el mundo y con los otros significativos (Bowlby, 1979).
A partir de estos conceptos teóricos se desarrollaron instru- mentos y técnicas para evaluar las formas del apego y sus ca- racterísticas saludables y patológicas. Se señala como ejem- plo representativo de este importante desarrollo, la técnica de la situación extraña de Ainsworth (Strange Situation) para evaluar el apego del niño y su cuidador. Se trata de un proce- dimiento de laboratorio semiestructurado en el que se podía observar a los bebés respondiendo frente a distintos estímulos (Ainsworth, 1969).
Los niños son confrontados con tres componentes estresantes:
- un medioambiente que no es familiar
- la interacción con un extraño
- dos breves separaciones de la madre/cuidadora.
El comportamiento de apego se activa o desactiva de acuer- do con ciertas condiciones. La presencia de la madre puede brindar seguridad y facilitar la separación y la exploración del medio ambiente.
En sus observaciones, Ainsworth identificó tres tipos de apego:
- Seguro: los niños buscan interactuar con su cuidador y este responde conforme a sus requerimientos.
- Inseguro evitativo: el niño no busca interactuar con su cuidador, no protesta ante las separaciones y parece no estar angustiado; trata de desenvolverse sin el amor y/o apoyo de otras personas.
- Inseguro ambivalente: el niño interactúa poco con su cui- dador, mantiene una combinación de conductas de contacto y rechazo. Temeroso ante la exploración del mundo exterior, propenso al aferramiento (Ainsworth, 1969).
¿De dónde surge el concepto de apego? Surge a partir del estudio de la conducta maternal de aves y primates en el marco de la etología. En este sentido, Bowlby subrayó la importancia de no perder de vista la función biológica adaptativa de las conductas de apego, así como la importancia de los factores genéticos que influyen en las conductas de la especie y del individuo (Bowlby, 1979).
Dado que muchas de las metodologías empleadas en esta línea revisten un carácter invasivo, existe gran cantidad de investigación psicobiológica realizada en animales. Si bien una simple extrapolación de datos de un campo a otro no es pertinente, existen fuertes fundamentos evolutivos para afirmar que los datos provenientes de la investigación animal aportan indicios interesantes para comprender el comportamiento humano. El propio Charles Darwin estableció este patrón de comparación en su obra, tanto en el campo de la fisiología como en el de la expresión emocional.
Darwin (1809-1882) publicó en 1859 la obra El Origen de las especies, donde expuso sus conclusiones sobre la transformación de las especies. El naturalista A.R. Wallace (1823- 1913), contemporáneo, había llegado a la misma hipótesis. Darwin realizó sus observaciones en una expedición científica de varios años de duración (1831-1836), que le sirvieron de fundamento para desarrollar su teoría.
A partir de la segunda mitad del siglo XVIII, la observación de que los individuos de una misma especie no eran todos parecidos entre sí, y que los descendientes no siempre eran iguales a sus progenitores, había llevado a pensar a algunos naturalistas como Bufon, Maupertuis y Erasmus Darwin (abuelo de Charles Darwin) que las especies actuales podrían haber surgido por transformación de las especies anteriores mediante la suma progresiva de diferencias. Al observar que las nuevas especies procedentes de América se parecían más a algunas del “Viejo Mundo” que a otras, pensaron que debía existir un parentesco, es decir, que las especies más semejantes procedían de un antepasado común.
El naturalista francés Jean-Baptiste Lamarck (1744-1829) publicó en 1809 la obra Filosofía Zoológica (la primera exposición de su teoría se denominó Indagaciones sobre los cuerpos vivientes), en la que expuso su hipótesis sobre la transformación gradual de las especies a lo largo del tiempo, conocida actualmente como lamarckismo, que constituyó la primera teoría de la evolución.
Los creacionistas sostenían que Dios creaba directamente las especies, mientras que Lamarck defendía que Dios crea la naturaleza y esta da lugar a las especies, debido a su tenden- cia natural hacia la complejidad y a las adaptaciones causa- das por las variaciones ambientales.
La explicación de la causa del largo cuello de la jirafa es un ejemplo clásico de la teoría de Lamarck. Según esta hipótesis, los esfuerzos realizados durante su vida por el antecesor de la jirafa para alcanzar las hojas de las ramas altas de los árboles provocaron que la longitud de su cuello aumentase. Sus descendientes heredaron este carácter y, a su vez, lo desarrollaron. Este proceso de evolución, al cabo de muchas generaciones, originó el cuello de la actual jirafa (Lamarck, 1971).
El lamarckismo, que ha sido superado por las teorías de la evolución posteriores, no pudo demostrar experimentalmente en aquel momento la tendencia natural de las especies a aumentar su grado de complejidad, ni tampoco cómo se transmiten los caracteres adquiridos a los descendientes.
Retomando a Darwin y su teoría de la evolución natural, en su tratado El origen de las especies plantea el mecanismo de selección natural como aquel fenómeno donde, en condiciones ambientales adversas para los organismos, se establece entre ellos una lucha por la supervivencia, en la que solo sobreviven los individuos más adaptados y se eliminan los demás. De esta manera se produce la selección natural de los más aptos. Únicamente los individuos que sobreviven son los que pueden reproducirse y así transmitir sus caracteres a los descendientes. La selección natural, con el transcurso del tiempo, va transformando paulatinamente a las especies (Darwin, 1979).
En lenguaje simple y coloquial explicaba que las especies cambiaban como resultado de una necesidad nueva; que la lucha por la supervivencia eliminaba las variaciones desfavorables y sobrevivían las más aptas; que el número de individuos de cada especie permanecía más o menos constante; y por medio de descripciones minuciosas, cómo variaban en todos los aspectos las distintas especies según el entorno.
Un ejemplo clásico lo constituyen las trece especies de pinzones de Darwin (género de aves) de las islas Galápagos. Principalmente, la diferencia de estas especies es el tamaño y la forma del pico que depende de su fuente de alimentación. Explica su aparición a partir de una primera especie de pinzón que llegó procedente de las costas de Ecuador, y cuyos descendientes se adaptaron a los diferentes tipos de alimentos y de ambientes que había en cada isla.
La teoría de Darwin sufrió diversas críticas: no explicaba cómo se originaba la variabilidad de la descendencia. Las causas de la variabilidad están relacionadas con las mutaciones y la recombinación genética, pero para llegar a este conocimiento sería necesario que se desarrollase la genética. Darwin no llegó a conocer los trabajos de Gregor Mendel (1822-1884), debido a su escasa difusión, en consecuencia no supo nunca el origen de la variabilidad de la descendencia y, por lo tanto no pudo responder a las críticas que le acusaban de no explicar el origen de dicha variabilidad.
Las leyes de Mendel, conjunto de reglas básicas sobre la transmisión por herencia genética de las características de los organismos padres a sus hijos, constituyen el fundamento de la genética. Las leyes se derivan del trabajo realizado por Mendel, publicado en 1865 y en 1866, aunque fue ignorado por mucho tiempo hasta su redescubrimiento en 1900 (Marantz Henig, 2001).
Finalmente el neodarwinismo (Teoría sintética de la evolución) planteó los puntos claves de la Teoría de la evolución en un congreso en Princeton:
- la variabilidad en la descendencia se debe a las mutaciones que originan nuevos genes y a la recombinación genética.
- la selección natural elimina a los individuos menos aptos y permite reproducirse a los más adaptados.
-la variación de la frecuencia génica, son las poblaciones las que evolucionan al variar sus frecuencias génicas. Los factores que producen la variación génica son: las mutaciones, la deriva genética, la selección natural y las migraciones.
-el aislamiento geográfico: una población debe mantenerse alejada de la otra para que dé lugar a una nueva especie (Sa- las e Iturbe, 2011).
Konrad Lorenz (1903-1989), zoólogo y etólogo austríaco, graduado en Medicina en 1928 y en Zoología en 1933, compartió el Premio Nobel de Medicina en 1973, con K. Von Frish y N. Tinbergen, por describir la impronta, es decir, el proceso fisiológico generado tras el nacimiento que garantiza el comportamiento maternal y filial entre madre y cría; estos hallazgos se integraron posteriormente en la teoría del apego humano (Lorenz, 1973; Bateson, 1990). Lorenz propuso la hipótesis de que muchas tendencias animales y humanas se basan en pautas genéticas latentes y son desencadenadas por sucesos del medio ambiente. Sugería que esos patrones eran tan importantes para la su- pervivencia del animal como sus características fisiológicas, y que ambos factores tenían un desarrollo evolutivo similar. Quizá sea más conocido porque descubrió que los estímulos aurales-auditivos y visuales de los progenitores de un animal son necesarios para inducirlo a seguirles, pero que cualquier objeto, incluido un ser humano, podía inducir la misma respuesta empleando los mismos estímulos. Llamó a este fenómeno impronta. Sus observaciones le permitieron fundamentar que las crías de los gansos comenzaban a seguir a su madre poco después de romper el cascarón, creando así un vínculo importante que ayudaba a la madre a protegerlos y a entrenarlos. Entre 1940 y 1950, Lorenz describió cómo los patitos que nacieron en su jardín de Altenberg lo tomaron como “madre pata”, y lo seguían a todas partes.
Esta “programación genética” desenlaza una serie de comportamientos que favorecen la protección de las crías al am- paro de sus progenitores. Los gansos recién nacidos detectaban un ser grande en el momento de romper sus cáscaras y se producía ese apego. Era un patrón más o menos permanente. Incluso algunos gansos silvestres, debido a esto, preferían pasar la noche cerca del cuarto del Lorenz y lo seguían a todas partes (Grandin y Deesing, 1998).
Por lo tanto, impronta es un concepto que se puede definir como patrones de acción fijos, que están genéticamente de- terminados y que se manifiestan a través de la influencia del ambiente particular a una especie animal. Es una forma de aprendizaje en la que un animal muy joven fija su atención en el primer objeto que ve, escucha o toca y el movimiento que hace a continuación tras ese objeto; en la naturaleza, ese objeto normalmente es uno de los padres.
Esta programación genética desencadena una serie de comportamientos que favorecen la protección de la cría al amparo de sus progenitores. Experimentalmente, otros animales y objetos inanimados han sido utilizados para estudiar este comportamiento. El estudio comparado del comportamiento de los animales ayuda a comprender la manera en que se establece el vínculo entre la madre y la cría, brindando los argumentos posibles, al hacer extensivos sus resultados a la especie humana (Ainsworth, 1969).
Como dato de interés específico los etólogos buscaron entender los mecanismos de patrones innatos de comportamiento, y las motivaciones por las cuales los animales se comportan de la forma en que lo hacen. Lorenz (1939, 1965, 1981) y N. Tinbergen (1948, 1951) desarrollaron el etograma, que es una lista completa de todas las conductas que un animal despliega en su entorno. El etograma incluye los comportamientos innatos tanto como los adquiridos, con “patrones fijos de acción” que son activados por lo que denominaron “estímulo-señal”. Lorenz y Tinbergen denominaron “estímulo señal” al objeto que desencadena la activación de un patrón fijo de acción. En un ejemplo: cuando un ave madre ve la boca abierta de sus crías, esto desencadena el comportamiento maternal de alimentarlas, por lo tanto la boca abierta es un estímulo señal que actúa como un interruptor que enciende un programa determinado genéticamente.
El Premio Nobel de Fisiología y Medicina en 1973, compartido por Lorenz con Nikolaas Tinbergen y Karl R. Von Frisch, los tres zoólogos que trabajaban en el estudio del comportamiento animal, causó cierta sorpresa en el mundo científico. Sin embargo, los argumentos que brindaron los integrantes del tribunal sueco de los premios Nobel se basaron en que sus trabajos con- tribuían a comprender mejor diversos aspectos de la Psiquiatría. Estableciendo enlaces, el psicoanalista inglés John Bowlby estudió el modo en que se desarrolla la conducta de apego en el bebé humano, y concluyó que esta puede incluirse dentro de las pautas generales de impronta (siempre que este término se aplique en un sentido genérico amplio). La Teoría de la impronta ya mencionada –forma de aprendizaje en que los ani- males precociales aprenden en los primeros días a aproximarse al primer objeto grande en movimiento– establece así una base de comparación natural en relación a las conductas humanas de apego. Refiere que los seres humanos nacen con la tendencia innata de apegarse a una persona protectora que los cuida. Bowlby introdujo la palabra attachment, que se traduce como apego. El apego, vínculo afectivo que el niño gesta con sus cuidadores y que le proporciona la seguridad emocional indispensable para un desarrollo saludable, forja los cimientos necesarios para el posterior desarrollo del niño y contribuye al bienestar psicológico o a la psicopatología.
La tesis fundamental de la teoría del apego es que el estado de seguridad, ansiedad o temor de un niño está determinado, en gran medida, por la capacidad de respuesta de la madre y/o cuidador (Bowlby, 1969). La falta de cuidados maternos pueden llevar a un desajuste en la integración social, a dificultades en las relaciones interpersonales y diferentes manifestaciones psicopatológicas.
Bowbly también puntualizó que es el tipo de cuidados, disfuncionales o pobres, más que la ausencia de la madre en sí misma, lo que causa las dificultades (deprivación materna).
El vínculo de apego tiene varios elementos claves:
- es una forma especial y perdurable de relación emocional con otra persona
- proporciona consuelo, agrado, sosiego y placer
- la pérdida, o amenaza de pérdida de esa persona evoca angustia.
La Organización Mundial de la Salud (OMS) publicó en 1951 un informe elaborado por Bowlby –Cuidado materno y Salud mental– a partir de una serie de entrevistas con los mejores especialistas en desarrollo infantil (Bowlby, 1954).
En el tema particular del vínculo madre-hijo se destacan los aportes de René Spitz (1887-1974), médico y psicoanalista. Fue quien acuñó el término hospitalismo, que utilizó para de- signar el conjunto de perturbaciones somáticas y psíquicas provocadas por la prolongada permanencia de los niños pequeños en una institución hospitalaria privados de la presencia y cuidados de su madre.
Spitz desarrolló sus investigaciones motivado en los trabajos de Anna Freud (1895-1982) y Maria Montessori (1870- 1952). A partir de 1935 se dedicó a la observación y el estudio del desarrollo infantil focalizándose en la importancia de los cuidados maternos y los efectos de la deprivación emocional. Desde una perspectiva integradora del psicoanálisis en la psicología genética, se interesó por las primeras relaciones de objeto, los estadios, las carencias afectivas y los trastornos del lenguaje vinculados con la internación de niños pequeños en las instituciones hospitalarias.
En el texto “El primer año de vida del niño”, Spitz describió la depresión anaclítica. Planteaba que “la ausencia de relaciones objetales causadas por la carencia afectiva detiene el desarrollo en todos los sectores de la personalidad…” […] “Puede presentar pérdida de la expresión mímica, anorexia, mutismo, insomnio, retardo psicomotor. Además, el lactante vuelve la regresión hacia sí mismo, son niños que pueden atacarse activamente a sí mismos, dándose cabezazos contra sus cunas, pegándose con el puño y arrancándose mechones de pelo. Este deterioro puede progresar hasta llevarlo al marasmo y a la muerte” (Spitz, 1979).
La depresión anaclítica es reversible: si la ausencia de la madre no es muy prolongada, al restablecerse el vínculo, la depresión cesa muy rápidamente (privación afectiva parcial). Si esta privación sobrepasa las dieciocho semanas, el niño probablemente llegue al estado de hospitalismo. En este es- tado, la separación madre-hijo, durante un tiempo muy largo o total, desemboca en la imposibilidad del niño para entablar contactos afectivos permanentes; por ejemplo, porque está en una institución de salud que da tratamiento impersonal. El hospitalismo puede dar lugar a estados irreversibles, incluyen- do la muerte. Debido a las investigaciones de Spitz, la concepción de la atención hospitalaria de niños pequeños permitió algunas modificaciones de relevante beneficio psicofísico en los niños que atraviesan situaciones de institucionalización.
Neurobiología del apego
De acuerdo con algunas investigaciones realizadas, si no se dan las condiciones adecuadas de interacción madre-hijo, el sistema del apego puede dejar de brindar su función protectora y convertirse, en sí mismo, en fuente de trastornos de diversos tipos (Lyons-Ruth et al., 2004).
El apego funda sus bases conceptuales en el imprinting, concepto que como ya se dijo deviene de la biología.
Las especies precociales (ya mencionadas), nacen con un nivel de desarrollo motor y perceptivo, por lo que muy rápi- damente pueden moverse y seguir a su objeto de referencia (seguir a su objeto materno).
El ser humano, en cambio, se encuentra entre las especies altriciales; las “crías” de estas especies nacen con los mecanismos perceptivos escasamente desarrollados y con poca movilidad. Dentro de las especies altriciales, el período de crecimiento del ser humano es especialmente lento y requiere un largo aprendizaje. Para que sea posible, resulta necesario que se desarrolle el proceso de apego, es decir, un tipo determinado de relación maternal que permita que el hijo sobreviva biológica y psicológicamente.
En las conductas de apego, las sustancias que intervienen son algunos neuropéptidos como la oxitocina y la prolactina, así como también los opioides endógenos como las endorfinas. Se demostró sobre todo en la investigación animal, que tanto los opioides cerebrales como los circuitos sobre los que actúa la oxitocina son activados por actividades sociales tales como el juego, el acicalamiento de las crías y la actividad sexual. Se postula entonces que los cambios en la acción de estos neuropéptidos sobre el cerebro pueden estar relacionados con el sentimiento de base segura del niño, así como con el comportamiento maternal en adultos (Panksepp, 1998).
La oxitocina es una hormona liberada en el sistema nervioso central por la neurohipófisis; ha sido estudiada en relación a su papel promotor de las contracciones del útero en el parto y con el amamantamiento. Se la ha estudiado también por su papel iniciador de comportamientos maternales de cuidado en numerosas especies.
En un estudio longitudinal de seis meses de seguimiento en parejas humanas (con 160 madres y padres que vivían con sus bebés recién nacidos) se demostró que los niveles de oxci- tocina aumentaron durante este período. Además, se encontró una correlación entre el aumento de oxcitocina y los compor- tamientos de contacto, vocalizaciones afectuosas, estimula- ción táctil y presentación de objetos (Gordon, Zagoory-Sharon, Leckman & Feldman, 2010).
Los opioides internos son neuropéptidos que tienen como función originaria calmar el dolor pero cuyapresencia también provoca sensaciones placenteras. La función de los opioides endógenos pudo ser corroborada en monos (Rhesus), los cuales aumentaban el nivel de su interacción social (aseo por pares) cuando recibían un bloqueador de los mismos (naltrexona) (Graves, Wallen & Maestripieri, 2002).
También se pudo observar que el desbalance de estos sis- temas químicos genera consecuencias psicopatológicas gra- ves. Por ejemplo, la depresión posparto y la psicosis puerperal han sido relacionadas con altos niveles de b-casomorfina, un opioide derivado de la leche que funcionaría como bloqueador de la producción de opioides endógenos (Nyberg, Linstrom y Terenius, 1988).
Las estructuras que conforman estos circuitos neurales, lla- mados de cuidado son: la corteza cingulada, el área septal, los núcleos basales de la estría terminal, la amígdala, el núcleo accumbens y algunas áreas del hipotálamo (Paanksepp, 1998). También se ha estudiado en diversas especies las respuestas en relación a la separación, en particular las vocalizaciones que realiza la cría cuando es separada de su madre, o el llanto en el ser humano. Hay otras manifestaciones posibles como la pérdida de apetito, del sueño, la irritabilidad o la depresión. El principal neuromodulador es el glutamato pero también participan la noradrenalina, la serotonina y el fac- tor de liberación de la corticotrofina (CRF) (Panksepp, 2006; Young, Liu & Wang, 2008). Existirían componentes comunes en el amor maternal, el comportamiento sexual y social, ya que estos mismos neuro- péptidos intervienen en los circuitos mencionados.
Se describen también los “reguladores ocultos” (hidden regulators) en el sistema, denominados así porque no son identificados como tales a través de la simple observación (Hofer y Sullivan, 2001). Por ejemplo, en ratas se ha estudiado cómo la disminución experimental del aseo a sus crías disminuye considerablemente el nivel de hormona de crecimiento de estas. Lo que explica que cuando la madre rata lame a su cría, está modulando la sensibilidad de determinados receptores a la serotonina, que a su vez regula la liberación de hormona de crecimiento por parte de la hipófisis. También se regularía la presión sanguínea de la cría a través del amamantamiento (Shair et al., 1986). Existirían diversos procesos biológicos de las crías que estarían regulados por “reguladores ocultos” que la madre ajustaría a través de la relación de apego, y que podrían aplicarse en humanos. Frente a una conducta maternal/ paternal abusiva, Bowlby sostuvo que, con la figura de cuida- do inicialmente las conductas de apego se incrementan para luego establecerse en un patrón de alejamiento (que puede derivar en distintos estilos de apego) (Bowlby, 1969).
Algunos autores desarrollaron un modelo experimental del apego en ratas, basados en premisas sobre el apego de Bowlby. Una de ellas es el desarrollo rápido de la conducta de apego hacia el cuidador, y la otra es la resistencia a extinguir estas conductas aún cuando haya un tratamiento abusivo por parte de aquel. Basaron sus estudios en la potenciación del condicionamiento del olor materno por parte de la cría y su resistencia en asociar un suceso aversivo con este olor (Mori- ceau y Sullivan, 2005).
Los autores sostienen que existe una adecuación del desarrollo del sistema nervioso para adaptarse a los distintos ambientes en los que se encuentra la cría.
En la línea de investigación relacionada con la epigenética, se ha demostrado cómo el comportamiento maternal de cuidado en ratas modifica la expresión de los genes encargados de expresar los receptores glucocorticoides en el hipocampo. Frente a un estímulo amenazador o estresor el hipocampo actúa sobre el hipotálamo generando la descarga del factor de liberación de corticotropina (CRF) sobre la hipófisis anterior, que a su vez, sintetiza y libera adrenocorticotropina (ACTH) sobre la corteza suprarrenal (Bale et al., 2002, 2004).
De esta manera, se liberan glucocorticoides, como el cortisol, que es clave en el mantenimiento de la respuesta al estrés, por ejemplo, favoreciendo el incremento del nivel de azúcar en la sangre y la metabolización de grasas, proteínas e hidratos de carbono. El nivel de glucocorticoides en sangre es captado por receptores en el cerebro, fundamentalmente en el hipocampo y otras zonas del prosencéfalo. Cuando se llega a un determinado umbral, el hipocampo inhibe la liberación de CRF y, a través de un mecanismo de retroalimentación negativa, se disminuye la respuesta al estrés (Weaver, Meaney & Szyf, 2006).
Muy significativo resulta que, cuanto más frecuente sea la conducta maternal de lamido a la cría en la primera semana de vida, mayor será la expresión genética de los receptores a glucocorticoides y, en consecuencia, menor la respuesta fren- te a eventos estresantes. Esta regulación, denominada epige- nética, se da a través de modificaciones funcionales del genoma que no involucran cambios en la secuencia de nucleótidos (Zhang & Meaney, 2010).
Llevados los estudios a seres humanos, se investigaron post mórtem neuronas del hipocampo de víctimas de suicidio con historia de maltrato infantil, sin historia de maltrato y controles (Mcgowan et al., 2009). Se concluyó que existían diferencias significativas entre los sujetos suicidas con historia de maltrato infantil y los demás, ya que tenían menos niveles de ARN mensajero de los receptores glucocorticoides, así como una metilación mayor del promotor de la expresión de éstos (NR3C1). Estos hallazgos pudieron relacionar una historia de maltrato en la infancia con una regulación epigenética de los receptores glucocorticoides, que promueve una mayor y más sostenida respuesta al estrés ante eventos amenazantes.
¿Cómo se define la epigenética?: Conrad Waddington (1905- 1975) acuñó y definió la epigenética como la “rama de la biología que estudia la interacción causal entre los genes y sus
productos, de los cuales emerge el fenotipo final” (Kaminker, 2007). Según Waddington la regulación epigenética mediaría la adaptación al medio ambiente, mediante la plasticidad del genoma, para generar distintos fenotipos ante las diferentes condiciones ambientales.
La epigenética se refiere, entonces, a los cambios heredables en la estructura y organización del ADN e histonas que no implican alteraciones en la secuencia de nucleótidos y que modifican la estructura y condensación de la cromatina, por lo que afectan la expresión génica y el fenotipo. Estas marcas generan modificaciones que afectan la actividad transcripcional de los genes y, una vez que se establecen, son relativamente estables en las generaciones siguientes (Morgan y Whitelaw, 2008). “Un sistema epigenético debe ser heredable, que se autoperpetúa y es reversible” (Riddihough y Zahn, 2010).
Por lo tanto, las modificaciones epigenéticas implican: metilación del ADN y modificaciones de las histonas, que producen un cambio en la expresión génica sin alteración del código genético (secuencia de bases de ADN descripta por Watson y Crick) (García et al., 2012).
Actualmente, el lamarckismo y la epigenética proponen una explicación para algunos efectos intergeneracionales en poblaciones humanas (Morgan y Whitelaw, 2008).
Los conceptos de Lamarck, descartados por la teoría moderna de la evolución, están resurgiendo en función de la evidencia que sugiere que los cambios epigenéticos son transmitidos de generación en generación y, por lo tanto, serían un mecanismo potencial de las influencias medioambientales que pueden ser heredadas de padres a hijos (postura teórica central de la evolución lamarckiana) (Handel y Ramagopalan, 2010) (Figura 1).
En esencia, los cambios epigenéticos ofrecen un mecanis-
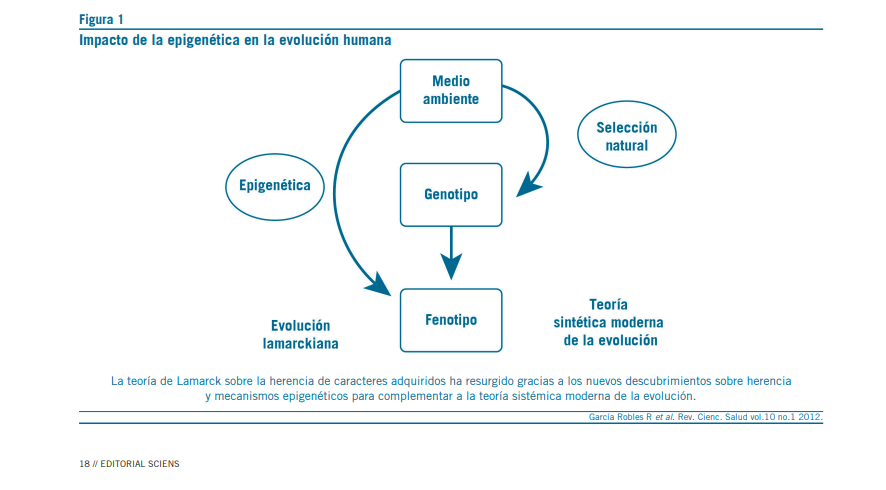
mo por el cual las experiencias vividas en un entorno deter- minado pueden modificar la función genética en ausencia de cambios en la secuencia de ADN (Medina y Alvano, 2016).
Se sabe que el genoma humano contiene alrededor de 30.000 genes codificantes; y que el estado de la cromatina es crítico para determinar cuándo, cómo y dónde debe efectuarse la transcripción de un gen en un producto determinado. La cromatina altamente condensada –heterocromatina– impide el acceso de los elementos activadores de la transcripción y determina el silenciamiento génico de la zona. En cambio, las regiones más laxas –eucromatina–, permiten el acceso de activadores que se acoplan con las regiones promotoras de los genes, y por lo tanto, el proceso de transcripción.
Se considera que las marcas epigenéticas regulan el estado “abierto” o “cerrado” de las regiones del genoma, o sea el estado activado o inactivado de los genes (Devaskar et al., 2007) (Figura 2).
Fenómenos epigenéticos
• la metilación del ADN
• la modificación de las histonas
• la intervención de secuencias de pequeños ARN no codi- ficantes.
Metilación del ADN: se sabe que el ADN está compuesto por cuatro bases diferentes que representan las letras del código genético: Adenina, Citosina, Guanina y Timina. En ocasiones el grupo químico metilo se añade a una base lo que agrega
un nivel de información extra. En organismos superiores la metilación está, en particular, restringida a la base citosina. La citosina metilada se asocia a la formación de cromatina “cerrada”, y en consecuencia con la desactivación de genes. La metilación puede estar sujeta a la acción de agentes am- bientales (Jaenisch y Bird, 2003; Feil, 2006).
Cofactores, como el ácido fólico y las piridoxinas que provienen de la ingesta, operan como dadores de grupos metilos. La impronta o “marcas de metilación” de un gen, que determinan su silenciamiento, se observa por ejemplo, en la inactivación del cromosoma X y en los genes parentalmente improntados.
En ciertos genes, una de las dos copias (la materna o la paterna) puede encontrarse normalmente “silenciada” por la impronta, con lo que se produce una expresión monoalélica, es decir de uno solo de los genes del par (ej., genes IGF2, factor de crecimiento insulínico tipo 2, y el receptor de IGF2). Un trastorno en este delicado proceso puede determinar alteraciones en el fenotipo generado por gametas con alteraciones de la impronta, como por ejemplo, en el síndrome de Beckwith Wiedemann. Este síndrome se caracteriza por sobrecrecimiento y propensión a tumores. En general, suele producirse porque un individuo puede recibir dos copias activas del gen IGF2, cuando normalmente solo una de las copias (la paterna) debe estarlo. Otro ejemplo relacionado con la impronta es el síndrome de Angelman y Prader-Willi (ambos involucran genes improntados de la misma región del cromosoma 15 (Devaskar, 2007; Godfrey, 2007).
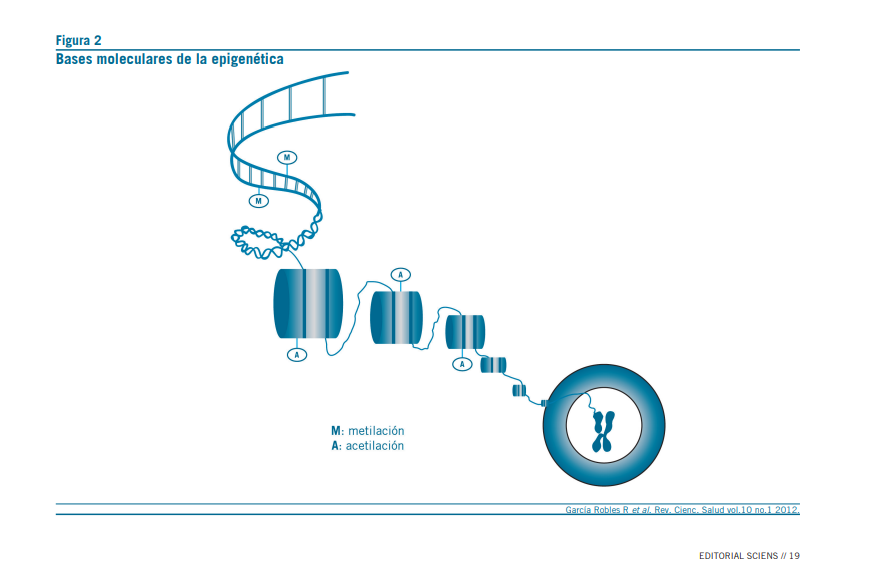
Modificación de histonas: se ha determinado que las histo- nas pueden sufrir modificaciones postraduccionales que alte- ran la condición de la cromatina. El nucleosoma consiste en 147 pares de bases de ADN, “enrolladas” en un octámero de histonas. Las modificaciones postraduccionales de las histonas consisten en particular en los siguientes procesos: acetilación, fos- forilación, deaminación, metilación, ubicuitinización, entre otros.
Hay estudios que apuntan a profundizar qué combinacio- nes específicas de modificaciones de las histonas pueden ser leídas como un código que determina, por ejemplo, si el gen implicado debería estar activado o inactivado, con lo cual se crea una nueva vía de señalización génica (Jaenisch y Bird, 2003; Jirtle y Skinner, 2007).
ARN no codificantes: pequeños ARN no codificantes pueden causar el silenciamiento génico a través de los denominados ARN de interferencia que portan un lugar regulatorio clave de la actividad génica. Esta característica está siendo utilizada para diversas terapéuticas. Se sabe que la secuencia de ADN de un gen no siempre determina un ARN que se traduce en proteína. El uso reciente de un modelo de ratón genéticamente ma- nipulado para provocar el síndrome de Rett demostró que la restauración de niveles normales de proteína MeCP2 (gen que codifica la proteína de unión a CPG de metilo 2) en las neu- ronas, revertiría los signos autistas que conforman parte del
síndrome (Devaskar y Raychaudhuri, 2007).
La heredabilidad de las marcas epigenéticas son un punto clave; en términos evolutivos los cambios estructurales de la cromatina, que están determinados por factores medioambien- tales, operarían como un determinante y cobrarían significación en el marco de la función adaptativa al medio (Feil, 2006).
De acuerdo con los estudios de Meaney y su grupo, la trans- cripción del gen que regula la expresión de los receptores glu- cocorticoides del hipocampo es alterada por el nivel de sero- tonina (5-HT). El mismo desencadena la activación de varias proteínas y factores transcripcionales potenciando la acción del promotor en la expresión de ese gen. Un aumento en los niveles de 5-HT en crías de ratas, producto de un lamido más frecuente en la primera semana de vida, regula en más la ex- presión genética de los receptores de glucocorticoides (Zhang & Meaney, 2010).
En esta línea de investigación, los hallazgos sobre la regu- lación epigenética a través de los comportamientos de apego muestran la interacción entre desarrollo, genética y psicopa- tología (Kendler & Greenspan, 2006).
Actualmente se sabe que los efectos del cuidado maternal en ratas también afectan la expresión del gen GAD1 (gen glu- tamato decarboxilasa), muy importante en la producción del neurotransmisor GABA y cuyas alteraciones en determinados circuitos neuronales están asociados a la esquizofrenia (Naka- zawa et al., 2011).
El apego en los primeros días de vida (en ratas) estaría rela- cionado con la resistencia a asociar el olor materno con suce- sos aversivos, y dicha resistencia cumpliría funciones adapta- tivas. Esta característica se relacionaría con cierta inmadurez de la amígdala en el período de aprendizaje inicial, hasta los
10 días de vida. Luego de esta etapa, la amígdala tendría un papel fundamental en el condicionamiento del miedo, por lo que se debe profundizar cómo influye el apego en el desarrollo de la amígdala y en todo el sistema neuronal de respuesta a la amenaza (Moriceau & Sullivan, 2005).
De acuerdo con los estudios realizados por Meaney, la res- puesta periférica a la amenaza es regulada epigenéticamente por los cuidados maternales (Zhang & Meaney, 2010). Aún no se han identificado con claridad los impactos hormonales, es- tructurales, de neurotransmisión y epigenéticos que producen los comportamientos maternales en el sistema córticolímbico. La epigenética cambia la perspectiva de la interacción de nuestro bagaje genético con el medioambiente y especialmen- te con condiciones nutricionales, ya que seríamos capaces de responder y adaptarnos a tales condiciones, además de trans-
mitir esta información a nuestros hijos (Heijmans, 2008). Acerca de la fisiopatología de la enfermedad humana, la in-
vestigación probablemente se dirija a revelar las condiciones que resultan de cambios epigenéticos y si es posible intervenir en el proceso para prevenir o curar la enfermedad (Handel et al., 2010). Desde otro punto de vista, son relevantes los estudios sobre el efecto en el desarrollo del sistema nervioso de las formas patológicas de apego, tanto en sus aspectos anátomo-fun- cionales (Moriceau, Raineki, Holman, Holman & Sullivan, 2009) como epigenéticos (McGowan et al., 2009). Los mismos permiten la estimación psicofisiológica del daño causado, la consecución de estrategias terapéuticas acordes y, en última instancia, la construcción de explicaciones más abarcativas
de estos fenómenos.
Conducta maternal y salud mental
Como ya fue mencionado, los efectos de la conducta ma- ternante temprana, que se registra en las conductas de aseo y cuidado de las crías (licking-grooming o LG), alteran la fun- ción del eje hipotalámico-pituitario-adrenal (HPA) y el desa- rrollo cognitivo y emocional. Esta conducta regula la expresión del gen del receptor de glucocorticoides (GR) en el hipocampo a través de la acetilación de las histonas y la metilación del ADN (Moriceau et al., 2009).
Los cuidados maternos frecuentes de atención al neonato tienen como consecuencia una menor producción de CRH y el aumento de la expresión de los GR en el hipocampo. Estos cambios permiten a las crías reaccionar de forma moderada, incluso en período adulto, a una situación de estrés.
Se señalan puntos centrales ligados a la conducta materna:
- Diferentes patrones de metilación en las crías de madres con alta o baja conducta maternante: las crías de madres con alta conducta maternante tienen menos sitios de metilación del ADN (menos silenciamiento génico) que las crías de ma- dres de baja conducta maternante. Estos diferentes patrones disminuyen la ansiedad y estimulan la propia conducta mater- nante de las crías cuando son adultas (transmisión transgene- racional) (Zieher y Guelman, 2006).
- Las ratas que fueron expuestas a estrés prenatal (PRS), presentaron hiperactivación de la respuesta HPA asociada a
una alteración del ritmo circadiano y de secreción aumentada de GC. También se pudo investigar trastornos del comporta- miento y altos niveles de ansiedad y depresión en la edad adulta (Darnaudery y Maccari, 2008).
- Durante los principios de la vida posnatal en los estudios realizados, las experiencias sociales tempranas tienen gran impacto, en particular la conducta materna e interacción en- tre pares, esta última estudiada en forma experimental a tra- vés del nido comunal (NC).
Las estimulaciones sociales tempranas afectan los niveles de neurotrofina a largo plazo. Se considera que la vulnerabilidad a trastornos psiquiátricos como la depresión se relaciona con alteración en los niveles de neurotrofinas, en especial de BDNF (Branchi et al., 2006). Una disminución sostenida en la metilación dentro del promotor BDNF puede mediar la ele- vación sostenida de transcripción BDNF en neuronas corticales (Feng et al., 2007).
Los cambios que se inducen en la crianza de cachorros dentro de un NC, como una mejor atención materna, parece ser transmitido durante al menos tres generaciones, incluso cuan- do la segunda y la tercera generación no vive en tales nidos (McEwen, 2008).
En un estudio realizado para constatar los efectos de la ad- versidad temprana en el desarrollo neuroconductual posterior, se efectuó la clasificación de las camadas (ratas) según la conducta materna (Sequeira-Cordero et al., 2013).
Así, dependiendo de la frecuencia de la conducta de LA durante los primeros días de vida (que podría ser equivalente a la infancia temprana en humanos), la muestra de ratas ma- cho fue subdividida en crías de madres con alto, medio y bajo LA, según el protocolo descrito por Champagne y col. (2003). Más tarde, para identificar los posibles efectos del cuidado materno, los dos grupos de crías fueron comparadas entre sí a las cuatro semanas de edad con respecto a una serie de parámetros conductuales y neurobiológicos (Sequeira-Corderoet al., 2013).
El estudio de conductas relacionadas con la ansiedad fue realizado con la prueba de campo abierto, donde el animal puede explorar libremente (Gould y et al., 2009).
Animales poco ansiosos, al menos en la cepa utilizada en este estudio (Sprague-Dawley), tendieron a desplazarse me- nos que los animales más ansiosos. Las crías de madres con bajo cuidado (ambiente temprano adverso) se desplazaron más, lo cual fue interpretado como un indicativo de mayores niveles de ansiedad, en comparación con las crías de madres con alto cuidado.
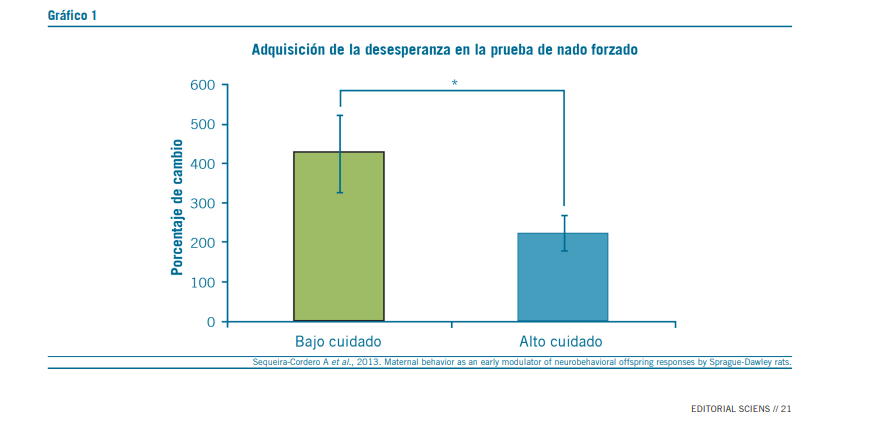
Por otro lado, también analizaron conductas relacionadas con la depresión utilizando la prueba de nado forzado (Slat- tery y Cryan, 2012). En esta prueba se pone al animal a nadar en un tanque de agua durante una primera sesión, en la cual aprende que no hay escapatoria posible. Un día después, en una segunda sesión, al enfrentarse de nuevo al estrés de tener que nadar sin posibilidad de escapatoria, el animal expresa altos niveles de inmovilidad, es decir, permanece únicamente flotando.
Esta conducta se menciona como reacción de desesperanza y ha sido relacionada con conductas depresivas. La adquisición de la desesperanza (incremento en el tiempo de inmovilidad en la segunda sesión con respecto a la primera) fue mayor en animales con bajo cuidado LA (Gráfico 1).
Adquisición de la desesperanza según el cambio en el tiempo de inmovilidad entre la preprueba y la prueba. El porcentaje de cambio en el tiempo de inmovilidad entre sesiones es significativamente mayor en crías de madres con bajo LA.
Para considerar el sustrato neurobiológico implicado investigaron las diferencias entre crías con alto y bajo LA, en tres regiones cerebrales: corteza prefrontal, hipocampo y núcleo accumbens. Los animales con bajo cuidado presentaron niveles más bajos en la neurotransmisión de serotonina y menores niveles de expresión del gen TrkB (tirosin quinasa B) en el
núcleo accumbens, al compararlos con crías de madres con alto cuidado. Por otro lado, no encontraron diferencias entre ambos grupos con respecto a las mediciones hechas en hipo- campo y corteza prefrontal.
De acuerdo con estos resultados, propusieron que el cui- dado materno es capaz de modular la neurotransmisión de serotonina en el núcleo accumbens y esto, a su vez, podría regular la expresión del gen TrkB (Sequeira-Cordero et al., 2013). Este gen codifica el receptor de la neurotrofina BDNF, proteína relevante en el cerebro que participa en la regulación de numerosos procesos fisiológicos y conductuales.
Es entonces que, el bajo cuidado de las crías y un ambiente temprano adverso se correlacionan con una disminución en la transmisión serotoninérgica y en la expresión del receptor TrkB y, por lo tanto, con una disminución en las vías de se- ñalización que controlan diferentes procesos cerebrales. Esto podría estar asociado con el desarrollo de conductas relacio- nadas con la ansiedad y la depresión.
En el trabajo proponen, además, como hipótesis, que la mo- dulación en la expresión del receptor TrkB podría estar sujeta a algunos mecanismos de regulación epigenética (metilación del ADN y modificaciones de proteínas histonas), como había sido previamente reportado (Weaver et al., 2004; Champagne et al., 2003).
Gen-ambiente
En un estudio realizado para investigar la relación gen-am- biente se constató que los estilos de apego se establecen poco después del nacimiento y forman la base para una vida psicológica saludable durante la adultez. Se investigó si los antecedentes genéticos (es decir, cepas isogénicas: C57BL
/ 6N y BALB / c) y los efectos epigenéticos influyen en los estilos de fijación en ratones, descubriendo que un surtido genético y epigenético específico desempeña un papel en el desarrollo de un estilo de fijación seguro o inseguro (Lassi y Tucci, 2017).
Cuando las madres biológicas cuidan a sus crías, el estilo de apego es principalmente seguro, independientemente del entorno genético. Sin embargo, cuando las madres de crianza crían cachorros, el estilo de apego puede ser seguro o inseguro. Se observó también que la fijación segura de los ratones conduce a una mayor sociabilidad durante la adultez, mientras que una fijación insegura conduce a una sociabilidad reducida. Los bebés con apego seguro confían en su cuidador principal como una base segura y desarrollan autonomía, una autoimagen positiva y la capacidad de entablar relaciones emocional- mente cercanas (Bucci et al., 2016), mientras que el apego inseguro se desarrolla cuando el cuidador no es consistente y no responde a las necesidades del bebé. Las consecuencias de los estilos de apego disfuncionales varían y afectan adversamente la personalidad, la seguridad, la emocionalidad y la sociabilidad de los adultos (Bremner, 2003; Heim y Nemeroff, 2001; Landers & Sullivan, 2012; Sheinbaum et al., 2015; Sullivan, 2012).
El estudio fue realizado con ratones como un modelo para comprender los componentes genéticos y epigenéticos de los estilos de apego temprano y las consecuencias de este apego en la edad adulta (Tabla 1).
Se basaron en los diferentes estilos de maternidad de dos cepas cosanguíneas comunes: BALB / c y C57BL / 6N. Mien- tras que las cepas BALB /c, pasan menos tiempo lamiendo a sus cachorros y muestran menos cuidados, las cepas C57BL / 6N son reconocidas como “buenas madres” (Calatayud et al., 2004; Priebe et al., 2005; Tarantino et al., 2011).
Para evaluar los comportamientos de apego en niños de 1 año, Ainsworth ideó el procedimiento de situación extraña (SSP) (Ainsworth et al., 1978). Es una prueba de comporta- miento basada en la tendencia natural de los bebés a unirse a los cuidadores, preferentemente la madre. En el SSP, se registra durante varios episodios cortos en una habitación, durante los cuales el bebé está en presencia de la madre y/o un extraño. Después de una evaluación de los estilos de interacción entre la madre y el bebé, el experimento evalúa la respuesta del bebé en presencia de una mujer desconocida (extraño) junto con la madre y luego en presencia del extraño solo. En este punto, la madre regresa mientras el extraño sale
Tabla 1
La interacción genambiente influye en el estilo de apego en los ratones
| Número de animales testeados para cada condición experimental | ||||
| Madre | Genotipo | Número de camadas | Número de cachorros por camada | Número total de cachorros |
| 1. El número total de animales testeados fue de 140. Se testearon dos camadas para cada genotipo. Cada camada fue de 6 o 10; 64 cachorros fueron de crianza, mientras que 76 fueron criados por sus madres biológicas. | ||||
| Biológica | (A) C57Bl/6N | 2 | 10, 10 | 20 |
| (B) F1r | 2 | 10, 10 | 20 | |
| (C) F1 | 2 | 10, 6 | 16 | |
| (D) BALB/c | 2 | 10, 10 | 20 | |
| De Crianza | (A) C57Bl/6N | 2 | 10, 6 | 16 |
| (B) F1r | 2 | 10, 6 | 16 | |
| (C) F1 | 2 | 10, 6 | 16 | |
| (D) BALB/c | 2 | 10, 6 | 16 | |
G. Lassi G, Tucci V. Gene-environment interaction influences attachment-like style in mice. 2017.
de la habitación, y luego el bebé queda solo; el extraño regresa y luego la madre regresa antes de que el extraño se vaya para siempre. El bebé pasa por un total de ocho episodios situacionales. El objetivo principal de esta evaluación es de- terminar el estilo de apego basado en el interés mostrado por el niño hacia el extraño, y el comportamiento de buscar con- suelo en la madre una vez que el infante y la madre se reúnan. El principal resultado de esta evaluación es que el estilo de apego se clasifica como seguro o inseguro (Ainsworth et al., 1978; Sheinbaum et al., 2015). El apego seguro está representado por la exploración activa del extraño, especial- mente cuando la madre está en la habitación, y luego busca el consuelo de la madre cuando regresa. El apego se interpreta como inseguro cuando el bebé evita al extraño y luego muestra evitación o indiferencia hacia la madre cuando regresa a la habitación.
En este estudio modificaron el SSP para estudiar el comportamiento similar a un accesorio en cachorros de ratón. Los resultados del estudio muestran importantes efectos genéticos y epigenéticos en la determinación de estilos particulares de apego y rasgos de comportamiento adulto.
Las conclusiones a las que arribaron:
- Tomados en conjunto, los comportamientos de los ratones llevaron a definir diferentes estilos de apego según las diferencias genéticas, epigenéticas y ambientales.
En particular, observaron que los ratones C57BL/6N presentaban los tres marcadores de comportamiento (es decir, preferencia materna, reunión con la madre y exploración del extraño) de un estilo seguro de apego, mientras que los ratones BALB/c mostraban solo dos de los tres marcadores positivos. El último grupo no exhibió la exploración de rebote de las madres durante su reunión; buscar a la madre en la versión humana de la prueba atestigua la unión segura del bebé (Ainsworth et al.,1978; Sheinbaum et al., 2015).
- Por lo tanto, aunque la mayoría de los cachorros criados por sus madres biológicas mostraban signos de apego seguro, los cachorros criados por madres adoptivas exhibían conduc- tas de apego seguras o inseguras de acuerdo con su genotipo. Además, observaron que cuando las madres adoptivas criaban a sus cachorros, todas las respuestas conductuales para defi- nir estilos específicos de apego eran impulsadas por el padre, con una especie de apego seguro en los descendientes de padres C57BL/6N, mientras que el apego inseguro ocurría en los descendientes de padres BALB/c.
- Como dato interesante refieren la observación en otros roedores, como los conejillos de Indias, en los cuales los ca- chorros prefieren estar más cerca de las madres que de otros adultos y la presencia de la madre es más efectiva para redu- cir los niveles de estrés, en comparación con otras mujeres adultas, cuando el cachorro se coloca en un entorno nuevo. (Hennessy et al., 2003).
- El apego también ha sido explorado, en ratas, por el grupo de Regina Sullivan. Su grupo ha descripto la neurobiología del apego y le ha asignado un papel principal a la amígdala
(Sullivan et al., 2000).
Demostraron que el apego ocurre incluso con traumas y/o un cuidador abusivo; descubrieron que la presencia de la presa suprimía la respuesta del cachorro a una amenaza o un aprendizaje aversivo permitiendo así que el joven sobreviviera, aunque con efectos psicológicos a largo plazo que podrían hacerse evidentes con la maduración (Perry y Sullivan, 2014). No se ha determinado un efecto directo de un gen impreso en el desarrollo del comportamiento de apego. Se piensa que los genes expresados por el padre maximizan la asignación de recursos a los cachorros, mientras que los genes expresados por la madre conducen a una distribución igual entre los descendientes. La explicación evolutiva de esta diferencia reside en una mayor relación materna que paterna entre los cachorros en desarrollo. En consecuencia, la expresión de un gen según el origen parental puede promover la explotación de los recursos maternos por parte del cachorro (o infante).
De hecho, si bien el papel clave de la madre es proporcionar nutrientes, prenatalmente (Reik et al., 2003) y perinatal- mente (Plagge et al., 2004), en el período posnatal se vuelve fundamental la promoción de señales positivas en el sistema sensorial de la madre (Wilkinson et al., 2007). Por último, los estilos de apego pueden predecir la interacción social adulta. Las experiencias de la vida temprana tienen efectos importan- tes a lo largo de la vida de un individuo (Roth y Sweatt, 2011).
Diversos enfoques clínicos han sugerido que la vida psico- lógica adulta a menudo es una expresión del estilo de apego durante la infancia. Además, los estudios a largo plazo han demostrado que un estilo de apego particular en los humanos es relativamente estable desde la infancia hasta la adultez temprana (Waters et al., 2000; Sheinbaum et al., 2015).
Kandel. Principios
Kandel en su artículo “Un nuevo marco teórico para la Psiquiatría”, postula un reencuentro de la Psiquiatría y la Psicología con la Biología, que él propone como la base epistemológica sobre la cual se podría desarrollar la teoría y la práctica psiquiátrica y psicológica dentro de parámetros científicos (Kandel, 1998).
Este autor enunció sus principales ideas enmarcándolas en cinco principios; en el cuarto de ellos señala que las alteracio- nes en la expresión de genes inducidas por el aprendizaje dan lugar a cambios en los patrones de conexiones neuronales. Estos cambios, según Kandel, no sólo contribuyen a las bases biológicas de lo individual, sino también podrían ser respon- sables de la iniciación y el mantenimiento de alteraciones de la conducta inducidas a través de sucesos de orden social.
Los estudios realizados por Kandel en el caracol marino Aplysia han brindado evidencia que el aprendizaje produce cambios sostenidos en la efectividad de las conexiones sináp- ticas alterando la expresión de genes, es decir, en la función transcripcional de los mismos (Olds, 1975).
También las investigaciones ya mencionadas en ratas, muestran que las diferencias individuales en la expresión de genes en regiones del cerebro que regulan la reactividad al estrés pueden ser trasmitidas de una generación a otra por medio de las variaciones del cuidado maternal de las crías.
Estos descubrimientos han sido indicadores acerca de las variaciones en el cuidado maternal como base para la transmi- sión comportamental no genómica de generaciones (Francis et al., 1999).
En su quinto y último principio, Kandel afirma que “si la psicoterapia es efectiva y produce cambios de larga duración en el comportamiento, presumiblemente hace esto median- te mecanismos de aprendizaje, que producen cambios en la expresión de los genes que alteran a la vez la fuerza de las conexiones sinápticas y los cambios estructurales y también modificando el patrón anatómico de interconexiones entre las células nerviosas del cerebro” (Kandel, 1991).
Por lo tanto la psicoterapia por medio de la palabra puede obtener mejorías en el paciente y, a su vez, se producen nece- sariamente cambios en el cerebro del mismo.
Algunos estudios mostraron una disminución de la actividad de una región del núcleo caudado en sujetos con trastorno obsesivo compulsivo que fueron tratados exitosamente con un tratamiento conductual (prevención de la respuesta) o con un psicofármaco (Fluoxetina). Mientras que los sujetos que no mejoraron con ninguno de esos tratamientos mantuvieron alta la actividad de ese núcleo cerebral.
Este trabajo fue fundamental para mostrar que los tratamien- tos cognitivos-conductuales basados en los principios del apren- dizaje modifican las conexiones neuronales de modo semejante a como lo hacen los psicofármacos (Baxter et al., 1992).
Epigenética y psicofármacos
Se sabe que las variables del entorno como ciertos psicofármacos pueden producir modificaciones epigenéticas (Medina y Alvano, 2016).
En relación a los antidepresivos en particular, si bien no contrarrestan en forma directa los efectos del estrés, tendrían la capacidad de restablecer la funcionalidad del circuito involucrado en la depresión.
El tratamiento crónico con antidepresivos provoca una translocación de la PKA (proteinquinasa A), aumentando su actividad en el núcleo donde genera la fosforilación y la activación del CREB (Factor de transcripción) (Nestler et al., 1989). El CREB puede mediar la acción de la vía de señalización intracelular del AMP cíclico (AMPc).
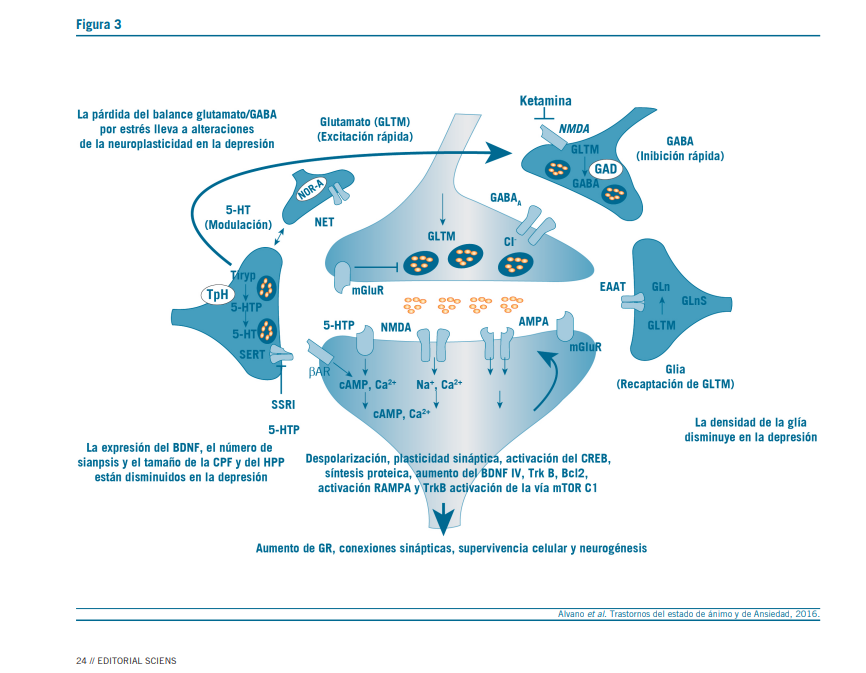
La fosforilación del CREB conlleva mecanismos epigenéti- cos ya que promueve la activación y la unión de un coactivador de la transcripción: CBP (proteína de unión del CREB); esta provoca la acetilación de histonas –actividad HAT intrínseca, histona acetil transferasa–, se abre la cromatina, facilitándose la unión del CREB al CRE y la subsiguiente activación trans- cripcional del BDNF (Wang et al., 2008).
La administración crónica de diferentes antidepresivos pro- duce el aumento de neuronas piramidales del área CA3 y las células granulares del giro dentado del hipocampo, en regiones límbicas y en corteza prefrontal (CPF). Es de señalar que el estrés produce disminución de esta neurotrofina. Otra vía de señalización, la MAP quinasa (MAPK) está relacionada con la supervivencia neuronal, la formación de memorias y diversos cambios plásticos. Por ella se fosforilará al CREB induciendo la expresión de Bcl-2, principal proteína antiapoptótica.
También se menciona otra vía de señalización utilizada por el receptor TrkB, la fosfatidilinositol-3´quinasa (PI3K), por la cual el BDNF inactiva proteínas proapoptóticas como la Bad. El corolario sería: antidepresivos: efectos neurotróficos: in- trincada maquinaria celular: CREB/BDNF/TrkB/MAPquinasa/ Bcl-2. Por lo tanto la acción del estrés sobre un organismo predispuesto implicaría en la fisiopatología de la depresión la disrupción de la neuroplasticidad, que sería bloqueada o revertida por los antidepresivos (Alvano, 2016) (Figura 3).
La represión del gen del BDNF originada por el estrés puede ser revertida por la Imipramina, según fuera demostrado por Nestler, al inducir una acetilación de la histona: el mecanismo de acción de la imipramina es la disminución selectiva en el hipocampo de los niveles de la enzima histona deacetila- sa-5 (HDAC-5) (Tsankova et al., 2007).
Los cambios de larga duración en la expresión de los factores neurotróficos y otras señales moleculares por alteraciones epigenéticas, se relacionaron con la depresión y la respuesta al tratamiento (Duman, 2013).
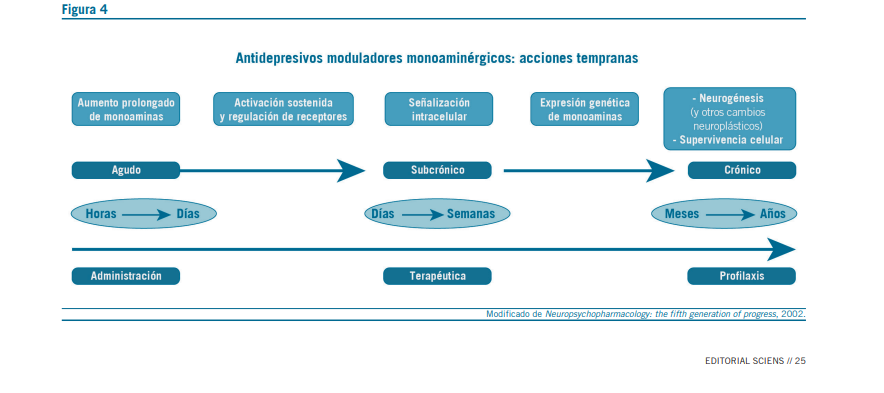
Se ha informado como efecto del tratamiento antidepresivo crónico, aumento de la neurogénesis y de la arborización dendrítica en el hipocampo (Willner et al., 2013) y en la corteza prefrontal medial (CPFm) (Duman, 2013) (Figura 4).
Si bien se sabe por diferentes estudios realizados que las acciones de los antidepresivos mediadas por el BDNF son esenciales, podrían intervenir otros factores neurotróficos. Uno de los más estudiados ha sido el factor de crecimien- to del endotelio vascular (vascular endothelial growth factor, VEGF). Se ha demostrado que mientras el BDNF es requerido para la supervivencia de las nuevas neuronas, en el proceso de proliferación estaría involucrado principalmente el VEGF (Will- ner, 2013).
Otros factores a considerar son: el factor de crecimiento 1 similar a la insulina y el factor de crecimiento de fibroblastos. Si bien el BDNF tiene efectos de tipo antidepresivo en el hipocampo, cuando se administra en el núcleo accumbens (NAc), provoca lo contrario, un efecto prodepresivo. De todas maneras, el tratamiento sistémico y crónico con BDNF tiene efectos antidepresivos lo que indica que el efecto en el hipocampo es el que predomina (Willner, 2013). Los tratamientos crónicos con antidepresivos aumentan la neurogénesis en el giro dentado del hipocampo (Surget et al., 2008).
La activación de sinapsis serotoninérgicas y noradrenérgicas en el hipocampo aumenta la producción de factores neurotróficos, lo que lleva a la reparación del daño morfológico producido por el estrés.
En la depresión hay una información afectiva sesgada, con un incremento de la activación de la amígdala y disminución de la respuesta del NAc, ambas estructuras reguladas por la habénula lateral (HBL). Esta es activada por el estrés y su principal eferencia es el núcleo dorsal del rafe (NDR) y en segundo lugar el área tegmental ventral (ATV) (Willner, 2013). Como dato significativo se ha propuesto en forma reciente un modelo alternativo “neuropsicológico cognitivo” donde se plantea que los antidepresivos causan cambios relativamente rápidos en el procesamiento de información emocional, pero
sin embargo la mejora anímica es lenta ya que el paciente debe volver a aprender asociaciones emocionales (Pringle et al., 2011; Roiser et al., 2012).
En otras investigaciones realizadas con modelos de roedores expuestos a estrés crónico se estudiaron los mecanismos moleculares de la depresión (Chistiakov et al., 2017). En estos modelos, la exposición temprana al estrés crónico, como el estrés prenatal o posnatal, indujo respuestas de estrés hiperactivas a largo plazo, anomalías del comportamiento y deficiencias funcionales en la función cerebral que persisten en la edad adulta. Además, estas alteraciones pueden transmitirse a descendientes de animales crónicamente estresados a través de varias generaciones. Es así que el estrés crónico produjo cambios epigenéticos estables en regiones cerebrales, principalmente en el sistema límbico. El tratamiento con antidepresivos pudo modificar la programación epigenética que fue inducida por el estrés anormal. Se sabe que el fracaso para hacer frente al estrés puede predisponer a un amplio espectro de enfermedades somáticas, como cáncer o patología cardiovascular, y participar en el inicio de anormalidades del estado de ánimo como depresión y trastornos de ansiedad (Wood y Valentino, 2017); McCrory et al., 2012). Estas modificaciones que forman parte entre otras de los mecanismos epigenéticos, están mediadas por una maquinaria enzimática epigenética especial que incluye ADN metiltransferasas (DNMT), histonas acetiltransferasas (HAT), histonas desacetilasas (HDAC) y otras enzimas.
Los estudios en estos modelos animales mostraron que la experiencia de la vida temprana, incluidos los eventos estre- santes y el cuidado materno, influyen en las respuestas al estrés a través de la programación epigenética a largo plazo (Bale, Baram et al., 2010).
La adversidad temprana modulaba la acetilación de la his- tona a través de cambios en los niveles de HDACs. En ratones adultos, la separación maternal condujo a niveles reducidos de HDACs en el cerebro anterior asociado con la elevación paralela en la marca H4K12 acetilada (Levine y Worrell et al., 2012). En los estudios se pudo demostrar que la terapia crónica con imipramina suprime la transcripción de CRH e induce hiperme- tilación de ADN en el locus de CRH solo en ratones sometidos a estrés social (Elliott, Ezra-Nevo, Regev et al., 2010). Otros investigadores mostraron reducción crónica inducida por el estrés de la acetilación de H3 en el hipocampo. La disminución en el hipocampo en la acetilación de H3 fue re- vertida por la imipramina (Hollis, Wang, Dietz, Gunjan et al., 2010; Hollis, Duclot, Gunjan, Kabbaj, 2011). La abundancia de datos generados a partir de modelos de roedores con estrés crónico sugiere un papel suficiente de modificaciones epigenéticas en la inducción y la regulación de las anomalías transcripcionales globales que pueden con- tribuir sustancialmente a la depresión. En comparación con el estrés adulto, las alteraciones inducidas por eventos adversos tempranos, como el estrés prenatal y el posnatal, tienen efectos más fuertes y más largos que pueden transmitirse a través de las generaciones. Los estudios epigenéticos actuales evolucionan para analizar genes candidatos individuales a la implicación del genoma con técnicas integradas como el uso combinatorio de ChIP-seq (método utilizado para analizar las interacciones de proteínas con el ADN).
Si se considera un papel exclusivo de las alteraciones del hipocampo en la patogenia de la depresión y otras enfermedades relacionadas con el estrés, la remodelación anormal de la cromatina en el hipocampo puede conducir a la sobreactivación de muchos retrotransposones –elementos genéticos que se pueden amplificar a sí mismos en un genoma y son ubicuos componentes del ADN de muchos organismos eucariotas– cuyo papel en el desarrollo de enfermedades neuropsiquiátricas debe ser investigado más a fondo.
Otro aspecto es la función en relación con el estrés, de la hidroximetilación del ADN en el cerebro poco conocida y se sugiere un posible papel de esta marca epigenética en la fun- ción neuronal (Houston et al., 2013).
En una revisión sistemática de la literatura en relación a los medicamentos utilizados para el tratamiento de los trastornos bipolares –estabilizadores del ánimo y antipsicóticos– y las modificaciones epigenéticas (Lockwood y Youssef, 2017) se incluyeron seis estudios con criterios de inclusión preespecificados. En estos estudios se investigaron los efectos epigenéticos con litio y ácido valproico administrados a ratas (Lee et al., 2015). Pudieron encontrar un aumento en la expresión de Leprgen Lepr, receptor de la leptina– al observar las células del hipocampo de las ratas que habían sido tratadas con litio y ácido valproico durante 30 días. Las alternancias epigenéticas en este estudio pueden explicar el mecanismo de acción, al menos en parte, para estos dos medicamentos. Sin embargo, los autores plantean que lo observado podría ser el efecto secundario metabólico relacionado con la leptina, diferenciándolo del efecto estabilizador del estado de ánimo. En otro estudio investigaron la metilación en personas du- rante diferentes estados de ánimo (maníaco, hipomaníaco, mixto, eutímico y deprimido) y analizaron los efectos del ácido valproico y el litio sobre la modulación BDNF (Dell’Osso et al., 2014). Los investigadores analizaron los niveles de BDNF a través de muestras de sangre periférica de células mononu-cleares y hallaron que, en un estado de ánimo mixto o maníaco, los niveles de metilación del BDNF se aproximaban a la de los sujetos control, pero que los pacientes en estado eutímico o deprimido tenían significativamente mayores niveles de metilación de BDNF. Se consideró de gran valor que en el estudio se examinara específicamente los estados de ánimo. Aunque en esta investigación la disminución en la metilación de BDNF no se mostró en un nivel estadísticamente significativo, se cree que es posible que el nivel pueda alcanzar significación con un tamaño de muestra más grande.
En la línea de investigación con antipsicóticos, Melka y colaboradores realizaron dos estudios para investigar los efectos de la olanzapina en ratas (Melka et al., 2013; Melka et al., 2014). De los genes investigados en el primero de los trabajos –un estudio preliminar por la cantidad pequeña de ratas que integraron la muestra–, 19 de 40 mostraron diferencias
significativas de metilación cuando fueron tratadas con olanzapina. Los mismos representan principalmente aumentos en la metilación en el hipocampo. Por otro lado, encontraron muchos cambios en la expresión de dopamina secundaria a la administración de olanzapina (Melka et al., 2013).
Posteriormente, Melka y colaboradores profundizaron el primer estudio para investigar los efectos epigenéticos de olanzapina en el cerebelo, el hígado y el hipocampo de ratas, ampliando la muestra. Como en el estudio anterior, encontraron que los cambios en la metilación observados eran específicos del tejido. En el hipocampo hubo un aumento significativo de la metilación en la vía dopamina-DARPP32 (fosfoproteína neuronal). También hubo una disminución en la metilación en CDC42 (proteína de unión). Este estudio confirmó los resultados obtendios en la primera investigación y aclaró algunos de los cambios epigenéticos que se observaron al administrar olanzapina (Melka et al., 2014).
Una de las implicaciones prácticas de descubrir los efectos epigenéticos de diferentes medicamentos es guiar aún más la estadificación y el tratamiento de pacientes, por ejemplo con trastorno bipolar, con el fin de proporcionar una mejor y más personalizada atención.
Es importante señalar, también, los cambios neuroplásticos posibles de las psicoterapias, de diferente marco teórico, con un efecto denominado top down, es decir de arriba hacia abajo (el efecto de los antidepresivos es bottom up, de
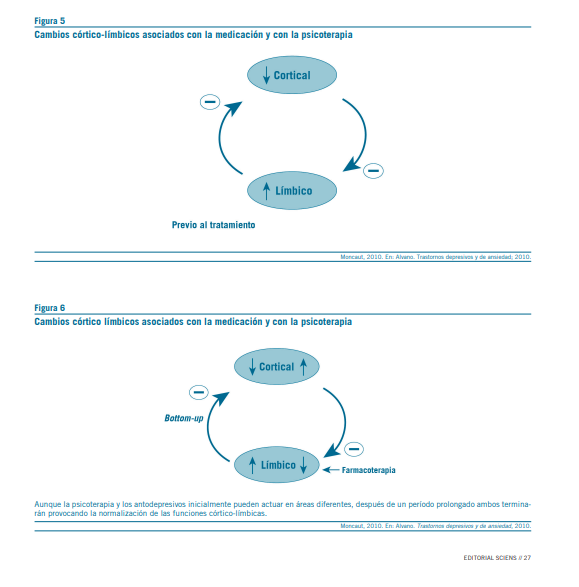
abajo hacia arriba), capaz de regular áreas límbicas como la amígdala, con aumento de la actividad cortical, CPF (Alvano, 2010; De Rubeis, 2008; Alvano y Moncaut, 2016) (Figuras
5 y 6).
Retomando, vemos entonces, que la literatura actual mues- tra que algunos de los medicamentos psiquiátricos investiga- dos pueden tener efectos epigenéticos. Por lo tanto, compren- der mejor las complejidades del epigenoma y profundizar los posibles efectos y contribuciones de los medicamentos en los diversos estados de enfermedad, deviene crucial para el futu- ro del diseño de fármacos y el desarrollo de nuevas terapias.
Conclusiones
• Neurodesarrollo y ambiente constituyen pilares centrales desde las primeras etapas de la vida.
• De acuerdo con la investigación realizada en el presente trabajo, se sabe que el cerebro está sujeto a influencias am- bientales que actúan en su estructura y función.
• La plasticidad cerebral subraya la capacidad de resistir y adaptarse dinámicamente a estímulos del estrés ambiental. Es entonces que el estrés de la vida temprana afecta diferentes funciones y estructuras en el neurodesarrollo y puede conducir a trastornos de diferente gravedad. Se concluye, además, que el estrés de la vida temprana puede explicar un mayor efecto epigenómico, que el de la vida adulta.
• Sabemos que un bebé requiere de un adecuado ambiente que estimule su desarrollo y maduración; el apego (atta- chment), definido por Bowlby contribuye a la supervivencia física y psíquica del sujeto generando seguridad y facilitando el conocimiento del mundo, en la medida que el niño va conformando modelos de representación internos. La interrupción temprana de la relación de apego madre-hijo tiene un efecto negativo en la plasticidad del cerebro y predispone a trastor- nos de diversas características.
• En los estudios realizados en modelos animales se constató que, cuanto más frecuente es la conducta maternal de lamido a la cría en el primer tiempo, mayor será la expresión genética de los receptores a glucocorticoides y, en consecuencia, será menor la respuesta frente a eventos estresantes. Esta regulación denominada epigenética, se da a través de modificaciones funcionales del genoma que no involucran cambios en la secuencia de nucleótidos.
• Diferencias significativas se subrayan en sujetos suicidas con historia de maltrato infantil, donde se hallaron menos niveles de ARN mensajero de los receptores glucocorticoides, así como una metilación mayor del promotor de la expresión de estos (NR3C1). Estos hallazgos pueden relacionarse con una regulación epigenética de los receptores glucocorticoides, que promueve una mayor y más sostenida respuesta al estrés ante eventos amenazantes y traumáticos.
• La epigenética cambia la perspectiva de la interacción de nuestro bagaje genético con el medioambiente, ya que seríamos capaces de responder y adaptarnos a tales condiciones, además de transmitir esta información a nuestros hijos.
• Por lo tanto, los hallazgos sobre la regulación epigenética a través de los comportamientos de apego, muestran la inte- racción entre desarrollo, genética y psicopatología.
• Algunos psicofármacos pueden producir también modificaciones epigenéticas. En la fisiopatología de la depresión, la disrupción de la neuroplasticidad por acción del estrés sería bloqueada o revertida por los antidepresivos.
• Se constató, como efecto del tratamiento antidepresivo crónico, en algunos de los estudios efectuados, el aumento de la neurogénesis y de la arborización dendrítica en el hipocampo y en la corteza prefrontal medial (CPFm) y el incremento de la producción de factores neurotróficos como el BDNF, lo que lleva a la reparación del daño morfológico producido por el estrés.
• La terapéutica epigenómica podría ser muy prometedora para el tratamiento de enfermedades complejas y las interven- ciones personalizadas, entre estas los trastornos psiquiátricos.
• Es posible, entonces, que con el conocimiento de los mecanismos epigenéticos, las “drogas epigenéticas” puedan ser la próxima vanguardia de la psicofarmacología.
• Es dable destacar que la antinomia histórica “natura-nurtura” ha sido superada, sentando así las bases para nuevos abordajes en los conceptos de salud y enfermedad.
• Es así que el “dogma” de la era genética atraviesa una innovadora “revolución”, considerando la relevancia y el “engranaje” particular entre la secuencia de genes y el contexto de su ambiente.
Agradecimientos
A mi Papá, “arborización dendrítica” en mi ser y mi familia, y con él a mi Mamá también, quien pocos meses antes de emprender “su nuevo viaje”, me impulsó a concluir este trabajo.
¡Siempre gracias!
A mi familia toda (un tono de color mayor a mi esposo y mis hijas) y a mis amigos, que siempre están.
Un agradecimiento particular a los Directores y a la Coordinadora de la Maestría que me permitieron este nuevo y fructífero aprendizaje.
Bibliografía
• Ainsworth, M. D. S. Object relations, dependen- cy and attachment: a theoretical rewiev of the in- fant-mother relationship. Child Development. 1969: 40:969-1025.
• Ainsworth, M. D. S., Blehar, M. C.; Waters, E. & Wall, S. Patterns of attachment: A psychological study of the strange situation. Nd ed. Oxford, UK: Erlbaum, Hillsdale, NJ. 1978.
• Alvano, S. A. Modulación de la fisiopatología de los trastornos depresivos y de ansiedad por antidepresi- vos. En: Alvano, S. A. et al. Ed. Trastornos depresivos y de ansiedad: aspectos neurobiológicos, clínicos y terapéuticos. Buenos Aires: Sciens; 2010:87-98.
• Alvano, S. A. Trattamento combinato psicotera- péutico e psicofarmacológico nei disturbi depressivi e d´ansia. Sono efficaci le psicoterapie psicodina- miche e la psicoanalisi? Fondamenti storici e neu- robiologici. Risultati clinici. Revista Sperimentali di Freniatría 2012;CXXXVI (1):47-83.
• Alvano, S. A. Modulación de la fisiopatología de los trastornos depresivos y de ansiedad por anti- depresivos. En: Alvano, S. A. et al. Trastornos del estado de ánimo y de ansiedad. Aspectos neurobio- lógicos, clínicos y terapéuticos. 1ra ed. Ciudad Au- tónoma de Buenos Aires: Sociedad Iberoamericana de Información Científica, SIIC, 2016: 145-160.
• Alvano, S. A.; Moncaut, M. Psicoterapia y niveles de evidencia. La importancia del tratamiento com- binado. Fundamentos históricos y neurobiológicos. Evidencia clínica. En: Alvano S. A. et al. Trastor- nos del estado de ánimo y de ansiedad. Aspectos neurobiológicos, clínicos y terapéuticos. 1ra ed. Ciudad Autónoma de Buenos Aires: Sociedad Ibe- roamericana de Información Científica, SIIC, 2016: 563-592.
• Bale, T. L.; Picetti, R.; Contarino, A.; Koob, G. F.; Vale, W. W. & Lee, K.-F. Mice deficient for both corticotropin-releasing factor receptor 1 (CRFR1) and CRFR2 have an impaired stress response and display sexually dichotomous anxiety-like behavior. The Journal of neuroscience: the official journal of the Society for Neuroscience. 2002; 22(1): 193-9.
• Bale T.L. & Vale, W. W. (2004). CRF and CRF receptors: role in stress responsivity and other beha- viors. Annual review of pharmacology and toxicology 2004; 44: 525-57.
• Bale T. L. & Baram, T.Z.; Brown, A. S. et al. Early life programming and neurodevelopmental disor- ders. Biol Psychiatry 2010; 68: 314-9.
• Bateson, P. Is Imprinting Such a Special Case? Philosophical Transactions: Biological Sciences. 1990; 329(1253), 125-131.
• Baxter, L. B.; Schwartz, J. M.; Bergman, K. S. et al. Caudate glucose metabolic rate changes with both drug and behavior therapy for obsessive-compulsive disorder. Arch Gen Psychiatry 1992; 49: 681-9.
• Bowlby, J. Ed. Attachment and Loss, (Volume 1) Attachment. London:Hogarth. 1969.
• Bowlby, J. The making and breaking of affectional bonds.London: Tavistock;1979.
• Bowlby, J. Los Cuidados Maternos y la Salud Mental. Organización Mundial de la Salud, serie de Monografías No. 2. Oficina Sanitaria Panamerica- na, Publicaciones Científicas. No. 14. Washington. 1954.
• Branchi, I.; Andrea, D.; Sietzema, I. Early social enrichment augments adult hippocampal BDNF levels and survival of BdrU-positive cells while in- creasing anxiety and “depression” 2006; J. Neu- rocscience.Res. 83: 965-973.
• Bremner, J. D. Long-term effects of childhood abuse on brain and neurobiology. Child Adolesc Psychiatr Clin N Am 2003; 12: 271–292.
• Bucci, S.; Seymour-Hyde, A.; Harris, A. & Be- rry, K. Client and therapist attachment styles and working alliance. Clin Psychol Psychother 2016; 23(2):155–165.
• Calatayud, F.; Coubard, S. & Belzung, C. Emotional reactivity in mice may not be inherited but influen- ced by parents. Physiol Behav 2004; 80:465–474.
• Champagne, F.; Francis, F.; Mar, A. y Meaney, M. J. Variations in maternal care in the rat as a mediating influence for the effects of environment on develop- ment. Physiology and Behavior 2003;79, 359–371.
• DeRubeis, R. J. et al. Cognitive therapy versus medication for depression: treatment outcomes and neural mechanisms. Nature Reviews Neuroscience 2008; 9: 788-796.
• Dimitry, C. H.; Bobryshev, Y. V. and Chekhonin, V.
P. Epigenetic Alterations in DNA and Histone Modi- fications Caused by Depression and Antidepressant Drugs: Lessons from the Rodent Models. Current Pharmaceutical Design 2017; 23: 1-13.
• Darnaudery, S.; Maccari. Epigenetic programming of the stress response in male and female rats by prenatal restraint stress. Science 2008; 571-585.
• Darwin, Ch. Selección natural o Supervivencia de los más aptos. En: El Origen de las Especies por medio de la selección Natural. Ed:13a. México. Ed Diana.; 1979: 89-137.
• Dell’Osso, B.; D’Addario, C.; Carlotta Palazzo, M.; Benatti, B.; Camuri, G.; Galimberti, D.; Fenoglio, C.; Scarpini, E.; Di Francesco, A.; Maccarrone, M. et al. Epigenetic modulation of BDNF gene: Differences in DNA methylation between unipolar and bipolar patients.J. Affect. Disord 2014; 166:330–333.
• Devaskar, S. U.; Raychaudhuri, S. Epigenetics-A science of heritable biological adaptation. Pediatric Research 2007; 61(Pt 2):1R-4R.
• Duman, R. S. Molecular and celular pathogenesis of depression and mechanism for treatment respon- se. In: Charney DS, Sklar P,Buxbaum JD, Nestler EJ. Neurobiology of mental illness. 4ta ed. New York: Oxford University Press; 2013: pp. 425-437.
• Elliott, E.; Ezra-Nevo, G.; Regev, L.; Neufeld-Co- hen, A.; Chen, A. Resilience to social stress coincides with functional DNA methylation of the Crf gene in adult mice. Nature Neuroscience 2010; 13: 1351-3.
• Feil, R. Environmental and nutritional effects on the epigenetic regulation of genes. Mutat Research 2006; 600(1-2):46-57.
• Francis, D.; Diorio, J.; Liu, D.; Meaney, M. J. Nongenomic transmission across generations of maternal behavior and stress responses in the rats. Science 1999; 286:1155-8.
• García, R.; Ayala, P. A.; Perdomo, S.P. Epigené- tica: definición, bases moleculares e implicaciones en la salud y en la evolución humana. Rev. Cienc. Salud. 2012; 10 (1):59-71.
• Grandin, T.; Mark, J.; Deesing, M. J. Genética de comportamiento animal, en: Temple Grandin (Ed.), Genetics and the Behavior of Domestic Animals. Primera Edición. San Diego, California: Academic Press, Departamento de Ciencia Animal, Colorado State University; 1998.
• Graves, F. C.; Wallen, K. & Maestripieri, D. (2002). Opioids and attachment in rhesus macaque (Macaca mulatta) abusive mothers. Behavioral Neu- roscience 2002; 116(3):489-493.
• Godfrey, K. M.; Lillycrop, K. A.; Burdge, G. C.; Gluckman, P. D.; Hanson M. A. Epigenetic mecha- nisms and the mismatch concept of the develop-
mental origins of health and disease. Pediatr Re- search 2007; 61(5 Pt 2):5R-10R.
• Gordon, I.; Zagoory-Sharon, O.; Leckman, J. F. & Feldman, R. Oxytocin and the Development of Parenting in Humans. Biological psychiatry 2010; 68(4):377-382.
• Gould, T.; Dao, D.; Kovacsics, C. (2009). The open field test. Mood and Anxiety Related Pheno- types in Mice. Neuromethods, 42 (12), 1-20.
• Handel, A. E.; Ramagopalan, S. V. Is Lamarckian evolution relevant to medicine? BMC medical gene- tics. 2010; 11(1):73.
• Heijmans, B. T.; Tobi, E. W.; Stein, A. D.; Put- ter, H.; Blauw, G. J.; Susser, E. S. et al. Persistent epigenetic differences associated with prenatal ex- posure to famine in humans. Proc. Natl. Acad. Sci. 2008; 105 (44):17046-9.
• Heim, C. & Nemeroff, C. B. The role of childhood trauma in the neurobiology of mood and anxiety di- sorders: preclinical and clinical studies. Biol Psy- chiatry 2001; 49, 1023:1039.
• Hennessy, M. B.; Young, T. L.; O’Leary, S. K. & Maken, D. S. Social preferences of developing gui- nea pigs (Cavia porcellus) from the preweaning to the periadolescent periods. J Comp Psychol 2003; 117:406–413.
• Hofer, M. & Sullivan, R. M. Toward a Neurobiology of Attachment. En: Nelson, Ch. A. y Luciana, M. (Eds). Handbook of Developmental Cognitive Neu- roscience. Massachusetts: MIT Press. 2001.
• Hollis, F.; Wang, H.; Dietz, D.; Gunjan, A.; Ka- bbaj, M. The effects ofrepeated social defeat on long-term depressive-like behavior and short-term histone modifications in the hippocampus in male Sprague-Dawley rats. Psychopharmacology (Berl) 2010; 211(1): 69-77.
• Hollis, F.; Duclot, F.; Gunjan, A.; Kabbaj, M. In- dividual differences in the effect of social defeat on anhedonia and histone acetylation in the rat hippo- campus. Hormones and Behavior J 2011; 59(3): 331-7.
• Houston, I.; Peter, C. J.; Mitchell, A.; Straubhaar, J.; Rogaev, E.; Akbarian, S. Epigenetics in the human bra- in. Neuropsychopharmacology 2013; 38(1): 183-97.
• Jaenisch, R.; Bird, A. Epigenetic regulation of gene expression: how the genome integrates intrin- sic and environmental signals. Nat Genet. 2003; 33(Suppl):245-54.
• Jian, F.; Shaun, F.; Guoping, F. Epigenetic Re- gulation of Neural Gene Expression and Neuronal Function. Pediatr Res 2007; 61: 58R–63R.
• Jirtle, R. L.; Skinner, M. K. Environmental epige- nomics and disease susceptibility. Nat Rev Genet; 2007; 8(4):253-62.
• Lee, R. S.; Pirooznia, M.; Guintivano, J.; Ly, M.; Ewald, E. R.; Tamashiro, K. L.; Gould T. D.; Moran,
T. H.; Potash, J. B. Search for common targets of lithium and valproic acid identifies novel epigenetic effects of lithium on the rat leptin receptor gene. Translational Psychiatry 2015;5:e600.
• Lockwood, L. E.; Su, S.; Youssef, N. A. The role of epigenetics in depression and suicide: A platform for gene-environment interactions. Psychiatry Re- search 2015; 228(3):235–242.
• Kaminker, P. Epigenética, ciencia de la adapta- ción biológica heredable Archivos argent de pediatr. 2007; 105(6):529-531.
• Kandel, E. R.; Schwartz, J. H.; Jessell, T. M. Principles of Neural Science. 3rd ed. East Norwalk, Connecticut: Appleton & Lange;1991.
• Kendler, K. & Greenspan, R. J. The Nature of Ge- netic Influences on Behavior: Lessons From “Sim-
pler” Organisms. American Journal Of Psychiatry, 2006; 163(10):1683-1694.
• Lamarck, J. B. Filosofía Zoológica. Ediciones mal- doror. Volumen 10, Barcelona, Mateu, 1971.
• Landers, M. S. & Sullivan, R. M. The development and neurobiology of infant attachment and fear. Dev Neurosci2012; 34:101–114.
• Lassi, G.; Tucci, V. Gene-environment interaction influences attachment-like style in mice. Genes Brain and Behaviour. John Wiley & Sons Ltd and In- ternational Behavioural and Neural Genetics Society 2017; Vol16(6): 612-618.
• Levine, A.; Worrell, T. R.; Zimnisky. R.; Sch- mauss, C. Early life stresstriggers sustained changes in histone deacetylase expression and histone H4 modifications that alter responsiveness to adoles- cent antidepressant treatment. Neurobiology Disea- se Journal 2012; 45: 488-98.
• Lockwood, L. E. and Youssef, N. A. Systematic Re- view of Epigenetic Effects of Pharmacological Agents for Bipolar. Brain Sciences. 2017; 7(11): 154.
• Lyons-Ruth, K.; Melnick, Sh.; Bronfman, E.; She- rry, S. y Llanas, L. Hostile- Helpless relational mo- dels and Disorganized Attachment patterns between parents and their young children: review of research and implications for clinical work. En: Atkinson, L. y Goldberg, S. Attachment issues in Psychopatholo- gy and Intervention. New Jersey: Lawrence Erlbaum Associates; 2004: 65-94.
• Lorenz, K. Why waterfowl? International Zoo Year- book, 1973;13(1): 1-6.
• Marantz Henig, R. The Monk in the Garden: The Lost and Found Genius of Gregor Mendel, the Father of Ge- netics. New York, Houghton Mifflin Harcourt, 2001.
• McCrory, E.; De Brito, S. A.; Viding, E. The link between child abuseand psychopathology: a review of neurobiological and genetic research. Journal of the Royal Society of Medicine 2012; 105: 151-6.
• McEwen, B. Understanding the potency of stress- ful early life experiences on brain and body func- tion. Science 2008; S11:S15.
• McGowan, P. O.; Sasaki, A.; Alessio, A. C. D.; Dymov, S.; Szyf, M.; Turecki, G. et al. Epigenetic regulation of the glucocorticoid receptor in human brain associates with childhood abuse. Nature neu- roscience 2009; 12(3): 342-348.
• Medina, J. H.; Alvano, S. A. Factores involucrados en la etiopatogenia de los trastornos de ansiedad y del estado del ánimo. En: Alvano, S. A. et al. Tras- tornos del estado de ánimo y de ansiedad. Aspectos neurobiológicos, clínicos y terapéuticos.1ra ed. Ciu- dad Autónoma de Buenos Aires: Sociedad Iberoame- ricana de Información Científica, SIIC, 2016: 65-76.
• Melka, M. G.; Castellani, C. A.; Laufer, B. I.; Rajakumar, R. N.; O’Reilly, R.; Singh, S. M. Olan- zapine induced DNA methylation changes support the dopamine hypothesis of psychosis. J. Molecular Psychiatry 2013; 1(1):19.
• Melka, M. G.; Laufer, B. I.; McDonald, P.; Caste- llani, C. A.; Rajakumar, N.; O’Reilly, R.; Singh S.
M. The effects of olanzapine on genome-wide DNA methylation in the hippocampus and cerebellum. Clin. Epigenetics. 2014; 6 (1):1.
• Morgan, D. K.; Whitelaw, E. The case for trans- generational epigenetic inheritance in humans. J of the Int Mamm. Genome Society 2008;19 (6):394-7.
• Moriceau, S. & Sullivan, R. Neurobiology of Infant Attachment. Developmental Psychobiology, 2005; 47(3):230-242.
• Moriceau, S.; Raineki, C.; Holman, J. D.; Holman,
J. G. & Sullivan, R. M. (2009). Enduring neurobe- havioral effects of early life trauma mediated throu-
gh learning and corticosterone suppression. Fron- tiers in behavioral neuroscience 2009; Sept 1;3:22.
• Nakazawa, K.; Zsiros, V.; Jiang, Z.; Nakao, K.; Kolata, S.; Zhang, S. et al. GABAergic interneuron origin of schizophrenia pathophysiology. Journal Neuropharmacology 2012; Vol 62(3):1574-1583.
• Neslter, E. J.; Terwiliger, R. Z.; Duman, R. S. Chronic antidepressant administration alters the subcellular distribution of cAPM-dependent pro- tein kinase in rat frontal cortex. J Neurochem 1989;53:1644-1647.
• Nyberg, F.; Linstrom, L. H. y Terenius, L. Reduced
-casein levels in milk samples from patients with postpartum psychosis. Biol. Psychiat. 1988; Vol 23: 115-122.
• Oiberman, A. Vínculo y apego. En: Nakab A, Cas- trillon S, Martinitto R, Orazi V. eds. Programa Na- cional de Actualización Pediátrica (PRONAP). Bs As. Publicación de la Sociedad Argentina de Pedia- tría. 2011: 34-52.
• Olds, J. Centros del placer en el cerebro. En: Psic contemporánea. Selecciones del Scientifican Ame- rican. Nd ed. Madrid: Ed. Blume; 1975: 28-34
• Panksepp, J. Affective Neuroscience. Nd ed. Oxford: Oxford University Press. 1998.
• Panksepp, J. Emotional endophenotypes in evolutionary psychiatry. Progress in neuro-psy- chopharmacology & biological psychiatry; 2006; 30(5):774-84.
• Perry, R. & Sullivan, R. M. (2014) Neurobiology of attachment to an abusive caregiver: short-term benefits and long-term costs. Dev Psychobiol 2014; 56:1626–1634.
• Plagge, A.; Gordon, E.; Dean, W.; Boiani, R.; Cinti, S.; Peters, J. & Kelsey, G. The imprinted signaling protein XL alpha s is required for postnatal adap- tation to feeding. Nat Genet 2004; 36:818–826.
• Pringle, A.; Browning, M.; Cowen, P. J.; Harmer,
C. J. A cognitive neuropsychological model of an- tidepressant drug action. Progress in Neuropsy- chopharmacology & Biological Psychiatry 2011; 35: 1586-1592.
• Reik, W.; Constancia, M.; Fowden, A.; Anderson, N.; Dean, W.; Ferguson-Smith, A.; Tycko, B. & Si- bley, C. Regulation of supply and demand for ma- ternal nutrients in mammals by imprinted genes. J Physiol 2003; 547: 35–44.
• Riddihough, G.; Zahn, L. M. Epigenetics. What is epigenetics? Introduction. Science 2010; vol 330:6004.pp611.
• Roiser, J. P.; Elliot, R.; Sahakian, B. J. Cognitive mechanisms of treatment in depression. Neuropsy- chopharmacology 2012; 37: 117-136.
• Roth, T.L. & Sweatt, J.D. Annual research review: epigenetic mechanisms and environmental shaping of the brain during sensitive periods of development. J Child Psychol Psychiatry 2011; 52:398–408.
• Salas, N.; Iturbe U. Evolución: la síntesis inaca- bada. Revista de la Sociedad Española de Biología Evolutiva. eVOLUCIÓN 2011; 6(2): 21-28.
• Sequeira-Cordero, A.; Masís-Calvo, M.; Mora-Ga- llegos, A.; y Fornaguera-Trías, J. Maternal behavior as an early modulator of neurobehavioral offspring responses by Sprague-Dawley rats. Behavioral Brain Research 2013; 237: 63-70.
• Shair, H.; Brake, S.; Hofer, M. & Myers, M. Blood pressure responses to milk ejection in the young rat. Physiology & behavior, 1986;37(1):171-6.
• Sheinbaum, T.; Kwapil, T. R.; Ballespi, S.; Mit- javila, M.; Chun, C. A.; Silvia, P. J. & Barrantes-Vi- dal, N. Attachment style predicts affect, cognitive appraisals, and social functioning in daily life. Front
Psychol 2015; 6:296.
• Slattery, D. A. & Cryan, J. F. (2012). Using the rat forced swimtest toassessantidepressant-like activity in rodents. Nature Protocols 2012; 7(6), 1009-1014.
• Spitz, R. A. Hospitalism: an inquiry into the genesis of psychiatric conditions in early childhood [I]. En: The psychoanalytic study of the child, 1945; Vol 1, 53-74.
• Spitz, R. A. El primer año de vida del niño. 5ta reimpresión, 1ra edición en Argentina. Bs As: Fondo de cultura económica;1979: 197-210.
• Sullivan, R. M.; Landers, M.; Yeaman, B. & Wil- son, D. A. Good memories of bad events in infancy. Nature 2000; 407: 38–39.
• Sullivan, R. M. The neurobiology of attachment to nurturing and abusive caregivers. Hastings Law J 2012; 63:1553–1570.
• Surget. A.; Saxe, M.; Leman, S.; Ibarguen-Vargas, Y.; Chalon, S.; Griebel, G. et al. Drug-dependent re- quirement of hippocampal neurogenesisin a model of depression and of antidepressant reversal. Biolo- gical Psychiatry 2008; 64(4): 293-301.
• Tarantino, L. M.; Sullivan, P.F. & Meltzer-Brody,
S. Using animal models to disentangle the role of genetic, epigenetic, and environmental influences on behavioral outcomes associated with maternal anxie- ty and depression. Front Psychiatry 2011; 2: 44.
• Tsankova, N.; Renthal, W.; Kumar, A.; Nestler, E. J. Epigenetic regulation in psychiatric disorders. Nature Reviews Neuroscience 2007; 8 (5): 355-367.
• Wang, J. W.; Dranosky, A.; Hen, R. The when and where of BDNF and the antidepressant response. Biol Psychiatry 2008: 64: 293-301.
• Waters, E.; Weinfield, N. S. & Hamilton, C. E. The stability of attachment security from infancy to ado- lescence and early adulthood: general discussion. Child Development 2000; 71(3): 703–706.
• Weaver, I. C.; Meaney, M. J.; & Szyf, M. Maternal care effects on the hippocampal transcriptome and anxiety-mediated behaviors in the offspring that are reversible in adulthood. Proceedings of the National Academy of Sciences of the United States of Ameri- ca. 2006; 103(9): 3480-5.
• Weaver, I. C.; Cervoni, N.; Champagne, F. A.; D’Alessio, A. C.; Sharma, S.; Seckl, J. R. et al. Epi- genetic programming by maternal behavior.Nature Neuroscience 2004;7:847–54.
• Wilkinson, L. S.; Davies, W. & Isles, A. R. Ge- nomic imprinting effects on brain development and function. Nature Rev Neurosci 2007; 8: 832–843.
• Willner, P.; Scheel-Krüger, J.; Belzung, C. The neurobiology of depression and antidepressant ac- tion. Neurosci BiobehavRev 2013; 37:2331-71.
• Wood, S. K.; Valentino, R. J. The brain norepi- nephrine system, stress and cardiovascular vul- nerability. Neuroscience & Biobehavioral Review 2017;74(Pt B): 393-400.
• Young, K.; Liu, Y. & Wang, Z. The neurobiology of social attachment: A comparative approach to behavioral, neuroanatomical, and neurochemichal studies. Comparative Biochemistry and Physiology 2008;148(4):401-410.
• Zhang, T.-Y.;& Meaney, M. J. Epigenetics and the environmental regulation of the genome and its function. Annual review of psychology; 2010; 61:439-66.
• Zieher, L. M.; Guelman, L. R. La epigénesis cro- matínica y su relevancia en las conductas complejas y en las patologías psiquiátricas. Psicofarmacología SCIENS, 2006; 6:37.






