NAC-antioxidante-neuroinflamacion-glutamato-psiquiatria-depresion-esquizofrenia-TOC-adicciones-cognicion-tratamiento
NAC – antioxidante – neuroinflamacion – glutamato-psiquiatria – depresion – esquizofrenia – TOC – adicciones -cognicion – tratamiento
Resumen
La N-acetilcisteína (NAC) es un derivado acetilado del aminoácido L-cisteínacon propiedades antioxidantes, antiinflamatorias y moduladoras del sistemaglutamatérgico. En los últimos años, ha emergido como un agentepsicofarmacológico complementario con potencial terapéutico en diversostrastornos neuropsiquiátricos. Este trabajo revisa críticamente la evidenciaexperimental y clínica disponible, analizando los principales mecanismos neurobiológicos implicados —restauración del equilibrio redox, modulación glutamatérgica y regulación de la neuroinflamación— y su correlato con la fisiopatología de enfermedades como la esquizofrenia (EZQ), la depresiónmayor, el trastorno obsesivo-compulsivo (TOC) y las adicciones. Se destacan loshallazgos que vinculan la disfunción del glutatión, el sistema sistema cistina-glutamato (x(c-)) y la activación microglial con alteraciones sinápticas y cognitivas. Los estudios clínicos recientes muestran efectos beneficiosos de la NAC como tratamiento adyuvante en síntomas negativos, disfunción cognitiva ycontrol de impulsos. En conjunto, la NAC representa una estrategia terapéutica segura, accesible y de base neurobiológica sólida, que justifica su incorporación a la investigación traslacional en psiquiatría. Palabra clave
N-acetilcisteína; glutatión; estrés oxidativo; glutamato; neuroinflamación;esquizofrenia; trastornos afectivos; psicofarmacología traslacional.
Objetivo del estudio
Este trabajo tiene como objetivo revisar críticamente la evidencia científicasobre la utilización de la N-acetilcisteína (NAC) en los trastornosneuropsiquiátricos, con especial énfasis en sus mecanismos de acción en elsistema nervioso central (SNC) y la validez clínica de los estudios publicados durante los últimos diez años (2023–2013).
De manera específica, se propone:
Analizar los fundamentos biológicos que sustentan el uso de la NAC comomodulador del equilibrio redox, del sistema glutama- térgico y de laneuroinflamación, tres ejes clave en la fisiopatología de los trastornos mentales.
Sintetizar y comparar la evidencia clínica proveniente de ensayos controladosaleatorizados, revisiones sistemáticas y meta- análisis que evalúan la eficacia yseguridad de la NAC en esquizofrenia, trastornos afectivos, trastorno obsesivo-compulsivo, adicciones y otros cuadros del espectro neuropsiquiátrico.
Vincular los hallazgos clínicos con los mecanismos neurobiológicossubyacentes, para ofrecer una perspectiva traslacional que oriente futuras líneas de investigación y nuevas aplicaciones terapéuticas en psicofarmacología.
Psicofarmacología26:139, febrero de2026
1.1. Antecedentes históricos de la n-acetilcisteína en medicina
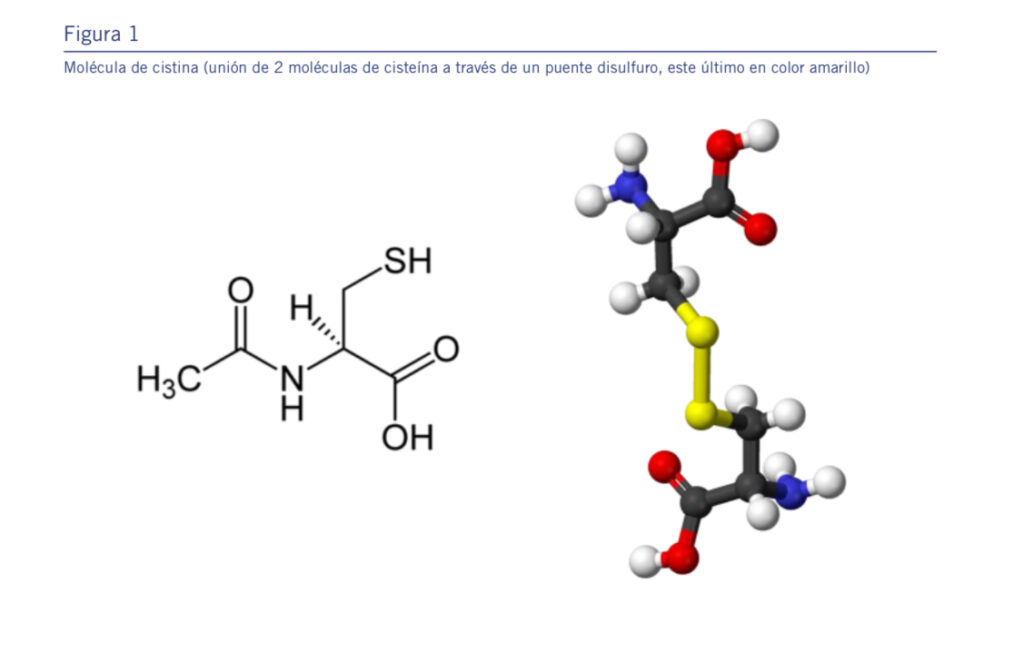
La NAC es un derivado acetilado del aminoácido L-cisteína, introducido en la práctica médica a mediados del siglo XX como agente mucolítico por su capacidad para romper los puentes disulfuro de las glicoproteínas del moco bronquial. Este efecto facilitó su empleo inicial en enfermedades respi- ratorias crónicas, como labronquitis crónica y la enfermedad pulmonar obstructiva crónica (EPOC), dondemejoraba la de- puración mucociliar y la función respiratoria. (VER FIG 1)
Posteriormente, en la década de 1970, la NAC adquirió un papel crucial comoantídoto frente a la intoxicación por paracetamol (acetaminofén), al reponer los niveles hepáticos de glutatión, el principal antioxidante endógeno. Esta indicación consolidó su posición como fármaco esencial en emergencias médicas,demostrando su seguridad incluso en dosis altas por vía oral o intravenosa.
Durante las décadas siguientes, la comprensión del papel del estrés oxidativo, laneuroinflamación y la disfunción del meta- bolismo del glutatión en diversasenfermedades crónicas —incluidas las neurodegenerativas y psiquiátricas—impulsó la investigación del potencial neuroprotector de la NAC. A partir de losaños 2000, múltiples estudios preclínicos demostraron que la NAC no solo actuaba como antioxidante directo, sino que también modulaba la neurotransmisión glutamatérgica a través del transportador cistina-glutamato (sistema x_c-), implicado en la regulación del tono excitatorio en regiones cerebrales crí- ticascomo el núcleo accumbens (NAcc), la corteza prefrontal (CPF) y el hipocampo. Lacistina es un aminoácido azufrado,una forma más estable y dimerizada de la cisteína, donde dos moléculas de éstas se unen por un puente disulfuro.
Estos hallazgos sentaron las bases para su investigación en el campo de la neuropsiquiatría, abriendo nuevas líneas de estudio en EZQ, trastornos del ánimo, TOC y adicciones. Los primeros ensayos clínicos controlados se desarrollaron entre 2008 y 2012, mostrando resultados alentadores como terapia adyuvante en síntomas negativos de EZQ y en la reducción del craving en dependencia de sustancias.
En los últimos diez años, la evidencia se ha expandido de manera considerable.La revisión sistemática de Bradlow et al.
(1) sintetizó más de una década de investigación clínica, posicionando a laNAC como uno de los agentes más prometedores en la intersección entreneurobiología, inflamación y psiquiatría. Según esta revisión, el interéscreciente en la NAC refleja un cambio conceptual hacia intervenciones farmacológicas que restauran la homeostasis redox y glutamatérgica, más quelimitarse a la modulación monoaminérgica clásica (1,2).
1.2. Justificación de su uso en neuropsiquiatría y sistema nervioso central (snc)
El creciente interés por la NAC en el campo de la neuropsiquiatría se sustentaen la evidencia de que numerosos trastornos mentales comparten mecanismosfisiopatológicos convergentes, vinculados al estrés oxidativo, laneuroinflamación y la disregulación del sistema glutamatérgico.
Estas alteraciones confluyen en un eje patobiológico común, caracterizado por el desequilibrio redox–neurotransmisor, que conlleva disfunción sináptica,alteraciones en la plasticidad
neuronal y daño celular progresivo en el SNC.
1.2.1. Mecanismos neurobiológicos implicados
La NAC actúa como precursor de cisteína y glutatión (GSH), el principal antioxidante intracelular, cuyo déficit ha sido documentado, como ya se dijo, enmúltiples trastornos psiquiátricos. Al restaurar los niveles de GSH, la NACreduce el daño oxidativo y mejora la integridad mitocondrial, promoviendo un ambiente neuroquímico más estable a través del aumento de la activación tónica de los receptores presinápticos mGluR2/3. En definitiva, se trata de un pro fármaco. El aminoácido cis- teína presenta limitada biodisponibilidad einsolubilidad, ade- más de no atravesar fácilmente la BHE. (3)
Además, la NAC modula el sistema glutamatérgico a través del transportadorcistina-glutamato (sistema x_c-), que regula la liberación extracelular deglutamato en el NAcc y la CPF
—regiones involucradas en la motivación, la recompensa y el control cognitivo—. Esta regulación indirecta contribuye a normalizar la hiperexcitabilidad glutamatérgica, una característica patológica común en la EZQ, el TOC y lostrastornos por consumo de sustancias (2,4,5).
A nivel inflamatorio, la NAC inhibe la activación microglial y la liberación de citoquinas proinflamatorias (como TNF-Þ, IL-6 e IL-1ß), reduciendo el “ruidoneuroinmune” asociado con la alteración de la conectividad funcional cortical y subcortical. Este efecto antiinflamatorio, junto con su acción antioxidante, restaura la homeostasis redox y mejora la señalización neuro- nal, favoreciendo la plasticidad y la neurogénesis. (1)
1.2.2. Convergencia fisiopatológica en los trastor- nos psiquiátricos
Diversos estudios y revisiones recientes han destacado que las vías oxidativas,inflamatorias y glutamatérgicas convergen en múltiples patologías mentales. En EZQ por ejemplo, se han documentado niveles reducidos de GSH en CPF ytálamo, correlacionados con síntomas negativos y deterioro cognitivo. En depresión y TB, la alteración redox se asocia con anhedonia, disfunción mitocondrial y aumento del estrés celular. En las adicciones, la disfunción delsistema x_c- y el exceso de glutamato extracelular en el NAcc favorecen loscircuitos de craving y recaída. (4,6)
Así, la NAC representa una intervención multimodal que aborda simultáneamentetres ejes biológicos disfuncionales —oxida- tivo, inflamatorio y glutamatérgico—, ofreciendo una ventaja teórica sobre los psicofármacos tradicionales centrados en neu- rotransmisores monoaminérgicos, sobre todo como adyuvante (serotonina-5HT-, dopamina –DA-, noradrenalina -NA) (1,7).
1.2.3. Relevancia clínica y traslacional
El interés clínico por la NAC reside en su perfil de seguridad favorable, su disponibilidad oral y costo accesible, y su capacidad de penetrar la BHE. Los resultados de los ensayos clínicos revisados por Bradlow y colaboradores (1)demuestran beneficios potenciales como terapia adyuvante en síntomas negativosde EZQ, depresión resistente, TOC y adicciones, con efectos significativos en dominios específicos como función cognitiva y control de impulsos.
En conjunto, estos hallazgos justifican la creciente exploración de la NAC como estrategia psicofarmacológica complementaria orientada a la neuroprotección, la modulación glutamatérgica y la restauración del equilibrio redox cerebral, posicionándola en la frontera entre la farmacología tradicional y la neurobiología traslacional.
2. BASES BIOLÓGICAS DE LA ACCIÓN DE LA N-ACE- TILCISTEÍNA EN EL SISTEMA NERVIOSO
Introducción
La comprensión moderna de los trastornos neuropsiquiátricos ha trascendido elparadigma monoaminérgico clásico, reconociendo que procesos celulares comoel estrés oxidativo, la neuroinflamación y la disregulación glutamatérgica desempeñan un papel central en la génesis y perpetuación de los síntomas. Dentro de este marco, la NAC ha adquirido relevancia como un agente con propiedadesneuroprotectoras, antioxidantes y moduladoras del sistema de neurotransmisión, loque la posiciona como una de las moléculas más investigadas en la intersecciónentre neurobiología molecular y psicofarmacología contemporánea. (1)
El sistema nervioso es especialmente vulnerable al desequi- librio redox, debido a su alta demanda metabólica, su abundancia de lípidos poliinsaturados y su limitada capacidad antioxidante intrínseca. Bajo estas condiciones, el exceso de especies reactivas de oxígeno (ROS) y nitrógeno (RNS) puede inducir dañooxidativo a proteínas, lípidos y ADN, contribuyen- do al deterioro sináptico y a ladisfunción neuronal observada en diversos trastornos psiquiátricos.
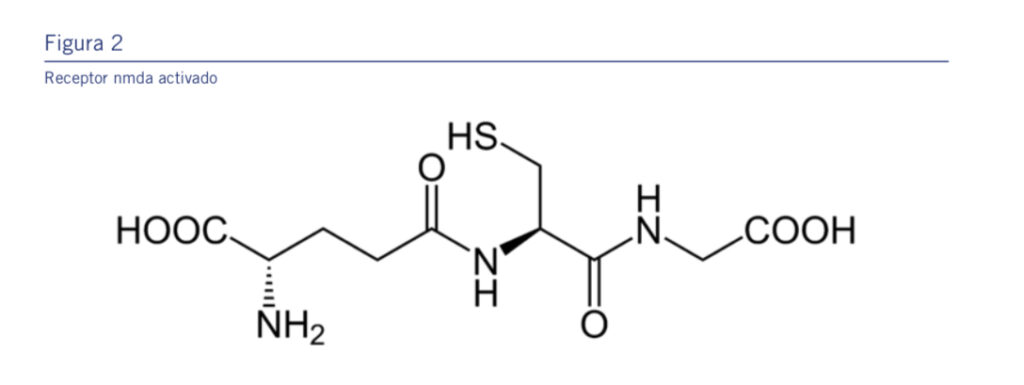
La NAC actúa sobre este eje patogénico restaurando la ho- meostasis celular mediante varios mecanismos complemen- tarios: reposición del glutatión reducido(GSH) (Ver figura 2), captura directa de radicales libres, modulación del sistema
cistina-glutamato (x(c-)) y reducción de la respuesta inflama-
toria microglial. Esta acción multifacética le confiere un perfil singular comoagente redox-neurotrófico, con potencial tera- péutico transversal en enfermedades del SNC caracterizadas por estrés oxidativo e inflamación crónica de bajo grado(2).
A continuación, se describen los principales mecanismos bio- lógicos por los cuales la NAC ejerce su acción en el SNC, comenzando por su función antioxidante fundamental.
2.1. Mecanismos antioxidantes: glutatión y espe- cies reactivas de oxígeno
El mecanismo antioxidante constituye el núcleo de la acción biológica de la NAC.Este se basa en su papel como precursor directo del GSH, un tripéptido formadopor cisteína, glutamato y glicina (Ver Fig 2), que representa el antioxidanteintracelular más importante del cerebro. El GSH participa activamen- te en laneutralización de radicales libres y en la regeneración de otros antioxidantes endógenos como las vitaminas C y E.
2.1.1. Síntesis de glutatión y rol de la NAC
El aumento de ROS —como el anión superóxido, el peróxido de hidrógeno y el radical hidroxilo— es un evento común en la fisiopatología del estrés oxidativocerebral. La NAC neutraliza
directamente estas moléculas reactivas mediante su grupo tiol, pero ademáspotencia las enzimas antioxidantes glutatión peroxidasa (GPx) y glutatión reductasa(GR), reforzando el sis- tema endógeno de defensa.
Estudios preclínicos han demostrado que la administración de NAC reduce la peroxidación lipídica y la nitración proteica, dos procesos vinculados con la degeneración neuronal y la disfunción sináptica. (1)
2.1.3. Implicancias neuropsiquiátricas
La disfunción del metabolismo del GSH se ha asociado con múltiples cuadros psiquiátricos. En la EZQ, niveles bajos de GSH se correlacionan con mayorseveridad de síntomas nega- tivos y deterioro cognitivo. En la depresión mayor, elestrés oxi- dativo se relaciona con la reducción del volumen hipocampal y alteraciones mitocondriales. En modelos animales de adic- ción, la NAC previene eldaño oxidativo inducido por drogas y normaliza la plasticidad sináptica del NAcc.
Estos hallazgos sugieren que la acción antioxidante de la NAC no solo tiene unefecto citoprotector, sino también neuromodulador, al restaurar las condiciones bioquímicas necesarias para una neurotransmisión equilibrada y una adecuadaplasticidad neuronal (4).
2.2. Modulación glutamatérgica (sistema x(c-), NMDA y regulación sináptica)
El glutamato es el principal neurotransmisor excitador del SNC y desempeña unpapel esencial en la plasticidad sinápti- ca, la memoria y la cognición. Sin embargo,su desregulación puede conducir a neurotoxicidad excitatoria y alteraciones del equilibrio excitatorio-inhibitorio, fenómenos implicados en la fisiopatología demúltiples trastornos psiquiátricos, entre ellos la EZQ, el TOC, las adicciones y los trastornos del ánimo.
En este contexto, la NAC se ha destacado como un modu- lador indirecto de la neurotransmisión glutamatérgica, capaz de restaurar la homeostasis excitatoriamediante mecanismos dependientes del sistema cistina-glutamato (x(c-)) y la modulación del receptor NMDA.
2.2.1. El sistema cistina-glutamato (x(c-)) como diana terapéutica
El sistema x(c-) es un antiportador de membrana presente prin- cipalmente en los astrocitos, que intercambia una molécula de cistina extracelular por una deglutamato intracelular. Este proceso no requiere energía y mantiene unaconcentración basal de glutamato en el espacio extracelular, necesaria para la regulación tónica de los receptores metabotrópicos del glutamato tipo 2/3 (mGluR2/3).
La NAC, al incrementar la disponibilidad de cistina, estimula la actividad delsistema x(c-), promoviendo la liberación controlada de glutamato desde losastrocitos. Este aumento moderado del glutamato extracelular activa los receptores mGluR2/3 presinápticos, loscuales ejercen un efecto inhibitorio sobre la liberación excesiva de glutamato sináptico.
El resultado es una normalización del tono glutamatérgico, que atenúa laexcitotoxicidad y favorece el equilibrio funcional entre la neurotransmisión excitatoria y la inhibitoria (2).
Este mecanismo es particularmente relevante en regiones cerebrales como elNAcc y la CPF medial, estructuras implicadas en la motivación, el control deimpulsos y la regulación afectiva. En modelos animales, la administracióncrónica de NAC restaura la función del sistema x(c-) en el NAcc, normalizando las alteraciones del circuito cortico-estriado observadas tras exposición a drogas de abuso o estrés crónico (4).
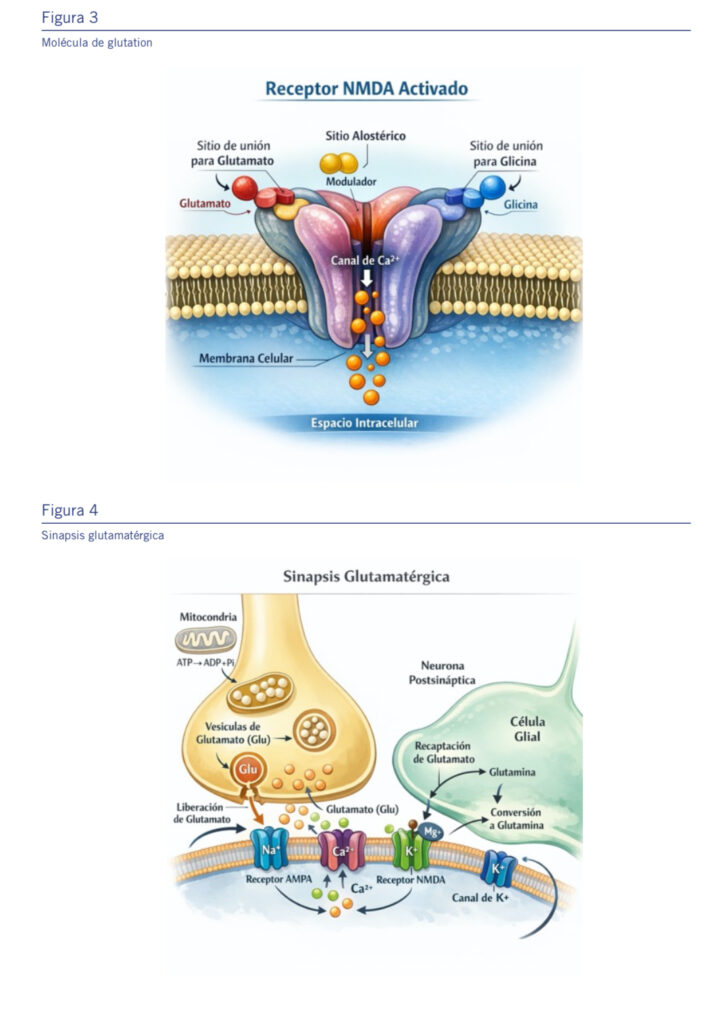
2.2.2. Modulación de los receptores NMDA y glu- tamato sináptico
Además de su acción sobre el sistema x(c-), la NAC influye in- directamentesobre la función de los receptores NMDA (N-me- til-D-aspartato) (Ver fig 3 y 4), críticos para la plasticidad sináptica y la cognición.
El receptor NMDA depende de la disponibilidad de glutatión y cisteína paramantener su función redox normal. En estados de estrés oxidativo, la oxidaciónde los sitios tiol del receptor reduce su sensibilidad al glutamato y contribuye auna hipofunción NMDA, fenómeno implicado en la fisiopatología de la EZQ.
La NAC, al restaurar el equilibrio redox neuronal, reactiva los sitios tiol delreceptor NMDA, mejorando la neurotransmisión glutamatérgica y la conectividad cortical. Esta normalización funcional podría explicar la mejoría en síntomas negativos y cognitivos observada en ensayos clínicos con pacientes con EZQ tratados con NAC (1,8).
Implicancias clínicas y traslacionales
El papel modulador de la NAC sobre la neurotransmisión glutamatérgica tiene implicancias directas en varios trastornos del SNC:
EZQ: la NAC ha mostrado reducir los síntomas negativos y mejorar la cognición, especialmente tras ≥24 semanas de tratamiento adyuvante, posiblemente porrestaurar la función NMDA y reducir la hiperexcitabilidad cortical (9).
Adicciones: en la dependencia de cocaína y cannabis, la NAC normaliza la disfunción glutamatérgica del NAcc, reduciendo craving y previniendo recaídas (3)(10).
TOC: al disminuir la liberación excesiva de glutamato, la NAC puede reducir la hiperactividad del circuito cortico-estria- do-talámico, mecanismo asociado a compulsiones (11).
En conjunto, la modulación glutamatérgica inducida por la NAC permite unaregulación homeostática de la excitabilidad neuronal, integrando su papelantioxidante con su acción neu- roreguladora. Este doble efecto convierte a la NACen una molécula única entre los agentes psicofarmacológicos, con un perfil orientado a la restauración de la función sináptica y la plasticidad neuronal, más que a la simple supresión sintomática.
2.3. Efectos antiinflamatorios, neuroprotección y microglía
El papel de la neuroinflamación como factor etiopatogénico común en los trastornos psiquiátricos ha sido firmemente establecido durante la última década. La activación crónica de las células gliales, en particular de la microglía, induce la liberación de mediadores proinflamatorios —como factor de necrosis tumoral alfa (TNF-α), interleucina-6 (IL-6) einterleu- cina-1α (IL-1α)—,que alteran la plasticidad sináptica, la neurotransmisión y la neurogénesis.
Este estado proinflamatorio persistente produce un desequilibrio neuroinmune, caracterizado por la disfunción de las conexiones fronto-límbicas y la alteraciónde los sistemas dopaminérgico y glutamatérgico, contribuyendo a síntomas como anhedonia, impulsividad, apatía y deterioro cognitivo.
Dentro de este contexto, la NAC actúa como un agente anti- inflamatorio y neuroprotector que interrumpe múltiples vías proinflamatorias y refuerza lacapacidad antioxidante intracelular, modulando de manera directa la activaciónmicroglial y la señalización intracelular asociada al estrés oxidativo.
2.3.1. Regulación de la activación microglial
La microglía, principal célula inmunitaria residente del SNC, puede adoptar distintos fenotipos funcionales según el contexto neuroinmune.
El fenotipo M1, de perfil proinflamatorio, se caracteriza por la liberación de ROS,óxido nítrico (NO) y citoquinas proinflamatorias, que contribuyen al dañoneuronal y a la disfunción sináptica. En contraste, el fenotipo M2, de tipoantiinflamatorio y reparador, promueve la regeneración neuronal, la fagocitosis dedetritos celulares y la resolución del proceso inflamatorio.
Estudios experimentales han mostrado que la N-acetilcisteína (NAC) reduce lapolarización microglial hacia el fenotipo M1 y favorece la transición al fenotipoM2, lo que disminuye la pro- ducción de mediadores proinflamatorios yaumenta la expre- sión de factores tróficos, como el factor neurotrófico derivado del cerebro (BDNF).
Este cambio fenotípico se asocia con una mayor preservación de las conexiones sinápticas y una reducción de la muerte neuronal en modelos experimentales deestrés crónico y toxicidad dopaminérgica (1).
2.3.2. Inhibición de vías inflamatorias intracelulares
La acción antiinflamatoria de la NAC se extiende a la inhi- bición de vías de señalización intracelular clave, implicadas en la respuesta inmunoneural y eldaño oxidativo. Entre ellas destacan:
• NF-KB (factor nuclear kappa-B): la NAC bloquea su activación al mantenerun estado redox reducido, lo que previene la translocación nuclear del complejop65/p50 y, en consecuencia, inhibe la transcripción de genes proinflamatorios.
• MAPK (mitogen-activated protein kinase) y JNK (c-Jun N-terminal kinase): se ha demostrado que la NAC atenúa la fosforilación excesiva de estas quinasas, reduciendo la respuesta inflamatoria y disminuyendo la apoptosis neuronal.
• NLRP3 (inflamasoma): estudios recientes indican que la NAC inhibe la activación del inflamasoma NLRP3, lo que re- duce la maduración de la interleucina-1β (IL-1β). Este me- canismo podría explicar su efectoneuroprotector en modelos experimentales de neurodegeneración y en psicosis inducida por estrés oxidativo (8).
2.3.3. Neuroprotección frente al daño oxidativo e inflamatorio
El efecto neuroprotector de la NAC se manifiesta en su capa- cidad parapreservar la integridad neuronal y sináptica frente a condiciones de estrés oxidativo, inflamación y excitotoxicidad.
En modelos animales de EZQ inducida por ketamina, la NAC previene lapérdida de interneuronas GABAérgicas corticales y normaliza la expresión deproteínas sinápticas como PSD-95 y synaptophysin, restaurando la conectividad funcional.
Asimismo, en modelos de depresión inducida por lipopolisacárido (LPS), laNAC reduce las concentraciones de IL-6 y TNF-α en hipocampo y CPF, correlacionándose con una mejoría en conductas anhedónicas y cognitivas (2).
En conjunto, estos hallazgos respaldan el rol de la NAC como agenteneuroprotector multimodal, capaz de integrar la modulación antioxidante,antiinflamatoria y sináptica, favoreciendo la resiliencia neuronal frente a lainjuria oxidativa y la disfunción neuroinmune.
2.3.4. Correlación clínica: inflamación y síntomas psiquiátricos
En el ámbito clínico, numerosos estudios han documentado una correlación entremarcadores inflamatorios sistémicos
Psicofarmacología26:139, febrero de2026
elevados (como PCR y cociente neutrófilos/linfocitos) y peor evoluciónsintomática en pacientes con EZQ, depresión o trastorno bipolar (TB).
Un ensayo reciente demostró que el uso adyuvante de NAC durante 4 semanas en pacientes con EZQ redujo significati- vamente el puntaje PANSS-negativo y tendió a disminuir el cociente neutrófilos/linfocitos, indicador indirecto del estado inflamatorio, aunque sin alcanzar significación estadística para este último parámetro (12).
De forma similar, en trastorno depresivo mayor, los estudios controlados muestran que la administración de NAC se asocia con reducción de síntomasresiduales y mejoría funcional, efectos que podrían estar mediados por lamodulación del eje inflamatorio cerebral y sistémico (6), así como también sobre la ideación suicida (13)
La activación microglial y la liberación de citoquinas proinflamatorias se handescrito ampliamente en esquizofrenia y se correlacionan con disfunciónsináptica y de sustancia blanca (14).
Esta convergencia entre disfunción glutamatérgica y estrés oxidativo ha sidodestacada en revisiones recientes sobre NAC y neuroinflamación (15).
2.4 Evidencia clínica cuantitativa y análisis crítico
Los ensayos clínicos sobre NAC en psiquiatría, aunque heterogéneos, muestran una tendencia global hacia efectos be- neficiosos modestos pero consistentes. En esquizofrenia, los metaanálisis reportan mejoras de entre 2 y 4 puntos en la subescala PANSS-negativa, con dosis entre 1200 y 3600 mg/ día durante ≥12semanas. En depresión mayor y bipolaridad, los estudios de Berk et al. (6) y Zheng et al. (7) evidencian reducciones significativas en síntomas residuales y mejora funcional, especialmente en cuadros resistentes.
En el TOC y en las adicciones, los resultados son también alentadores: reducciones en Y-BOCS de aproximadamente 4 puntos, y disminución del craving con mantenimiento del efecto tras la suspensión del fármaco. Los ensayosrecientes en adicciones a opioides y cocaína refuerzan el valor de la NAC como coadyuvante multimodal, actuando sobre estrés oxidativo y disfunciónglutamatérgica.
En conjunto, los efectos de la NAC son modestos en magnitud, peroreproducibles y clínicamente relevantes en dominios de síntomas negativos, control de impulsos y afectividad residual —áreas donde los tratamientosconvencionales ofrecen respuestas limitadas. Su perfil de seguridad, biodisponibili- dad oral y costo bajo la posicionan como un candidato ideal paraestrategias de neuroprotección traslacional. (Ver tabla 1)
2.5. Farmacocinética
Tras la administración de NAC por vía oral la absorción se pro- ducerápidamente, alcanzando concentraciones séricas máxi- mas en 2 a 3 horas.Luego de una dosis de 200 a 400 mg el pico plasmático es de 0,35 a 4 mg/L a los 60-120minutos. Se desacetila y circula en forma libre ligada a las proteínas plasmáticas. La biodisponibilidad es de un 5 %, debido a la n-desacetilación enmucosa intestinal y primer paso hepático.
Su vida media es de aproximadamente 6 h (11 en niños). Ésta aumenta un 80 % en insuficiencia renal grave y en cirrosis. También se observa un incremento en losniveles plasmáticos de cisteína y glutatión, aspecto relacionado con su propio mecanismo de acción. Difunde de forma rápida a los líquidos extracelulares,localizándose principalmente a nivel de la secre- ción bronquial. Su volumen dedistribución es de 0,33 a 0,47 l/Kg. Se degrada principalmente en hígado (70%), riñones y pulmones Su eliminación es renal en un 30 % (clearence de 0,19 a 0,211 L/h) y sus principales metabolitos los aminoá- cidos cistina y cisteína. Un 50 % circula unida a proteínas por uniones disulfuro (lábiles) o enlaces peptídicoscovalentes luego de 4 horas de su administración. Su principal producto de excreción es el sulfato inorgánico (16, 17,18).
La NAC es permeable a la membrana celular, por lo que no requiere sertransportada como la cisteína por el sistema ala- nina-serina-cisteína (ASC), un sistema de transporte de aminoácidos neutros dependiente de Na. Dentro de la célula es rápidamente hidrolizada y convertida en cisteína .Luego de 2 horas de laadministración oral de NAC a ratas, la concentración más alta se observó en el riñón y el hígado, seguido de las glándulas suprarrenales, los pulmones, el bazo, lasangre, los músculos y el cerebro. La NACA (NAC acetilada), es un metabolito activo que atraviesa BHE (16, 17,19).
CONCLUSIONES
La evidencia revisada indica que los efectos antiinflamatorios y neuroprotectoresde la NAC forman parte de un eje multifactorial que integra mecanismosantioxidantes, redox y glutamatérgicos, ofreciendo una base biológica coherentepara su uso adyuvante en diversos trastornos psiquiátricos.
No obstante, esta interpretación debe abordarse con cautela crítica. La mayoría delos estudios disponibles son ensayos de pequeña o mediana escala, conheterogeneidad metodológica, muestras clínicas diversas y variabilidad en dosis, duración y combinaciones farmacológicas. Estas limitaciones dificultan establecer una relación causal robusta entre la modulación inflamatoria y los beneficios sintomáticos observados.
Además, aunque los resultados en EZQ son consistentes , particularmente en la reducción de síntomas negativos y residuales, su magnitud de efecto suele ser modesta (dife- rencias absolutas de 2–4 puntos en subescalas PANSS o MA- DRS), lo que sugiere un papel coadyuvante, no sustitutivo, dentro del abordaje farmacológico integral.
Desde una perspectiva traslacional, la falta de biomarcadores específicos que correlacionen la respuesta clínica con cambios en marcadores inflamatorios o redox sigue siendo una deuda pendiente. La integración de neuroimagen funcional, proteómica y análisis longitudinales del eje neuroinmune podríaayudar a delimitar mejor los subgrupos de pacientes que más se benefician del tratamiento con NAC.
Finalmente, el futuro del campo probablemente dependerá de la combinaciónracional de NAC con otros agentes moduladores del estrés oxidativo e inflamatorio —como antioxidantes mitocondriales, inhibidores de microglía o antiinflamatorios selectivos del SNC—, dentro de estrategias personalizadas de neuroprotección psiquiátrica.
Psicofarmacología26:139, febrero de2026
Tabla 1
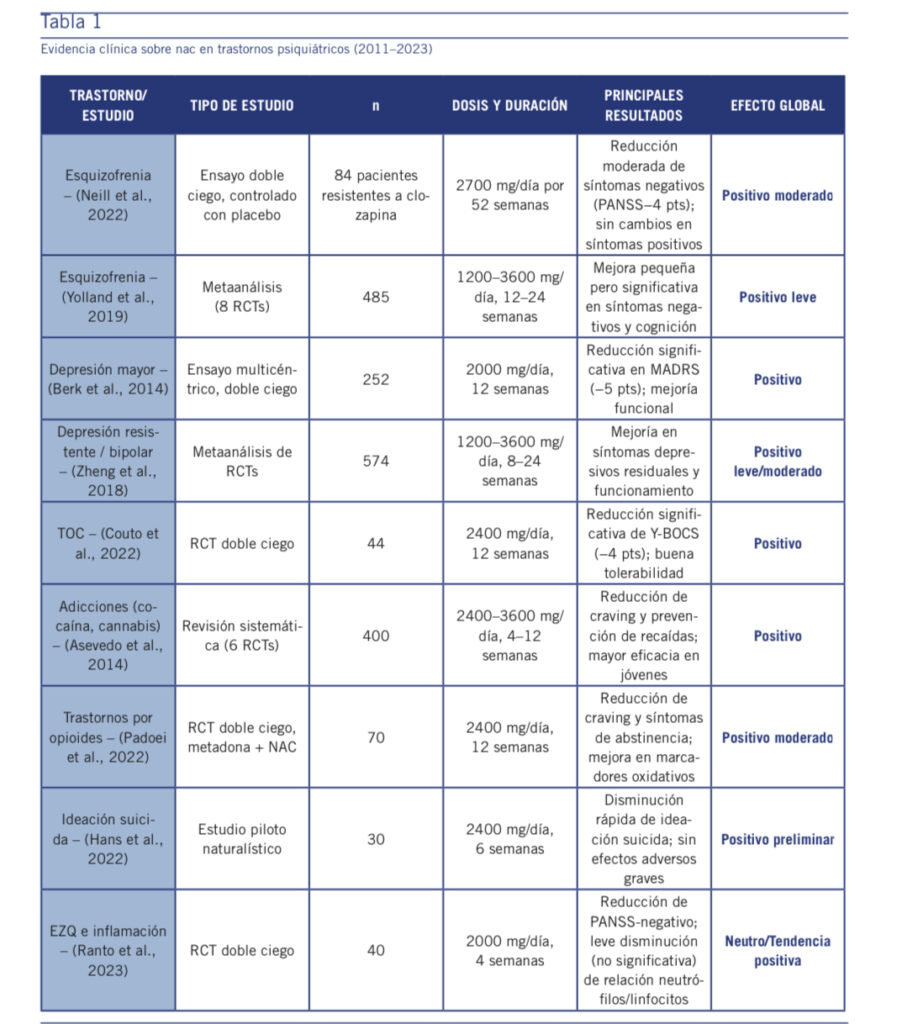
En síntesis, la NAC representa una intervención segura, accesible y conceptualmente atractiva, pero su impacto clínico real todavía requiere confirmación mediante estudios multicéntricos, controlados y de mayor potencia estadística, que permitan traducir la plausibilidad biológica en evidencia clínica definitiva.
Psicofarmacología26:139, febrero de2026
BIBLIOGRAFÍA
• 1- Bradlow, R., Berk, M., Kalivas, P., Back, S., & Kanaan, R. (2022). The Potential of N-Acetyl-L-Cysteine (NAC) in the Treatment of Psychiatric Disorders. CNS Drugs, 36, 451 -482. https://doi. org/10.1007/s40263-022-00907-3.
• 2- Dean O., Giorlando, F., Berk, M. (2011). N-acetylcysteine in psychiatry: current therapeutic evidence and potential mechanisms of action.. Journal of psychiatry &neuroscience : JPN, 36 2, 78-86 . https://doi.org/10.1503/jpn.100057.
• 3- Asevedo, E., Mendes, A., Berk, M., & Brietzke, E. (2014). Systematic review of N-acetylcysteine in the treatment of addic- tions.. Revista brasileira de psiquiatria, 36 2, 168-75 . https://doi. org/10.1590/1516-4446-2013-1244.
• 4- Ooi, S., Green, R., & Pak, S. (2018). N-Acetylcysteine for the Treatment of PsychiatricDisorders: A Review of Current Evidence. BioMed Research International, 2018.https://doi. org/10.1155/2018/2469486.
• 5- Silva-Netto, R., Jesus, G., Nogueira, M., & Tavares, H. (2014). N-acetylcysteine in the treatment of skin-picking disorder.. Revista brasileira de psiquiatria, 36 1, 101 . https://doi.org/10.1590/1516-
4446-2013-1154.
• 6- Berk, M., Dean, O., Cotton, S., Jeavons, S., Tanious, M., Kohl- mann, K. et al (2014).The efficacy of adjunctive N-acetylcysteine in major depressive disorder: a double-blind,randomized, placebo-con- trolled trial. The Journal of clinical psychiatry, 75 6, 628-36 .https:// doi.org/10.4088/jcp.13m08454.
• 7- Zheng, W., Zhang, Q., Cai, D., Yang, X., Qiu, Y., Ungvari, G et al (2018). Nacetylcysteine for major mental disorders: a systematic review and meta
analysis of randomized controlled trials. Acta Psy- chiatrica Scandinavica, 137.https://doi.org/10.1111/acps.12862.
• 8- Yolland, C., Hanratty, D., Neill, E., Rossell, S., Berk, M., Dean, O et al (2019). Meta-analysis of randomised controlled trials with N-acetylcysteine in the treatment of schizophrenia. Australian & New Zealand Journal of Psychiatry, 54, 453 – 466. https://doi. org/10.1177/0004867419893439.
• 9- Neill, E., Rossell, S., Yolland, C., Meyer, D., Galletly, C., Harris,
A. et al (2022). N-Acetylcysteine (NAC) in Schizophrenia Resistant to Clozapine: A Double-Blind, Randomized, Placebo-Controlled Trial Targeting Negative Symptoms. Schizophrenia Bulletin, 48, 1263 – 1272. https://doi.org/10.1093/schbul/sbac065.
• 10- Padoei, F., Mamsharifi, P., Hazegh, P., Boroumand, H., Ostad- mohammady, F.,Abbaszadeh-Mashkani, S et al (2022). The therapeu- tic effect of N-acetylcysteine as anadd-on to methadone maintenance therapy medication in outpatients with substance use disorders: A randomized, double-blind, placebo-controlled clinical trial. Brain and Behavior, 13. https://doi.org/10.1002/brb3.2823.
• 11- Couto, S., Rodrigues, J., Trigo, P., Da Luz, B., & Gil, V. (2022). The Role of N-Acetylcysteine in Obsessive-Compulsive (OCD) and Re- lated Disorders. European Psychiatry, 65, S644 – S645. https://doi. org/10.1192/j.eurpsy.2022.1653.
• 12- Ranto, I., Herdaetha, A., & Kusuma, W. (2023). Effectiveness of Adjuvant Treatment of N-Acetylcysteine on Negative Symptoms and Neutrophil-Lymphocyte Ratio (NLR) in Schizophrenic Patients. JUXTA: Jurnal Ilmiah Mahasiswa Kedokteran Universitas Airlangga. https://doi.org/10.20473/juxta.v14i22023.70-75.
• 13- Hans, D., Rengel, A., Hans, J., Bassett, D., & Hood, S. (2022). N-Acetylcysteine as anovel rapidly acting anti-suicidal agent: A pilot naturalistic study in the emergency setting. PLoS ONE, 17. https://
doi.org/10.1371/journal.pone.0263149.
• 14- Najjar S, Pearlman DM. (2015) Neuroinflammation and white matter pathology in schizophrenia: systematic review. Schi- zophr Res. 2015;161(1):102–12. https://doi.org/10.1016/j. schres.2014.11.041
• 15- Coles AS, Kozak K, George TP. (2018) A review of brain gluta- mate, oxidative stress,and antioxidants in schizophrenia. CNS Spectr. 23(3):230–7.doi.org/10.1017/S1092852917000205
• 16- Bavarsad Shahripour R, Harrigan M, Alexandrov A (2014). N-acetylcysteine (NAC) in neurological disorders: mechanisms of actionand therapeutic opportunities. Brain and Behavior; 4(2): 108–
122. DOI: 10.1002/brb3.208
• 17-Angemi JA. (2022) N-acetilcisteína: relación entre mecanismos de acción y probablesusos en trastornos neuropsiquiátricos. Psicofar- macología ; 130:4-12.
• 18- Ramos-Villegas Y, Padilla-Zambrano H,Blanco-Teherán C, López-Cepeda D, Quintana-Pájaro L, Corrales-Santander H et al. (2017). N-Acetilcisteína en neuroprotección y lesión traumática ce- rebral: revisión de la literatura. Rev. Chil. Neurocirugía 43: 166-169.
• 19- Samuni, Y, Goldstein S, Dean O, Berk M (2013). The chemistry and biologicalactivities of N-acetylcysteine. Biochim. Biophys Acta 1830: 4117–4129. DOI: 10.1016/j.bbagen.2013.04.016






