Aumento de peso por antipsicóticos, sus efectos en los tejidos
Resumen
La cada vez más alta prevalencia del síndrome metabólico (SM) en la población humana aumenta y acelera la evolución de las enfermedades crónicas de la esfera cardiovascular-metabólica, entre ellas, la pandemia diabética y la hipertensión arterial con sus consiguientes secuelas. Por otro lado, la dispensa de medicamentos aumenta continuamente, año tras año; en parte por la aparición de nuevos tratamientos que han cambiado y mejorado la expectativa de vida, y en parte por el marketing aplicado, ya que el ser humano es proclive al consumo de los mismos. No es de extrañar entonces que a las posibles causas generales del SM, se agregue la generada por uso de varios fármacos que como efecto adverso lo desencadena. Son ejemplos, los psicofárma- cos y anticonvulsivantes, los antihistamínicos clásicos, los antirretrovirales inhibidores de la proteasa, ciertos antibióticos como las quinolonas, los corticoides y varios más. Paradójicamente, muchas de estas moléculas son de amplia prescripción y consu- mo como consecuencia de las complejas situaciones socio-culturales que se presentan en el devenir diario de las sociedades.
Hace más de 10 años hemos advertido el problema en nuestro medio con relación al uso de psicofármacos en general y a los antipsicóticos (AP) en particular como desencadenantes de SM publicando una revisión sobre el tema; asimismo, en la misma revisión se establecieron algunas recomendaciones para la prevención/reducción del mismo en la población vulnerable, en con- cordancia con el Consenso Americano Intersocietario sobre antipsicóticos, diabetes y obesidad de ese tiempo.
Por todo lo mencionado, son objetivos de esta presentación revisar, siguiendo la biología de sistemas, los distintos procesos por los cuales los psicofármacos, especialmente los AP, pueden desencadenar SM; a la vez que mostrar, en lo posible, aquellos mecanismos moleculares conocidos y cuál podría ser la contribución de la patología de base en su desarrollo.
Palabras clave
Síndrome metabólico – Lípidos – Antipsicóticos – Biología molecular.
Serra Héctor Alejandro Serra, Muñoz Santiago. “Aumento de peso por antipsicóticos, sus efectos en los tejidos”. Psicofarmacología 2021;128:14-17. Puede consultar otros artículos publicados por los autores en la revista Psicofarmacología en sciens.com.ar
Introducción
Actualmente el síndrome metabólico es una patología muy frecuente en la población general. Esta problemática de salud no es ajena a los pacientes psiquiátricos, especialmente aquellos que presentan diagnóstico de esquizofrenia y trastorno bipolar. El síndrome metabólico es un conjunto de signos físicos y bioquímicos como obesidad, dislipemia y disglucemia de etiología imprecisa que, a partir de la cuarta década de vida, predispone al desarrollo de enfermedad vascular, endocrinopatías, trastornos osteoarticulares y neoplasias con importante morbimortalidad. Hoy día, el síndrome metabólico ha sufrido una conversión epidémica mundial que, vista en perspectiva, se debería al estilo de vida adoptado por el ser humano en los últimos tiempos, aun zanjando sus idiosincrasias étnico-socio-culturales.
Por otro lado, la aparición de nuevos tratamientos farma- cológicos ha mejorado la expectativa y calidad de vida de los enfermos. Sin embargo, como estas moléculas no son inocuas y en general deben recibirse en forma prolongada, esto ha condicionado la aparición de nuevas situaciones que otrora
no se veían. No es de extrañar entonces que, entre los efectos adversos crónicos de una gran variedad de drogas como an- tipsicóticos, antidepresivos, anticonvulsivantes, glucocorticoi- des, antirretrovirales, antihistamínicos, antineoplásicos, etc. se agregue también el síndrome metabólico.
La biología de sistemas enfoca la enfermedad y sus tratamientos en diversos niveles desde lo molecular a lo social, y viceversa. Bajo sus propiedades emergentes los fármacos causales de síndrome metabólico pueden ser vistos a nivel celular-orgánico como llaves o interruptores moleculares que producen obesidad, hipertensión o diabetes, pero a nivel social como una gran carga que debe soportar la población toda. Por ello, el objetivo de esta revisión es comprender los mecanismos que se ponen en marcha para generar síndrome metabólico en los pacientes con antipsicóticos. Creemos que es de especial interés para la práctica médica, el conocimiento de los mecanismos fisiopatológicos de las enfermedades y su constante actualización en el estado del arte.
Psicofármacos y mecanismos involucrados
Los psicofármacos son moléculas lo suficientemente liposolubles o anfifílicas como para permanecer en el interior celular un cierto tiempo e interferir con canales, bombas, transportadores y sistemas de señalización, o ser sustratos-inhibido- res-inductores de reacciones del metabolismo intermedio o reacciones de depuración xenobiótica del organismo.
Por lo expresado, las formas mediante las cuales las sustan- cias mencionadas podrían generar síndrome metabólico se- rian afectando la neurotransmisión en circuitos procesadores de conductas homeostáticas complejas y de la recompensa, modificación de tejidos o de su accionar neuroendocrino y es objetivo de esta parte comentarlas.
- Interferencia sobre la neurotransmisión central e hipota- lámica:
Diferentes estudios han vinculado el antagonismo-agonismo inverso de distintos neuro y psicofármacos sobre receptores hipotalámicos H1 y 5-HT2c con su capacidad inductora de síndrome metabólico. Tanto las pocas neuronas histaminérgi- cas túbero-mamilares como las serotonérgicas del rafe proyectan sus fibras axonales por todo del SNC pues participan en varias funciones homeostáticas y cognitivas. De acuerdo con la figura 1 ambos sistemas producen anorexia ya que, directa o indirectamente, estimulan las neuronas POMC/CART del núcleo arcuato (Arc) o inhiben las orexinérgicas del núcleo paraventricular (PVN) y empleando los receptores mencionados. Para los receptores H1, cuanto mayor es la afinidad antago- nista de la droga usada (menor pA2) mayor es el efecto orexígeno que aparece durante el tratamiento crónico (superior a las 4-6 semanas), esto se comprueba para los antipsicóticos,
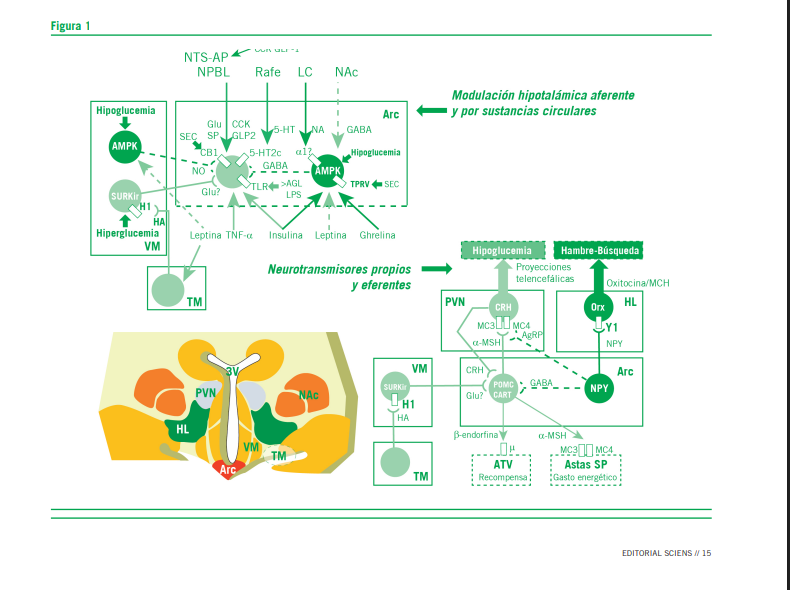
antidepresivos tricíclicos y antihistamínicos clásicos (aunque muchas veces el empleo de difenhidramina, clorfeniramina o hidroxizina es corto y esporádico). En cambio, para los re- ceptores 5-HT2c no se aplica lo dicho ya que presentan acti- vidad constitutiva estimulando las neuronas que lo expresan, como las POMC/CART, sin necesidad de neurotransmisor. La variedad 5-HT2c es la que menos se expresa en el sistema nervioso central y, además, es una de las pocas proteínas que sufren edición postranscripcional, la cual modifica di- cha actividad basal. Los antipsicóticos atípicos tetracíclicos: clozapina, olanzapina y quetiapina, y el antihistamínico ci- proheptadina son agonistas inversos 5-HT2c, mientras que los atípicos haloalquil derivados: risperidona, ziprasidona y aripiprazol son antagonistas puros. De los mencionados, los agonistas inversos exhiben mayor actividad orexígena, explica- ble por la supresión de la actividad constitutiva 5-HT2c sobre las neuronas blanco que dejan de estar estimuladas en forma tónica. Asimismo, a nivel del Locus Coeruleus (LC) interneu- ronas GABAérgicas expresando también receptores 5-HT2c generarían un tono basal inhibitorio sobre las neuronas nora- drenérgicas que activan la conducta orexígena; la interacción de estos agonistas inversos a ese nivel crearía una inhibición de la inhibición con descarga de noradrenalina en el hipotála- mo activando el apetito.
- Interferencia sobre la neurotransmisión autonómica:
El sistema nervioso parasimpático es un estimulante adi- cional de la secreción insulínica a través de la presencia de mAChR tipo 3; mientras que el simpático es un inhibidor po- tente mediante receptores a1, ambos ubicados sobre las pro- pias células beta. Así se pensó que estos receptores podrían generar cuadros metabólicos o integrarse con otros defectos para ocasionarlos a través de una disfunción insulínica. La hipótesis más sencilla señala que el bloqueo persistente mA- ChR y a dado por antipsicóticos y antidepresivos tricíclicos podría respectivamente menoscabar o sobrecargar la capa- cidad funcional beta, promoviendo hipo e hiperinsulinemias alternantes transitorias con las consecuencias previstas. Sin embargo, una serie de evidencias contradictorias diluirían la importancia de estos mecanismos autonómicos; por ejemplo, los anticolinérgicos antiespasmódicos no promueven cambios en la secreción de insulina en forma apreciable, la clozapina (antipsicótico atípico) produce sialorrea, efecto estimulante más que antagónico de los mAChR, y estudios en animales de experimentación muestran que el efecto modulador autonó- mico de la secreción insulínica dependería de varios mecanis- mos incluso parácrinos.
El tejido adiposo y su relación con los antipsicóticos atípicos
Es ya conocido que el tejido adiposo se incrementa en los casos de aumento de peso por el efecto adverso de los antipsicóticos atípicos. Se postulan varios mecanismos por los cuales los antipsicóticos atípicos podrían ejercer el efecto adverso tan frecuente de aumento de los depósitos de lípidos a saber:
Efecto de los antipsicóticos de segunda generación sobre la diferenciación de los adipocitos blancos
Las proteínas de unión a elementos reguladores de esteroles SREBP (sterol regulatory element-binding protein), constitui- das por SREBP 1a, 1c y SREBP-2 presentan un rol regulato- rio en la diferenciación de los preadipocitos en su pasaje un adipocito maduro. Las proteínas de unión a elementos regu- ladores de esteroles (SREBP) son una familia de factores de transcripción que regulan la biosíntesis de lípidos y la adipo- génesis mediante el control de la expresión de varias enzimas necesarias para la síntesis de colesterol, ácidos grasos, triacil- glicerol y fosfolípidos.
Ensayos in vitro sobre preadipocitos murinos 3 T3-L1 en los que se los trataba con Olanzapina presentaban una activación de SREBP 1. Asimismo, se ha documentado que clozapina in- duce la expresión de SREBP-1 en las etapas tempranas y tar- días de la diferenciación de células madre derivadas de tejido adiposo humano. Estos ejemplos junto a otras modificaciones moleculares especificas en los adipocitos muestran como los antipsicóticos de segunda generación están involucrados en el aumento de expresión de SREBP con el consiguiente efecto lipogénico.
Efecto de los antipsicóticos de segunda generación en la fun- ción endocrina del tejido adiposo
Para iniciar podemos nombrar a una famosa adipocina, la adiponectina, que es una de las moléculas más relevantes secretadas por los adipocitos. Esta proteína modula caminos de metabolización de los hidratos de carbono, lípidos y procesos vasculares en base a sus propiedades antiinflamatorias, anti-aterogénicos y sensibilizante de insulina. No hay al momento una corriente homogénea de pensamiento en torno a la expresión de adiponectina, debido a que se encuentran en la literatura ensayos donde el tratamiento con distintos antipsicóticos de segunda generación brinda resultados diferentes, es decir, en algunos aumenta la expresión de adiponectina mientras en otros disminuye.
Podemos también nombrar a otra adipocina, la leptina, que está ampliamente relacionada al aumento de la grasa del cuer- po. Presenta función moduladora sobre la ingesta de comida, así como también sobre el gasto energético. Se ha reportado que la exposición de los pre-adipocitos 3T3-l1 a clozapina por 2 o 10 dias, produce una disminución en los niveles de ARNm de leptina así como también disminuye su secreción en el medio de cultivo. Es de interés nombrar que en este es- tudio los autores también testearon en las células de prueba 3T3-L1 a los principios activos difenhidramina, e histamina, donde se falló en la modificación de los niveles de leptina. Esto sugiere que los procesos que involucran la leptina no estarían mediados a través de los receptores H1. Por otro lado, el tratamiento con serotonina si genero una disminución en la secreción en comparación con las células control, al mismo tiempo, no se encontró en los testeos una función sinergística o aditiva cuando se combinó con la clozapina.
Discusión y conclusiones
El SM relacionado al uso de psicofármacos es un problema evidente que reduce la expectativa de vida de los pacientes psiquiátricos; por ello, cuanto más se conozca sobre él, mejor podrá ser resuelto
Sin embargo, 3 puntos deben ser señalados al analizar este problema.
Primero, las observaciones clínicas no siempre se correlacionan con las experimentales así que muchas veces no es fácil de interpretarlas. Esta debilidad podría deberse en parte a la duración de los estudios con psicofármacos; estos son de corto plazo (meses) mientras que los tratamientos prescriptos los exceden ampliamente (años). Por ello se recurre a modelos como los comentados para suplir estas discrepancias. Stahl y colaboradores han propuesto un “modelo de autopista” para explicar la evolución del SM inducido por AP; no obstante, más que un camino recto a un punto, el SM inducido por psicofármacos sería un círculo sin salida; la ganancia de peso por hiperorexia es evidente para los AP y los antidepresivos tri- cíclicos pues el bloqueo agudo de los GPCRs aminérgicos in- terfiere sobre las vías centrales de control de ingesta y recom- pensa. Sin embargo, las acciones intracelulares analizadas parecen ser lo suficientemente fuertes para iniciar y continuar por tiempo indefinido manifestaciones como obesidad, dispi- lemia, etc.; acciones que se retroalimentan y que conducen a la falla insulínica cuando el páncreas endócrino no puede sustentar la situación, y así para comenzar de nuevo con un cuadro agravado con intolerancia a la glucosa y trastornos vas- culares. Evidentemente, aquellos fármacos que cuenten con más de un mecanismo, como los AP atípicos y los antimaníacos, y sean expuestos por más tiempo más eficientes serán a la hora de generar SM.
Segundo, existe cierta falta de conocimiento sobre cuánto puede contribuir la patología de base a la génesis de SM en estos pacientes. Ya Allison y colaboradores muestran en su metaanálisis que la esquizofrenia por si sola cursa con ganancia de peso leve pero significativa, aunque no le adjudican importancia. Se han sugerido como posibles causas de la misma la inactividad o el sedentarismo, junto al tabaquismo y al patrón alimentario actual; pero este enfoque sencillo se ve contrastado por varias observaciones que sugieren predisposición al SM en las enfermedades mentales.
Y tercero, un aspecto poco claro es cuánto puede influir la carga genética de cada paciente para favorecer o no la aparición de SM ante el uso de alguno de los fármacos en particular. Se ha escrito mucho sobre el polimorfismo en la región promotora del gen para el receptor 5-HT2c (cambio de citosina por timina o C/T en posición -759) y ganancia de peso por AP atípicos. Sin embargo, el alelo C es proclive al aumento de peso tanto en individuos sanos como en enfermos tratados con AP.
En suma, se podría admitir que los psicofármacos desencadenan SM porque crean un desacople entre las señales neuroendócrinas externas (inhibición a nivel de los receptores) y los reguladores metabólicos intracelulares (por activación metabólica directa) y ello cause el círculo sin salida donde las terapias higiénico-dietéticas y farmacológicas que se indiquen tiendan al fracaso. Pero, cuidado, el terminar en diabetes tipo 2 o en sus complicaciones implica también descuido profesional y subvaloración de la situación.
Bibliografía
- Alegría Ezquerra E, Castellano Vázquez JM, Alegría Barrero A. Obesity, metabolic síndrome, and diabetes: Cardiovascular implications and therapy. Rev Esp Cardiol 2008; 61: 752-64.
- Bertolio, R., Napoletano, F., Mano, M. et al. Sterol regulatory element binding protein 1 cou- ples mechanical cues and lipid metabolism. Nat Commun 10, 1326 (2019).
- Bonnavion P, Mickelsen LM, Fujita A, de Le- cea L, Jackson AC. Hubs and spokes of the late- ral hypothalamus: Cell types, circuits and beha- viour. J Physiol 2016; 594: 6443-62.
- Calzada Leon, et al. Reguladores neuroendo- crinos y gastrointestinales del apetito y la sa- ciedad. Boletín médico del Hospital Infantil de México, 65(6), 468-487.
- Chargraoui A, Thibaut F, Skiba M, Thuillez C, Bourin M. 5-HT2C receptors in psychiatric disor- ders. A review. Prog Neuropychopharmacol Biol Psychiatry 2016; 66: 120-35.
- Chen, C.C., et al., Overexpression of Insig-2 inhibits atypical antipsychoticinduced adipoge- nic differentiation and lipid biosynthesis in adi- pose-derived stem cells. Sci Rep, 2017. 7(1):
p. 10901,
- Fadel DO, Barmat R, Plotquin Y, Serra HA. Los antipsicóticos y su influencia en la generación del síndrome metabólico y de cardiopatías. Psi- cofarmacología 2005; 5(32): 27-33.
- Ferreira V, Grajales D, Valverde ÁM. Adipose tissue as a target for second-generation (atypi- cal) antipsychotics: A molecular view. Bio- chim Biophys Acta Mol Cell Biol Lipids. 2020 Feb;1865(2):158534.
- Heymsfield, S.B., et al., Recombinant leptin for weight loss in obese and lean adults: a rando- mized, controlled, dose-escalation trial. JAMA, 1999. 282(16): p. 1568-75.
- Kurzthaler, I. and W.W. Fleischhacker, The clinical implications of weight gain in schi- zophrenia. J Clin Psychiatry 2001. 62 Suppl 7:
p. 32-7.
- Manu, P., et al. Weight gain and obesity in schizophrenia: epidemiology, pathobiology, and management. Acta Psychiatr Scand 2015. 132(2): p. 97-108.
- Pillinger T, Beck K, Stubbs B, Howes OD. Cho- lesterol and triglyceride levels in first-episode psychosis: Systematic review and meta-analysis. Br J Psychiatry 2017; 211: 339-49.
- Serra HA, Fadel DO. Síndrome metabólico y psicofármacos, un fenómeno creciente y peligro-
so. Parte 1. Revista de la Sociedad Argentina de Endocrinología Ginecológica y Reproductiva 2017; 24: 14-26.
- Serra HA, Fadel DO. Síndrome metabólico y psicofármacos, un fenómeno creciente y peligro- so. Parte 2. Revista de la Sociedad Argentina de Endocrinología Ginecológica y Reproductiva 2017; 24: 66-72.
- Stahl SM, Mignon L, Meyer JM. Which comes first: Atypical antipsychotic treatment or car- diometabolic first? Acta Psychiatr Scand 2009; 119: 171-9.
- Trujillo, M.E. and P.E. Scherer, Adiponec- tin-journey from an adipocyte secretory protein to biomarker of the metabolic syndrome. J Intern Med, 2005.257(2): p. 167-75.
- Watts AG. The structure of the neuroendocrine hypothalamus: The neuroanatomical legacy of Geoffrey Harris. J Endocrinol 2015; 216: T25-39.
- Ye, J. and R.A. DeBose-Boyd, Regulation of cholesterol and fatty acid synthesis. Cold Spring Harb Perspect Biol, 2011. 3(7).
- Yeo SH, Colledge WH. The role of Kiss1 neu- rons as integrators of endocrine, metabolic and environmental factors in the hypothalamic-pitui- tary-gonadal axis. Front Endocrinol (Lausanne) 2018; 9: 188.







No comments! Be the first commenter?