Intervenciones neuropsicofarmacológicas en los trastornos parafílicos
Resumen
El trastorno parafílico es una patología que a partir del DSM 5 tiene una entidad propia y diferencial de las parafilias como eran concebidas. Tiene múltiples atravesamientos desde los cuales ha sido estudiado, descripto, interpretado y hasta justifi- cado su abordaje en distintos contextos clínicos. En el presente artículo se abordarán las estrategias neuropsicofarmacológicas aplicadas a este trastorno, sus bases neurobiológicas y el marco clínico actual con focalización en las características semioló- gicas y conductuales. Se analizarán las publicaciones referidas al tema y propuestas de tratamiento farmacológico con especial atención en sus bases biológicas de intervención.
Palabras clave
Trastornos parafílicos – Parafilia – Neuropsicofarmacología – Riesgo.
Martín Mazzoglio y Nabar, Daniel Silva. “Intervenciones neuropsicofarmacológicas en los trastornos parafílicos”. Psicofarmacología 2020;124:18-30. Puede consultar otros artículos publicados por los autores en la revista Psicofarmacología en sciens.com.ar
Introducción
La conducta sexual humana está atravesada por componen- tes biológicos, psicológicos, sociales, culturales y antropoló- gicos. Es subjetiva para cada persona humana -en tanto su autopercepción- al tiempo que se asienta sobre un soporte biológico dentro de un contexto psicosocial y, si bien se re- conocen etapas o fases, la duración y contenido de estas son heterogéneas.
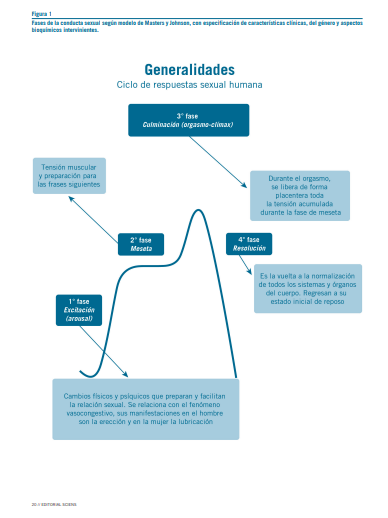
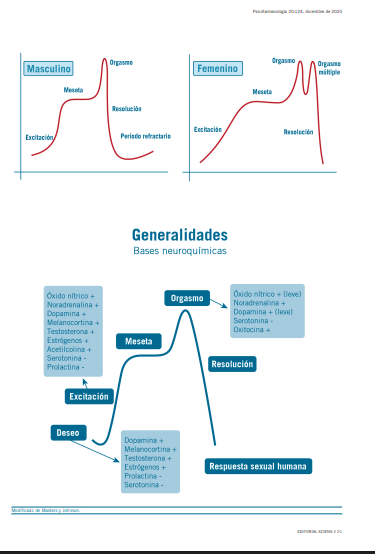
Esta conducta sexual, según Masters y Johnson, consta de distintas fases en las que se involucran neurotransmisores y hormonas que ejercen su acción tanto a nivel central como periféricos. Distintas áreas del cerebro humano se activan para dar una respuesta frente a los estímulos diversos y he- terogéneos. En el gráfico 1 se especifican las características conductuales y neuroquímicas del ciclo de la respuesta sexual
humana con su diferencia entre los hombres y las mujeres. Esta diferencia descripta en el ciclo de la conducta sexual hace décadas, fue ratificada y ampliada por estudios de neu- roimagen funcional que estudiaron mediante resonancia mag- nética funcional el cerebro de distintos sujetos según género y discriminaron el procesamiento de imágenes sexuales en zonas distintas (Gráfico 1).
En relación con la fase de excitación sexual, y desde un punto de vista neurobiológico, Redouté et al. (2000) plan- tearon un modelo neuroconductual con 4 componentes: cog- nitivo, emocional, motivacional y autonómico. El componente cognitivo se encarga de la categorización y evaluación del es- tímulo con aumento de la atención hacia el estímulo sexual, sus procesos se relacionan con las regiones de las cortezas prefrontal orbitaria y parietal superior; el componente emocio-
nal se asocia con la cuantificación hedónicadel estímulo en displacentero o placentero y se correlaciona con las cortezas somatosensorial secundaria, insular anterior, el complejo nu- clear amigdalino que evalúa el contenido emocional del es- tímulo sexual y el procesamiento general de las emociones, así como con la modulación que ejerce la corteza prefrontal dorsal y medial; el componente motivacional se asocia con las regiones caudales del giro cingulado anterior (que mediante las proyecciones con el estriado ventral focalizan la atención ejecutiva y se relacionan con zonas del componente cogniti- vo); y el componente autonómico relacionado con los efectos sobre aparatos cardiovascular y respiratorio, y está asentado en la activación de las zonas mediales del hipotálamo, cor- tezas insulares posteriores y las porciones rostrales del giro cingulado anterior.
Las parafilias secaracterizan por la excitación sexual como
respuesta a objetos o situaciones sexuales que no forman par- te de los estímulos adecuados,normativos, o convencionales y que, en diversos grados, pueden interferir con la aptitud para una actividad sexual efectiva recíproca.
La palabra fue acuñada por el psiquiatra y psicoanalista austríaco Wilhelm Stekel -quien fuera considerado como el mejor discípulo de Freud (Wittels, 1924)- y deriva del grie- go antiguo. La etimología se referencia en los términos πara (pará), “al margen de” o “al lado de” y jilia (philía), “amor” sustantivoque hacereferencia a aquello por lo cual el indivi- duo se siente atraído convirtiéndolo en un objeto de amor.
A partir del DSM 5 se establece una importante distinción en lo que concierne a las parafilias puesto que establece una distinción entre la parafilia y el trastorno parafílico; no obstan- te, el manual divide los trastornos relacionados con la conduc- ta sexual en “disfunciones sexuales”, “trastornos parafílicos” y “disforia de género”.
Las parafilias no son ipso facto trastornos mentales, si bien una parafilia es condición necesaria pero no suficiente para tener un trastorno parafílico. Una parafilia per se no justifi- ca automáticamente la intervención clínica o no la requiere, por su parte el trastorno parafílico es una parafilia que causa malestar o deterioro en el sujeto, o cuya satisfacción supuso un daño personal o riesgo de daño ajeno. Los sujetos que presen- tan estas ideaciones (que muchas veces quedan en el plano de la fantasía) o conductas que les generan deterioro, riesgo personal o a terceros, no presentan conciencia de enferme- dad que lleven la problemática a consulta para un tratamiento toda vez que concurren para realizarlo cuando los actos con- llevan conflictos con la sociedad o con la ley.
El objetivo del presente artículo es actualizar sobre las in- tervenciones farmacológicas de los trastornos parafílicos, con especificación de la distinción surgida en el DMS 5 sobre la clasificación de esta conducta sexual humana devenida en trastorno, entendido como “un síndrome caracterizado por una alteración clínicamente significativa del estado cognitivo, la regulación emocional o el comportamiento de un individuo, que refleja una disfunción de los procesos psicológicos, bio-
lógicos o del desarrollo que subyacen en su función mental y que habitualmente van asociados a un estrés significativo o una discapacidad, ya sea social, laboral o de otras actividades importantes”.
Desarrollo Delimitación clínica
Como hemos señalado, los trastornos parafílicos son una patología codificada en el DSM 5 como F65.xe implican la excitación sexual ante objetos, situaciones y/o destinatarios atípicos para las convenciones socio-culturales del entorno como ser niños (trastorno de pedofilia), objetos o situaciones (trastorno de fetichismo), roces (trastorno de froteurismo), ex- hibiciones (trastorno de exhibicionismo), los actos de humi- llar, golpear, atar o generar sufrimiento en otro/s (trastorno de masoquismo sexual con o sin asfixiofilia), o los cuadros clasi- ficados como trastornos parafílicos no especificados que in- cluyen cadáveres (necrofilia), animales (zoofilia), entre otros. Cabe destacar que algunas prácticas que pueden parecer in- usuales a otras personas o al personal sanitario no constituyen un trastorno parafílico simplemente porque sean inusuales y que los sujetos pueden tener intereses parafílicos, pero no cumplen los criterios para el trastorno.
Las fantasías parafílicas son recurrentes e intensas de ex-
citación sexual, con comportamientos sexuales angustiosos o incapacitantes y que involucran dichos objetos o personas sin consentimiento, o el sufrimiento o la humillación de la misma persona o de la/s pareja/s (partenaire sexual) con probabilidad de causar daño. Pero se debe aclarar dos puntos cruciales:
- las conductas sexuales no convencionales per se no son una desviación o constituyen una parafilia, más aún si son aisladas, existe una elasticidad lúdica dentro de la sexualidad que es característica natural de la función erótica;
- si el comportamiento sexual (convencional o no) no es nocivo para los participantes y es llevado a cabo por adultos que consienten sin ninguna clase de coerción y no visto por terceros, se debe considerar como un comportamiento privado y personal.
Como características semiológicas se resaltan que estas fantasías deben ser intensas y persistentes, así como provo- car angustia o deterioro significativo en áreas sociales, etc. o tienen el potencial de dañar a otros. Muchas veces el capital imaginativo de la fantasía parafílica genera sentimientos de culpa y vergüenza, así como disforia hasta que no es concre- tada. Asimismo, pueden tener una alteración en la capacidad de sentir afecto y mantener intimidad emocional sexual recí- proca, como entre otros aspectos
Existe controversia en torno a la etiología del trastorno para- fílico. Si bien la mayoría de las explicaciones actuales asocian procesos a psicodinámicos, con el advenimiento del avance de las neurociencias, mediante neuroimágenes se hallaron alteraciones en el funcionamiento y la anatomía cerebral de alguno de los trastornos como en los sujetos con trastorno de pedofilia.
Existen tres grados de manifestación de las conductas pa- rafílicas:
- mínima, donde la expresión erótica fantaseada es placen- tera para el individuo y aparece espontáneamente sin pertur- bar actividades sexuales convencionales y/o cotidianas del sujeto;
- acentuada, donde la expresión erótica es fantaseada o actuada, placentera para el sujeto, pero el mismo busca insis- tentemente concretarla para satisfacer las actividades sexua- les cotidianas del individuo y afecta las actividades de la vida diaria u otros órdenes de la vida;
- predilecta o dependiente, aquí la expresión erótica inter- fiere la actividad sexual convencional y/o cotidiana del sujeto reemplazándola en forma electiva, preferencial (prevalente) o única (exclusiva).
El grado mínimo de la conducta parafílica corresponde a lo denominado parafilia y el grado dependiente al trastorno para- fílico dado el deterioro que causa. En el caso de la acentuada requiere de un profundo examen semiológico para valorar si la conducta constituye el trastorno.
Por último, no es infrecuente que en un mismo individuo se presenten varias parafilias, los trabajos de investigación publicados por Freund et al (1998), Abel y Osborn (1992) y Marshall (2007) lo ratifican con distintos porcentajes de pre- valencia. Además, la comorbilidad entre el trastorno parafílico con diagnósticos psiquiátricos del eje I (muchas veces la cau- sa de consulta) como los trastornos depresivos, del espectro bipolar, fobias, por déficit de atención y por uso problemático de sustancias que pueden ascender hasta el 70% de los ca- sos. Y los profesionales deben evaluar con especial atención a la comorbilidad con las conductas psicopáticas dado que se constituye un factor de riesgo asociado con conductas delic- tivas y criminales.
Tabla 1
Algoritmo de tratamiento de las parafilias y los trastornos parafílicos según la WFSBP (World Federation of Societes of Biological Psychiatry).
| Nivel | Descripción | Recomendación |
| 1 | Parafilias que no afectan las actividades sexuales convencionales ni cotidiana del sujeto. | Psicoterapia de tipo cognitivo-conductual. |
| 2 | Casos leves de trastornos parafílicos que no pasan al acto con bajo riesgo de violencia sexual. | Antidepresivos IRSS. |
| 3 | Trastornos parafílicos llevados al acto con caricias pero sin penetración y fantasías sexuales parafílicas sin sadismo sexual. | Antidepresivos IRSS con bajas dosis de antiandrógenos. |
| 4 | Riesgo moderado y alto de violencia sexual son sa- dismo sexual. | Dosis máxima de análogos esteroideos sintéticos. |
| 5 | Alto riesgo de violencia sexual y trastornos parafíli- cos severos. | Análogos de GnRH de larga duración. |
| 6 | Casos de extrema violencia. | Análogos de GnRH con análogos esteroideos sintéticos, se puede utilizar IRSS de forma conjunta. |
Psicofarmacología aplicada a la respuesta sexual humana
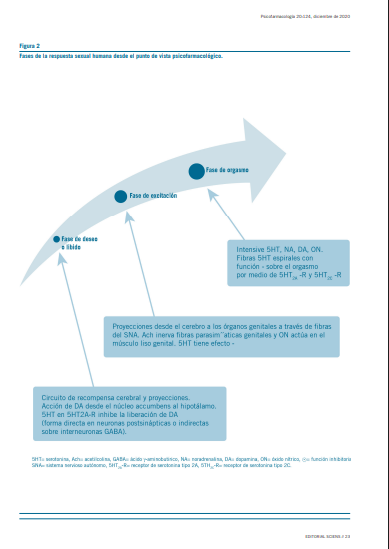
Desde el punto de vista psicofarmacológico, se pueden con- siderar 3 fases de la respuesta sexual en humanos, en función de los neurotransmisores implicados en cada una. Las fases son: fase de deseo o libido, fase de la excitación o arousal y fase del orgasmo. El conocimiento de estas fases junto con sus neurotransmisores y modulares, basadas en un modelo lineal y esquemático, permitirá comprender las bases para las intervenciones neuropsicofarmacológicas (Gráfico 2).
La fase de deseo o de la libido es la primera y se relaciona con el impulso sexual. Aquí intervienen tanto neurotransmi- sores como hormonas y recuerdos de experiencias pasadas, motivo por el cual es una red psiconeuroendocrinológica que ejerce función de forma equilibrada para lograr un fin. En esta fase el circuito de recompensa cerebral humano tiene un lugar preponderante, y su neurotransmisor principal (dopami- na) es limitante para las funciones que se llevan a cabo. El circuito de recompensa cerebral se ubica en estructuras del encéfalo, subcorticales cerebrales y extra-cerebrales, y tiene distintas áreas que lo modulan como la amígdala, la corteza hipocampal y zonas de la corteza prefrontal. Su localización central se asienta en las proyecciones entre el núcleo accum- bens (perteneciente al estriado ventral, ubicado por debajo de la comisura anterior y con zonas caudales del cuerpo estriado) con el área tegmental ventral (o llamada área A10, ubica- da en la zona rostral del mesencéfalo superior). La dopamina del núcleo accumbens ejerce su acción en diversas zonas del hipotálamo para regular el deseo sexual como el área preóp- tica medial (relacionada con la motivación sexual en modelos de animales), el núcleo paraventricular (controla la respuesta genital) y el núcleo ventromedial (relacionado con conductas defensivas y sexuales). Además de la dopamina, intervienen la serotonina, la testosterona, los estrógenos, la melanocortina, la prolactina.
En relación con la serotonina, tiene una injerencia negativa sobre el deseo y motivación sexual dado su acción inhibitoria en la liberación de dopamina. Los receptores 5HT1A y 5HT2A influyen en la liberación de dopamina ya sea de forma directa o a través de neuronas gabaérgicas, pero tienen acciones opuestas. Los receptores 5HT2A actúan como freno dopaminérgico dado que cuando la serotonina se une en las neuronas postsinápticas se inhibe la liberación de dopamina. Asimismo, cuando la serotonina se une a este receptor ubica- do en las interneuronas gabaérgicas genera la liberación del GABA que inhibe la liberación de dopamina. Por su parte, la prolactina tiene una acción negativa en el deseo sexual y su implicancia en las disfunciones sexuales no está completamente descripta. De esta forma, los fármacos antagonistas del receptor 5HT2A estimulan la liberación de dopamina e inhiben la de prolactina.
La fase de excitación, con su impacto a nivel genital, comienza en el cerebro y para alcanzar los órganos diana recorre la médula espinal y discurre por las fibras del sistema nervio- so autónomo (simpáticas y parasimpáticas) hasta los tejidos de los órganos genitales. Aquí intervienen 2 neurotransmisores principalmente, la acetilcolina que inerva fibras parasimpáticas genitales y el óxido nítrico que actúa en el músculo liso genital; así como otros neurotransmisores que modulan la excitación sexual que son la serotonina (ejerce un efecto negativo), la noradrenalina, la melacortina, los estrógenos y la testosterona.
En la fase del orgasmo intervienen la serotonina, noradrena- lina, la dopamina y el óxido nítrico. Las fibras serotoninérgicas espinales descienden y tienen una función inhibitoria sobre el orgasmo al actuar en los receptores 5HT2A y 5HT2C.
En los casos de pacientes con conductas sexuales compul-
sivas, y desde una perspectiva neurobiológica, se hipotetiza que estarían asociados con una actividad anómala del circuito de recompensa y sus moduladores, puesto que existiría un dé- ficit en la inhibición desde áreas de la corteza prefrontal sobre el estriado ventral que respondería a una hiperactivación y reactividad del cuerpo amigdalino y el área tegmental ventral.
Estrategias terapéuticas neuropsicofarmacológicas
Uno de los principales autores que iniciaron publicaciones científicas a partir de estudios relacionados con esta temática fue Freund en la década de 1980.
• Inhibidores de la recaptación de serotonina selectivos
En la literatura científica no existen trabajos de investiga- ción realizados a doble ciego, randomizados, contra placebo del uso de IRSS en pacientes con trastornos parafílicos (Thi- baut et al, 2010; Hall et al., 2007; Briken & Kafka, 2007), pero el uso off-label (fuera de indicación, en relación con las indicaciones aprobadas por autorizadas regulatorias de un país) de los antidepresivos IRSS en el tratamiento de los trastornos parafílicos se constituyó como una indicación en la práctica clínica. Dado el mecanismo de acción de los IRSS, se considera que son útiles parcialmente para su tratamiento, puesto que disminuyen el deseo sexual mediante el aumento de la serotonina (Osborn & Wise, 2005). Sus efectos adversos incluyen la disfunción eréctil, alteraciones en la eyaculación y la disminución de la libido.
El descenso del deseo sexual y la prolongación para alcan- zar el orgasmo son los efectos secundarios de tipo adverso más prevalentes de estas moléculas, menos frecuente es la disfunción eréctil y con mucha menor prevalencia, la anorgas- mia. Cabe destacar que su prevalencia es estudios pivotales es baja debido al sub-reporte que tiene el efecto de los IRSS en la esfera sexual, debido a que la metodología empleada a través de autoreporte y se ponen en juego cuestiones de per- sonalidad y vergüenza en los pacientes; pero se han descripto tasas de hasta el 80 % de incidencia de impacto sexual debi- do al uso de estas moléculas (Hu et al. 2004). Cabe destacar que los estudios más nuevos señalaron que el uso crónico de antidepresivos IRSS afecta la fertilidad en los varones por su efecto en la concentración y movilidad de espermatozoides; pero estos cambios son reversibles luego de discontinuado el tratamiento.
No sólo los antidepresivos con efecto serotoninérgico pueden tener un efecto a nivel de la esfera sexual, también los antidepresivos no serotoninérgicos fueron asociados con un retardo eyaculatorio. Un estudio multicéntrico que comparó varios antidepresivos IRSS halló que la paroxetina causaba un mayor retardo eyaculatorio y/o impotencia que la fluoxetina sertralina o fluvoxamina (Montejo-González et al., 1997). Es- tos autores describieron que la disfunción sexual inducida por los IRSS era un fenómeno dosis-dependiente. Waldinger et al. (2001, 2003) reportó que 20 mg de paroxetina por día tenían más efecto que 20 mg de citalopram para el retraso eyaculato- rio. El estudio de Kennedy et al. (2000), de tipo prospectivo, comparó paroxetina, sertralina, venlafaxina y moclobemida; hallaron que los hombres presentaban mayor afectación en la fase del deseo o libido que las mujeres, pero sin diferencias de género en las demás fases. Tanto la venlafaxina como la moclobemina y la duloxetina presentaron menor incidencia de disfunción sexual que los IRSS (en especial paroxetina) (Delgado et al., 2005).
Los antidepresivos IRSS, en la fase del deseo, disminu-
yen la libido por la estimulación de receptores 5HT2A en los centros mesocorticales y mesolímbicos relacionados con el placer sexual que generan una hipoactividad de las neuronas dopaminérgicas mesolímbicas a nivel de la corteza prefrontal y del núcleo accumbens, lo cual genera una ausencia en la estimulación del circuito de recompensa y de los núcleos hipotalámicos. A nivel de la fase de excitación puede afectar la respuesta genital, pero en la fase del orgasmo inhiben los reflejos espinales de la eyaculación y orgasmo mediante la estimulación de receptores 5HT2A y 5HT2C en la médula espinal porción dorsal.
Los antidepresivos IRSS más estudiados para el tratamiento de los trastornos parafílicos son la sertralina y la fluoxetina, y demostraron eficacia farmacoclínica en altas dosis (Kakfa y Prentky, 1992; Garcia et al, 2013; Assumpcao et al., 2014). Los consensos de expertos recomiendan su uso clínico en los trastornos parafílicos leves o moderados en población adolescente, en los casos que se presenta comorbilidad con trastornos obsesivos, del control de los impulsos y depresivos (Thibaut et al, 2010; Assumpcao et al., 2014). Asimismo, existen asociaciones internacionales y protocolos de abordaje terapéutico que los recomiendan como intervención para disminuir la excitación sexual.
La base para su uso en estos trastornos se basa en su modu- lación de las fases del ciclo sexual descriptas, principalmente en el deseo sexual (libido) y en las conductas impulsivas y compulsivas asociadas con estos trastornos.
Los estudios clínicos y preclínicos vincularon a las conductas agresivas, impulsivas y violentas con una deficiencia del neurotransmisor serotonina (5-HT). Por ende, estos sujetos podrían beneficiarse con tratamientos farmacológicos dirigidos a la inhibición de los transportadores de 5-HT (como los IRSS), a la activación de los receptores 5-HT1A (como lo realiza la buspirona) o al bloqueo de los receptores 5HT2A (como lo generan los antipsicóticos de segunda generación). Se postuló que el tratamiento agudo con estos fármacos induciría
cambios fásicos en la función serotoninérgica que estarían asociados con sus efectos anti-agresivos transitorios. Por su parte, el tratamiento crónico con estas moléculas promovería cambios neuroadaptativos que no han sido todavía descriptos totalmente como la desensibilización del autoreceptor que se asocia con la aparición de efectos terapéuticos. Los trabajos publicados también reportaron que la activación de los receptores 5HT1A, 5HT1B, 5HT2A/C en áreas mesocorticales y límbicas reduce las conductas agresivas, así como el agonismo de los receptores 5HT1A y 5HT1B en la corteza de la región pre- frontal medial incrementaría la conducta agresiva (Takahashi A, et al., 2012).
La serotonina y su receptor no son los únicos implicados, sino blancos diana que tienen funciones asociadas y limitan- tes para que se puedan generar este tipo de conductas; no se deben interpretar los resultados de las investigaciones desde un punto de vista determinístico ni menos aún lineal dado que existen muchos factores para tener en cuenta (neurodesarro- llo, medio ambiente, niveles cognitivos, recursos interperso- nales, socialización, entre otros)
Cabe destacar que, pese a la generalización del uso de los antidepresivos IRSS, al antidepresivo tricíclico clomipramina también fue utilizado con éxito clínico y su eficacia fue atri- buida a la significativa inhibición en la recaptación serotoni- nérgica (Osborn & Wise, 2005).
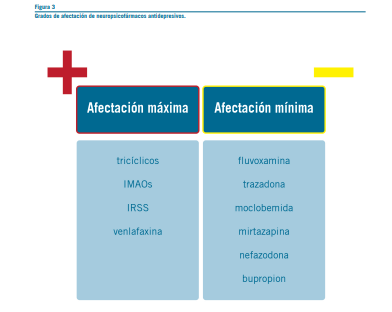
No todos los neuropsicofármacos antidepresivos afectan por igual la función sexual. En el gráfico 3 se los divide en dos grupos.
• Psicoestimulantes
Un estudio abierto de 3 años de duración que utilizó el psicoestimulante metilfenidato, bloqueante de la recaptación de noradrenalina y dopamina a nivel de la corteza prefrontal, como coadyuvante en el tratamiento con antidepresivos IR- SSs, reportó una disminución en la signo-sintomatología del trastorno parafílico y en las escalas implementadas, así como en el tiempo empleado durante el día para la realización de dicho comportamiento (Guay, 2009).
• Antipsicóticos de segunda generación
Este grupo de fármacos se asociaría con alteraciones en la
función sexual por medio del bloqueo 5HT2A a nivel postsináp- tico y debido al aumento de la prolactinemia. En el estudio CATIE los pacientes con esquizofrenia presentaron similares tasas de alteraciones sexuales con el uso de los antipsicóticos de primera y de segunda generación, sin distinción de los ni- veles de prolactina. Un metaanálisis reportó la incidencia de alteraciones sexuales y evidenció que la tioridazina y clozapi- na fueron los que registraron mayores alteraciones, mientras que la ziprasidona y la quetiapina las menores. El aripiprazol y la ziprasidona causan el efecto más leve a nivel de la fase del deseo sexual, mientras que el aripiprazol y la quetiapina tienen el menor efecto en la fase del orgasmo (Serretti y Chie- sa, 2011).
• Estabilizadores del ánimo
Existen reporte de caos que describen la anorgasmia y alte- raciones en la fase de la libido, asociadas con el uso de dival- proato de sodio, efecto de tipo dosis dependiente, usualmente junto con el uso de otras medicaciones y sin respuesta con efecto clínico positivo frente a las reducciones en la dosis. Un estudio con más de 100 pacientes determinó que el uso de litio como monoterapia se asociaba con un 14 % de disfun- ciones sexuales, pero si se lo asociaba con benzodiacepinas la incidencia de las disfunciones llegaba al 49 % (Ghadirian et al., 1992).
Los efectos adversos secundarios inciden tórpidamente en
la adherencia terapéutica de los pacientes y pueden motivar el abandono del tratamiento. Asimismo, así existiera un fármaco sin efectos secundarios, ello no constituiría el éxito terapéu- tico por la finalización de los trastornos parafílicos y menos aún los actos parafílicos, dado que entre los componentes del trastorno se imbrican otros factores más allá de los neurobio- lógicos que son igual de importantes.
• Tratamiento hormonal
Las terapias con estrógenos ya no son utilizadas, pese a su eficacia para el tratamiento de los trastornos parafílicos, debi- do al riesgo de cáncer de mama y episodios tromboembólicos
entre otros efectos adversos.
El deseo sexual se asocia en gran medida con los niveles de concentración de andrógenos, así como otras fases de la respuesta sexual humana como la erección en mucho menor medida. Pero la testosterona como la dihidrotestosterona son andrógenos implicados en la conducta sexual y también en las conductas agresivas. Se han reportado niveles elevados de testosterona en ofensores sexuales. Los antiandrógenos esteroideos reducen los niveles de testosterona mediante un feed-back inhibitorio del eje hipotálamo-pituitario e inhibición de la liberación de la hormona luteinizante (LH en inglés). El tratamiento basado en antiandrógenos incluye el acetato de ciproterona, progesterona, acetato de medroxiprogesterona, el factor liberador de la hormona luteinizante (LHRH) y los aná- logos del factor liberador de hormona gonadotrofina (GNRH) como el acetato de leuprolide (Krueger & Kaplan, 2002; Hall & Hall, 2007; Briken et al., 2003, 2004; Rosler & Witztum, 1998). Estos fármacos actúan mediante la reducción de los niveles de testosterona, con disminución del deseo sexual y de la respuesta excitatoria.
La medroxiprogesterona (acetato de medroxiprogestero- na) fue la primera en ser estudiada para los pacientes con trastornos parafílicos. Además de la inhibición hipotalámi- co-pituitaria, incrementa el metabolismo y la excreción de la testosterona por medio de la activación de la enzima testos- terona-5-a-reductasa a nivel hepático durante el proceso de eliminación, no obstante, altera el proceso de síntesis de la testosterona a nivel testicular. La medroxiprogesterona se une a la globulina fijadora de testosterona, por lo cual modula el desligamiento de la testosterona de la proteínaligadora de este esteroide para hacerla disponible y así disminuye la tes- tosterona libre. La dosis oral utilizadaen los reportes de ca- sos, a doble ciego y cruzados, osciló entre 100 y 400 mg vía oral, pero la práctica clínica fue más favorable con el uso de administración intramuscular de liberación controlada (300- 400 mg) cada 10 días. Demostró eficacia en la reducción del deseo sexual, de las conductas sexuales desviadas llevadas en actocomo de las fantasías sexuales desviadas luego de 1 a 2 meses de tratamiento (Thibaut et al, 2010; Assumpcao et al., 2014). Este fármaco fue discontinuado en Europa debido a la relación entre beneficios y riesgos, justamente uno de los efectos adversos graves es la embolia pulmonar.
El acetato de ciproterona es un esteroide sintético que se une a los receptores cerebrales de andrógenos y actúa como un inhibidor competitivo de la testosterona. Es uno de los productos más utilizados para el control hormonal de los tras- tornos parafílicos. Su mecanismo de acción se basa en la inhibición de la liberación de la hormona liberadora de gonadotropina (GnRH) y de la hormona luteinizante (LH), así como un efecto de bloqueo específico de los andrógenos. Genera una desregulación de los receptores de andrógenos que bloquean la recaptación intracelular de la testosterona, impidiendo su unión a los receptores y bloqueando el metabolismo intracelular de los mismos. Tiene distintas formas farmacéuticas y de dosificación: intramuscular de liberación controlada (200-400 mg/semana) cada 2 semanas, u oral 50-200 mg diarios. Según Freund (1980), 50 mg diarios generan una reducción del impulso sexual, 100 mg diarios producen una reducción significativa en el 80 % de los casos y sólo el 20 % de los pacientes requieren dosis de 200 mg diarios. Presentó eficacia a las 4-12 semanas por medio de la reducción de las fantasías sexuales y de la actividad en conductas parafílicas en el 80-90 % de los sujetos reclutados de distintos estudios (Thibaut et al., 2010; García et al., 2013). En el caso de los sujetos que recayeron en las conductas, los investigadores lo asociaron con un mal cumplimiento del tratamiento.
Tanto con el acetato de medroxiprogesterona como el deciproterona reducen los niveles de testosterona de forma efectiva, pero esto no se asocia correlativamente con igual magnitud con la disminución del impulso sexual, de las fantasías parafílicas y menos aún del pasaje al acto. La eficacia farmacoclínica de ambos fármacos no está totalmente funda- mentada puesto que no hay suficientes estudios a doble ciego y controlados, excepto el de Bradford (1998); se destaca que el poder realizar con metodología a doble ciego controlado contra placebo este tipo de estudios en una población con trastorno parafílico presenta muchas limitaciones desde lo éti- co dado quienes reciban el placebo tienen mayor probabilidad de pasaje al acto y/o delinquir relacionado con su ideación parafílica.
Los análogos del factor liberador de hormona gonadotrofina provocan un down regulation de la secreción de hormona luteinizante y de la hormona foliculoestimulante por medio de la unión a los receptores pituitarios. Durante la primera semana de tratamiento, puede inducir un aumento del comportamiento parafílico debido a la liberación de hormona luteinizante y el aumento inicial de testosterona. La ciproterona ha sido utilizada para el aumento de testosterona. El uso crónico de este tipo de moléculas provoca una rápida desensibilización de los receptores de GnRH, debido a la disminución de hormona luteinizante. Los análogos de la GnRH incluyen otras moléculas, algunas son inyectables y pueden ser administradas mensualmente, excepto la triptorelina que se administra trimestralmente.
Un estudio de 2012 realizado de manera multicéntrica en hospitales psiquiátricos, basado en estudios clínicos a doble ciego llevados a cabo en Alemania, sugirieron que la combi- nación de triptorelina con psicoterapia disminuía las fantasías sexuales desviadas, impulsos y conductas en pacientes con parafilias (Briker y Berner, 2012). La duración del tratamien- to con análogos de la GnRH permaneció abierta. Las guías de tratamiento sugirieron una mínima duración del tratamiento de 3 a 5 años para los casos de trastornos parafílicos severos con alto riesgo de violencia sexual (Thibaut et al., 2010; Gar- cía y Thibaut, 2011). La eficacia fármaco-clínica se mantuvo siempre que la terapia antiandrogénica se mantuviese con adherencia. El mayor seguimiento registrado fue a 7-10 años (García et. al., 2013).
Debido a que el tratamiento hormonal con antiandrógenos genera hipoandrogenismo, se producen efectos colaterales que incluyen ginecomastia, feminización, astenia, sofocos, disminución del vello en el cuerpo y la cara, disminución del volumen testicular, aumento de peso, cambios en la tensión arterial, alteraciones en la tolerancia a la glucosa, dolor eyaculatorio episódico, síntomas depresivos, desmineralización ósea y dolor en el sitio de la inyección. Estos efectos adversos requieren tratamiento con suplementos de calcio o de vitamina D; los bifosfonatos son efectivos para tratar las alteraciones óseas en pacientes que reciben antiandrógenos. Las contra- indicaciones para el uso de antiandrógenos incluyen alteraciones tromboembólicas, pacientes en etapa de la pubertad, embarazadas, mujeres en periodo de amamantamiento, hiper- tensión no controlada, enfermedad renal y/o cardíaca, altera- ciones hepáticas, depresión severa, osteoporosis, enfermeda- des de la glándula pituitaria y alergia al compuesto. Algunas investigaciones han hallado que las terapias complementarias con pequeñas dosis de testosterona mejoran la osteoporosis y la disfunción eréctil en los pacientes, sin recaídas o reacti- vación de los pensamientos parafílicos (Briken et. al, 2003).
Las guías de tratamiento recomiendan previamente los chequeos del peso corporal, tensión arterial, electrocardiograma, densidad mineral ósea, hemograma y hepatograma completos, glucosa, función renal, dosaje de FSH, LH, testosterona y prolactina. Los síntomas depresivos deben ser evaluados mensualmente y las enzimas hepáticas trimestralmente, los demás valores semestralmente, excepto los niveles de testos- terona que deberán ser evaluados con menor frecuencia para valorar la adherencia al tratamiento (Thibaut et al., 2010).
Thibaut propuso un algoritmo de tratamiento farmacológico para los trastornos parafílicos basado en las historias clínicas de pacientes tratados por su grupo de trabajo, y sobre la base de variables significativas de seguimiento como la respues- ta y adherencia al tratamiento, el riesgo de violencia sexual e intensidad de la fantasía parafílica y/o pasaje al acto. El algoritmo usa la clasificación por niveles del 1 al 6: en nivel 1 recomienda la terapia cognitivo-conductual para pacientes con bajo riesgo de violencia sexual; en nivel 2 recomienda el tratamiento con altas dosis de antidepresivos IRSS para los casos de trastornos parafílicos moderados o aquellos que no respondieron a la terapia cognitivo-conductual; del nivel 3 al nivel 6 recomiendan el tratamiento hormonal. En todos los niveles, el grupo de Thibaut recomienda para todos los tras- tornos parafílicos el tratamiento con psicoterapia.
• Otros fármacos
Junto con los antidepresivos y/o la terapia hormonal, existen otras moléculas que pueden ser útiles en algunos pacientes con trastorno parafílico.
Los fármacos antiepilépticos, como el topiramato, pueden ser beneficiosos para el tratamiento de este trastorno, en especial para el fetichismo (Shiah et al., 2006), como también para otros trastornos parafílicos no especificados según el DSM 5 que se caractericen por conductas adictivas en la esfera sexual y compulsivas (Fong et al., 2005; Khazaal y Zulli- no, 2006). El mecanismo de acción se basaría en el bloqueo de los canales de sodio voltaje-dependientes, la potenciación gabaérgica (inhibitoria) y el bloqueo de los receptores glutamatérgicos para AMPA/kainato que son excitatorios.
En la publicación de Rubenstein y Engel sobre reporte de caso, utilizaron litio combinado con antidepresivo tipo IRSS para el tratamiento de un paciente con trastorno parafílico de tipo fetichista luego de una mala respuesta con el uso de sólo antidepresivos que también había sido tratado con ansiolíti- cos y antipsicóticos (Rubenstein y Engel, 1996). Si bien los autores descartaron la presencia de trastornos del espectro bi- polar, adicionaron el litio para potenciar los efectos del IRSS. La respuesta obtenida fue favorable en cuanto a la disminu- ción y eliminación de las conductas parafílicas, sin efecto en las fantasías y sin efectos adversos significativos. Los autores describieron que la adición del litio sobre el mecanismo del IRSS actuaría como un sinergismo en dicho bloqueo de la recaptación, con efecto a nivel de otras vías químicas como la dopaminérgica y mediante la depleción del inositol en las zonas donde existiría una mayor concentración de neurotrans- misores basado en las consideraciones neurobiológicas del trastorno evidenciadas por estudios funcionales.
Las medicaciones simpático miméticas también serían útiles en los pacientes con trastorno parafílico que presenten comorbilidad con un trastorno por déficit de atención (Ru- benstein y Engel, 1996; Kafka y Hennen, 2000).
También los fármacos con potente acción anticolinérgica y/o bloqueante de los receptores a1 alteran el proceso de ex- citación sexual.
Una publicación donde se utilizó naltrexona, un antagonista opiáceo, fue útil para el abordaje de un grupo de adolescentes con causas relacionadas con ofensas sexuales. Este fármaco bloquea los receptores opioides mu y de esta forma evita que otro ligando (exógeno o endógeno) genere efectos placenteros con la reducción de conductas compulsivas por disminución de la ideación previa a éstas. La eficacia postulada fue asocia- da con la disminución referida de las fantasías sexuales y de la actividad masturbatoria (Ryback, 2004). Fedoroff publicó otro caso con buena respuesta farmacoclínica de un paciente con trastorno parafílico fetichista tratado con buspirona, un ansiolítico no benzodiacepínico (Fedoroff, 1988).
En el caso de los fármacos que actúan mediante el antago- nismo dopaminérgico, como la clorpromazina que tiene varios reportes, los resultados han sido contradictorios.
Varela y Black reportaron un caso que respondió positivamente con carbamacepina y clonazepam para un cuadro de trastorno parafílico de pedofilia. La carbamacepina modifica la excitabilidad de la membrana por su acción sobre los cana- les iónicos de sodio, potasio y calcio, y según estudios de neuroimagen funcional en este trastorno existe una hiperfunción anómala de zonas cerebrales subcorticales en respuesta a imágenes de niños. Presentó respuesta farmacoclínica en sus síntomas de ansiedad y disforia asociada con las conductas pedófilas, y el paciente no presentaba ningún otro trastorno comórbido. Los pensamientos y conductas fueron disminuyendo y pudo mantenerse con buena performance hasta 1 año (cuando fuera publicado) (Varela y Black, 2002).
Si bien los casos reportados son individuales o de pequeños grupos, sirven como una evidencia para delinear el tratamien- to conjunto neuropsicofarmacológico y psicoterapeútico. Se necesita mucha más investigación basada en evidencias, con formatos de estudios clínicos controlados y aleatorizados que provean más información sobre los beneficios y limitaciones de las intervenciones neuropsicofarmacológicas en los trastor- nos parafílicos, toda vez que debemos partir de la premisa que son una de las distintas intervenciones para abordar clínica- mente el trastorno dentro del equipo interdisciplinario.
Estrategias terapéuticas no farmacológicas
Estas intervenciones incluyen a la terapia cognitivo-con- ductual con sus distintas técnicas de abordaje según fase, gravedad y tipología de la conducta. Dado que no es el ob- jetivo del presente artículo desarrollar estas estrategias, sólo se mencionará que usualmente se desarrollan en grupo y los profesionales deben evaluar profundamente características de la personalidad de los sujetos. Se debe detectar la comorbili- dad con trastornos de personalidad tipo narcisista y límite, así como aquellos con rasgos psicopáticos. En el caso de sujetos con rasgos psicopáticos, los profesionales deberán conformar los grupos terapéuticos donde no deberían estar en el mismo grupo dos sujetos con esta comorbilidad para que se pueda atenuar la tendencia oposicionista, disruptiva y manipuladora de éstos.
El objetivo general de esta terapia consiste en modificar
el interés sexual parafílico del sujeto y sustituirlo por otros mediante “intervenciones de reacondicionamientos” con dife- rentes técnicas, así como la detección de factores de riesgo, comprender qué busca el sujeto con la conducta parafílica y qué interés satisface, y la detección de señales de alerta.
Históricamente han sido descriptas otras intervenciones, como las castraciones físicas (orquiectomía o neurocirugía estereotáxica) y químicas, que no sólo afectan derechos hu- manos de los sujetos y son antiéticas, sino que pueden tener efecto criminógeno. Hay casos descriptos de sujetos que, al no poder utilizar sus genitales para satisfacer sus impulsos violentos, utilizan otros objetos e instrumentos y realizan con- ductas más violentas. Estos datos comprueban que las inter- venciones biológicas no tienen una respuesta completa para el trastorno puesto que la génesis y bases de este son de tipo multifactorial.
Conclusiones
El trastorno parafílico es una entidad clínica con múltiples atravesamientos en su etiología y evolución que requieren un abordaje multidisciplinario. Su abordaje en contexto asistencial interpela a los profesionales a realizar una profunda se- miología del trastorno valorando antecedentes médicos, personales y medioambientales, así como posibles indicadores de violencia y criminalidad. Es fundamental una correcta y minuciosa semiología del trastorno para luego poder evaluar indicadores de respuesta a las intervenciones clínicas duran- te su evolución. Las intervenciones neuropsicofarmacológicas en el trastorno parafílico presentan bajo nivel de evidencia científica, son diseñadas para cada paciente en función de su signo-sintomatología y son una de las distintas intervenciones (psicoeducativa, psicoterapéutica) con las que se puede abordar esta patología.
Bibliografía
- Abel GG, Osborn C. The Paraphilias: The Ex- tent and Nature of Sexually Deviant and Crimi- nal Behavior. Psychiatric Clinics of North Ameri- ca 1992; 15(3):675-87.
- Assumpcao AA, Garcia FD, Garcia HD, Bra- dford JM, Thibaut F. Pharmacologic treat- ment of paraphilias. Psychiatr Clin North Am 2014;37(2):173-81.
- Bradford JM (1998). Treatment of men with paraphilia. NEJM 338(7):464-465.
- Briken P, Berner W. P278 study group. Dou-
ble-blind, controlled, clinical trial planned in Germany to investigate the efficacy of psycho- therapy combined with triptorelin in adultmale patients with severe pedophilic disorders: pre- sentation of the study protocol. Isr J Psychiatry Relat Sci 2012;49(4):306-13.
- Briken P, Hill A, Berner W. A relapse in pe- dophilic sex offending and subsequent sui- cide attempt duringluteinizing hormone-re- leasing hormone treatment. J Clin Psychiatry 2004;65(10):1429.
- Briken P, Hill A, Berner W. Pharmacotherap of paraphilias withlong-acting agonists of lutei-
nizing hormone-releasing hormone: a system aticreview. J Clin Psychiatry 2003;64(8):890-7.
- Briken P, Kafka MP. Pharmacological treat- ments for paraphilic patients and sexual offen- ders. Curr Opin Psychiatry 2007;20(6):609-13.
- Clayton AH, Montejo AL. Major depressive di- sorder, antidepressants, and sexual dysfunction. J Clin Psychiatry 2006;67(Suppl 6):33-7.
- Delgado PL, Brannan SK, Mallinkrodt CH, et al. Sexual function in gassessed in 4 dou- ble-blinded placebo- and paroxetine-controlled trials of duloxetine for major depressive disorder. J Clin Psychiatry 2005;66:686-92.
- Fedoroff JP. Buspirone hydrochloride in the- treatment of transvestic fetischism. J Clin Psy- chiatry 1988;49(10):408-9.
- Fong TW, de la Garza R, Newton TF. A case report of topiramate in the treatment of nonpara- philic sexual addiction. J Clin Psychopharmacol 2005;25(5):512-4.
- Freund K (1980). Therapeutic sex drive reduc- tion. Act Psychiatric Scand 62 (Suppl 287).
- Freund K, Seto MC. Preferential rape in the theory of courtship disorder. Arch Sex HYPER- LINK “https://link.springer.com/journal/10508”- Beh 1998; 27: 433–43.
- Garcia FD, Delavenne HG, AssumpcaoAde F, Thibaut F. Pharmacologic treatment of sex of fenders with paraphilic disorder. Curr Psychiatry Rep 2013;15(5):256.
- Garcia FD, Thibaut F. Current concepts in the pharmacotherapy of paraphilias. Drugs 2011;71(6):771-90.
- Ghadirian AM, Annable L, Bélanger MC. Lithium, benzodiazepines and sexual func- tion in bipolar patients. Am J Psychiatry 1992;149:801-5.
- Guay DR. Drug treatment of paraphilic and non paraphilic sexual disorders. Clin Ther 2009;31(1):1-31.
- Hall RC, Hall RC. A profile of pedophilia: de- finition, characteristics of offenders, recidivism, treatment outcomes, and forensicissues. Mayo Clin Proc 2007;82(4):457-71.
- Hu XH, Bull SA, Hunkeler EM, et al. Incidence and duration of side-effects and thoserated as bother some with selective serotonin reuptake- inhibitor treatment for depression: a patient re- port versus physician estimate. J Clin Psychiatry 2004;65:959-65.
- Kafka MP, Hennen J. Psychostimulantaugmen- tation during treatment with selective serotonin reuptake inhibitors in men with paraphilia-re- lated disorders: a case series. J Clin Psychiatry 2000;61(9):664-70.
- Kafka MP, Prentky R (1992). Fluoxetine treat- ment of non paraphilic sexual addictions and pa- raphilias in men. J Clin Psychiatry 53(10):351-8.
- Kennedy SH, Eisfeld BS, Dickens SE, et al. Antidepressant-induced sexual dysfunctiondu- ring treatment with moclobemide, paroxetine, sertraline and venlafaxine. J Clin Psychiatry 2000,61:276-81.
- Khazaal Y, Zullino DF. Topiramate in thetreat- ment of compulsive sexual behavior: case report.
BMC Psyciatry 2006;6:22.
- Krueger RB, Kaplan MS. Behavioral and psy- chopharmacological treatment of the paraphi- lic and hypersexual disorders. J PsychiatrPract 2002;8(1):21-32.
- Marshall WL. Diagnostic issues, multiple para- philias, and comorbid disorders in sexual offen- ders: The irincidence and treatment. Aggression and Violent Behavior 12 (2007) 16–35.
- Mews A, DiBella L, Purver M. Impacte va- luation of the prison-based Core Sex Offender Treatment Program. Ministry of Justice Analytic Series. London: Crown; 2017.
- Montejo AI, Llorce G, Izquierdo JA, Rico-Vi- llademoros F, et al. Incidence of sexual dys- function associated to different antidepressan- tagents. A prospective and multicentric study in 1022 patients. J Clin Psychiatry 2001;62(Suppl 3):10-21.
- Naylor AM. Endogenous neurotransmitters me- diating penile erection. Br J Urol 1998;81:424- 31.
- Osborn C, Wise TN. Hand book of sexual dys- function. Boca Raton: Taylor & Francis; 2005.
- Redouté J, Stoléru S, Grégoire MC, Costes N, Cinotti L, Lavenne F, Le Bars D, Forest MG, Pujol JF. Brain Processing of Visual Sexual Sti- muli in Human Males. Human Brain Mapping 2000;11:162–177.
- Rosler A, Witztum E. Treatment of men with paraphilia with a long-actinganalogue of go- nadotropin-releasing hormone. N Engl J Med 1998;338(7):416-22.
- Rubenstein EB, Engel NL. Successful treat- ment of travestic fetischism with sertraline and lithium. J Clin Psychiatry 1996;57(2):92.
- Ryback RS. Naltrexone in the treatment of adolescent sexual offenders. J Clin Psychiatry 2004;65(7):982-6.
- Serreti A, Chiesa A. A meta-analysisof se- xual dysfunction in psychistric patients ta- king antipsychotics. Int Clin Psychopharmacol 2011;26:130-140.
- Shiah IS, Chao CY, Mao WC Chuang YJ. Treat- ment of paraphilic sexual disorder: the use ofto- piramate in fetischism. Int Clin Psychopharma- col 2006;21(4):241-3.
Takahashi A, Quadros IM, Almeida RMM de, Miczek KA. Behavioral and Pharmacogenetics of Aggressive Behavior. Curr Top Behav Neurosci 2012; 12: 73–138.
- Thibaut F, de la Barra F, Gordon H, Cosyns
P, Bradford JM. WFSBP Task Forceob Sexual Disorders. The world federation of societies of biological psychiatry (WFSBP) guidelines for the biological treatment of paraphilias. World J Biol Psychiatry 2010;11(4):604-55.
- Varela D, Black DW. Pedophilia treated with- carbamazepine and clonazepam. Am J Psychia- try 2002;159(7):1245-6.
- Waldinger MD, Zwinderman AH, Oliver B. An- tidepressants and ejaculation: a double-blind, randomized, fixed-dose study with mirtazapi- ne and paroxetine. J Clin Psychopharmacol 2003;23:467-70.
- Waldinger MD, Zwinderman AH, Oliver B. SS- RIs and ejaculation: a double-blind, randomized, fixed-dose study with paroxetine and citalopram. J Clin Psychopharmacol 2001;21:556-60.
- Wittels, F Sigmund Freud: su personalidad, su enseñanza y su escuela. Londres, 1924, p. 17.







No comments! Be the first commenter?