Incidencia de neutropenia en pacientes que iniciaron tratamiento con clozapina entre julio de 2022 y julio de 2023 asistidos en el hospital Vilardebó
Resumen
Esta monografía examina la incidencia de neutropenia en pacientes tratados con clozapina entre julio de 2022 y julio de 2023 en el Hospital Vilardebó. Dada la potencial severidad de la neutropenia como efecto adverso del tratamiento con clozapina, este estudio busca establecer una comprensión clara de su prevalencia, los factores de riesgo asociados y el registro de su uso en nuestro medio. Se analizó una cohorte de 81 pacientes, evaluando parámetros como edad, sexo, dosificación de clozapina, y duración del tratamiento. Los hallazgos indican que la incidencia de neutropenia sigue siendo una preocupación significativa, particularmente en las primeras 18 semanas de tratamiento. Los resultados sugieren la necesidad de estrategias de monitoreo más rigurosas y adaptadas para minimizar el riesgo de complicaciones hematológicas severas. Este estudio contribuye a la literatura existente al proporcionar datos actualizados sobre la incidencia de neutropenia en un contexto clínico específico, y enfatiza la importancia de la vigilancia continua y la intervención temprana.
Palabras clave
Clozapina – Neutropenia – Esquizofrenia resistente – Efectos adversos hematológicos – Monitoreo de seguridad.
Introducción y marco teórico
La clozapina es el antipsicótico de elección para el trata- miento de la esquizofrenia resistente. Es un antipsicótico de segunda generación aprobado por la FDA para el tratamiento
de las disquinesias tardías, los síntomas psicóticos de la en- fermedad de Parkinson y las conductas suicidas en pacientes con esquizofrenia (1–49).
El concepto de esquizofrenia resistente fue introducido por
Kane para definir aquellos pacientes que no presentaban me- joría sintomática a pesar de varios intentos de tratamiento farmacológico; este la definió como aquella enfermedad en la que existieron 3 períodos de tratamiento en los 5 años prece- dentes con antipsicóticos (de por lo menos 2 clases diferentes de químicos) a dosis equivalentes o superiores a 1000 mg/día de Clorpromazina por un periodo de 6 semanas, cada uno sin alivio sintomático significativo (4).
Luego este concepto sufrió diferentes interpretaciones se- gún diferentes manuales y estudios clínicos. Sin embargo, actualmente existe consenso en determinar la resistencia después de la falta de respuesta a dos pruebas terapéuticas con antipsicóticos a dosis óptimas o máximas durante un pe- ríodo de entre 4 y 8 semanas, siendo al menos uno de ellos un antipsicótico de segunda generación o atípico y se estima que afecta a aproximadamente el 30% de los portadores de esquizofrenia (5).
La tasa de prescripción de un fármaco se define como el número de dosis diarias administradas cada 1000 habitantes en un período de un año. Según la Organización Mundial de la Salud (OMS), para la clozapina es de 300 mg/día. Otra forma de valorar su frecuencia de prescripción es mediante la cantidad de personas que la reciben cada 100.000 habitan- tes. En este sentido, en 2014 Finlandia presentó una tasa de prescripción de 189 cada 100.000 habitantes, siendo el país con la tasa más alta, mientras que los valores mundiales se ubican en el rango de 100 a 500 pacientes por cada 100.000 habitantes (6).
Si bien la eficacia de la clozapina es superior a la de otros antipsicóticos [4], no se considera un tratamiento de primera línea debido a su extenso perfil de efectos adversos. Entre los efectos adversos más preocupantes se encuentran los cardía- cos, como la miocarditis, y los hematológicos, como la neu- tropenia. La incidencia de neutropenia inducida por clozapina varía en diferentes estudios, con tasas que oscilan entre el 0,1% y el 3,8% (7, 8).
Existen diferentes valores de referencia para definir la neu- tropenia, que varían según las regiones. En Estados Unidos (EE.UU.), se clasifica en leve, moderada y severa, mientras que en Reino Unido se utiliza una clasificación de verde a rojo, siendo las clasificaciones análogas en cuanto a la grave- dad. Los puntos de corte en EE. UU. son: neutropenia leve de 1000 a 1499 neutrófilos por mm3, neutropenia moderada de 500 a 999 neutrófilos por mm3 y neutropenia severa menor a 500 neutrófilos por mm3. En cambio, en Reino Unido, los valores para una neutropenia leve (verde) son de 2500 o más neutrófilos por mm3, una neutropenia moderada (ámbar) se encuentra en el rango de 2000 a 2499 neutrófilos por mm3 y una neutropenia severa (rojo) implica un número menor a 1500 neutrófilos por mm3. En Uruguay, contamos con una guía del Hospital Vilardebó, centro de referencia de pacientes
con patología mental del país, que se ajusta a los valores es- tadounidenses de neutropenia (7).
En cuanto al momento de aparición de la agranulocitosis, el 80% de los casos ocurren en las primeras 18 semanas, con una disminución de la tasa de eventos al 0,7% en el primer año y al 0,07% en el segundo año (9). Sin embargo, existen pruebas contradictorias, como el metaanálisis realizado en 2019 que sugiere un aumento del riesgo después del primer año de tratamiento (10).
En algunos estudios que compararon la incidencia de neu- tropenia en pacientes tratados con clozapina y en pacientes tratados con otros antipsicóticos diferentes a la clozapina, se observó que la tasa de neutropenia en pacientes tratados con clozapina no fue significativamente mayor que en aquellos tratados con otros fármacos. Estos resultados sugieren que el riesgo elevado de neutropenia en comparación con otros antipsicóticos podría no estar respaldado adecuadamente, y que existe el mismo riesgo o incluso mayor para otros antip- sicóticos.
Existen otros factores asociados a la presencia de neutrope- nia, entre ellos el sexo femenino, la edad avanzada y el uso concomitante de valproato de sodio, lo cual se ha asociado con un aumento en la incidencia del evento (11, 12).
En un estudio, la incidencia de neutropenia fue similar en pacientes con esquizofrenia, ya sea que recibieron clozapina o no, lo que sugiere que podría estar asociada a otros facto- res propios de la enfermedad y no necesariamente al uso del fármaco (13).
La etiología de la neutropenia inducida por clozapina aún no está completamente dilucidada (14). Se estima que hay un mecanismo complejo con una predisposición determinada por la mutación de los genes HLA-DQB1, HLA-B y SLCO1B3/ SLCO1B7 (15, 16), que están involucrados en la respuesta inmune del individuo. Por esta causa, se infiere que la neu- tropenia inducida por clozapina tiene una causa autoinmune mediada por la acción de los linfocitos T, en contraposición a una causa tóxica (17). Se estima que todos estos factores contribuyen a que la prescripción de clozapina en nuestro país esté por debajo de los estándares establecidos por la OMS (18).
Las diferentes pautas y la necesidad de realizar estudios hematológicos pueden generar una prescripción menor debido a una percepción de un mayor riesgo de efectos adversos que no se corresponde con la bibliografía internacional (19).
Existen pautas preestablecidas para el seguimiento hema- tológico durante el uso de clozapina con el objetivo de guiar a los técnicos en la monitorización de la aparición de neutrope- nia. En el año 2015, el Ministerio de Salud Pública (MSP) de nuestro país elaboró un protocolo que determina la necesidad
de realizar un hemograma en los 10 días previos al inicio del tratamiento con clozapina, seguido de hemogramas semanales hasta la semana 18. Posteriormente, se recomienda realizar he- mogramas cada 4 semanas mientras dure el tratamiento (20).
Adicionalmente, en el año 2018, se desarrolló en el Hospi- tal Vilardebó un protocolo práctico para el uso de clozapina. Este protocolo involucró a un equipo multidisciplinario con- formado por servicios de medicina, psiquiatría, enfermería, laboratorio y farmacia del hospital, con el objetivo de brindar sugerencias para el inicio, seguimiento y discontinuación del tratamiento con clozapina. Según este protocolo, se reco- mienda realizar hemogramas semanales durante las primeras 26 semanas, seguidos de hemogramas quincenales durante las siguientes 26 semanas, y luego hemogramas mensuales mientras se mantenga el tratamiento (21).
Existen ejemplos de situaciones en las que se ha modifica- do el estándar de seguimiento hematológico con resultados interesantes, con el objetivo de minimizar el contagio en el contexto del COVID-19. En el sur de Inglaterra, se prolongó el intervalo de tiempo entre las monitorizaciones hematoló- gicas de pacientes en tratamiento con clozapina de 4 a 12 semanas. Un estudio publicado en 2023, cuyo objetivo fue determinar el impacto de este cambio en la pauta, no encon- tró evidencia de un aumento en la incidencia de neutropenia severa en comparación con el grupo de control (22).
Objetivos
Generales
Determinar la incidencia de neutropenia en las primeras 26 semanas de iniciado el tratamiento con clozapina en pacientes cuyo tratamiento fue iniciado durante el periodo comprendido entre el 1/7/2022 y el 30/6/2023 en el Hospital Vilardebó.
Específicos
- Determinar si existe una relación entre la dosis de Cloza- pina y la incidencia de neutropenia.
- Precisar si existe una relación entre el tiempo de evolu- ción del tratamiento y la aparición de neutropenia.
- Evaluar la incidencia de pacientes cuyo tratamiento con clozapina fue suspendido por la presencia de neutropenia.
- Describir las características demográficas (edad y sexo) de las personas que han desarrollado neutropenia asociada a clozapina en nuestro estudio.
Materiales y métodos
Se realizó un estudio de cohortes en usuarios del Hospital Vilardebó que iniciaron tratamiento con clozapina. Se selec-
cionaron individuos de ambos sexos, mayores de 18 años que comenzaron el tratamiento en el periodo comprendido entre el 1 de julio de 2022 y el 30 de junio de 2023 y cuyo segui- miento paraclínico se llevó a cabo en el Hospital Vilardebó. Se obtuvieron los datos del registro de farmacia del Hospital Vilardebó de los pacientes que comenzaron tratamiento con clozapina en el periodo estudiado. El criterio de exclusión fue tener una edad menor a 18 años al momento del comienzo del tratamiento.
Se realizó una revisión de historias clínicas en formato vir- tual y de papel con el objetivo de recabar los datos clínicos y paraclínicos relevantes. Se analizaron los datos patronímicos, la justificación del uso de clozapina, las dosis utilizadas, los valores hematimétricos iniciales y los de seguimiento; se co- tejaron los datos con los registros en controles clínicos para valorar adherencia, persistencia y tolerancia al tratamiento, así como causas de discontinuación.
Se elaboraron fichas de cada paciente que incluyeron los datos recabados.
Se consideró una observación completa aquella en la que el individuo completó 26 semanas de tratamiento con clozapina en forma ininterrumpida con hemogramas semanales durante este periodo; una observación suficiente aquella en la que el individuo completó 26 semanas de tratamiento con clozapina en forma ininterrumpida, contando con datos hematimétricos en el curso de este periodo sin cumplir con los requerimientos establecidos por los protocolos institucionales; y una observa- ción insuficiente la de aquellos pacientes que no completaron las 26 semanas de tratamiento por abandono del mismo o aquellos de los que no hubo registro de seguimiento.
Para la definición del evento se tomaron como referencia los valores establecidos por las guías del Hospital Vilardebó que definen la presencia de neutropenia leve con valores de neutrófilos entre 1000 y 1499/mm3, neutropenia moderadora entre 500 y 999/mm3 y neutropenia severa con valores por debajo de 500/mm3.
Las variables incluidas en este estudio fueron sexo, edad, recuento de neutrófilos, severidad de la neutropenia, dosis de clozapina, tiempo de tratamiento en semanas y suspensión del tratamiento.
Este trabajo fue realizado en Montevideo, Uruguay, en el período comprendido entre febrero y abril del 2024.
Análisis de datos
Para evaluar la duración del tratamiento con clozapina an- tes de su suspensión, implementamos análisis de superviven- cia utilizando el modelo de Kaplan-Meier. Este método nos permitió observar el tiempo transcurrido hasta la interrupción del tratamiento y analizar las diferencias entre grupos estra-
Figura 1
| Tabla de presentación de resultados agrupados | |
| Variable | Resultado |
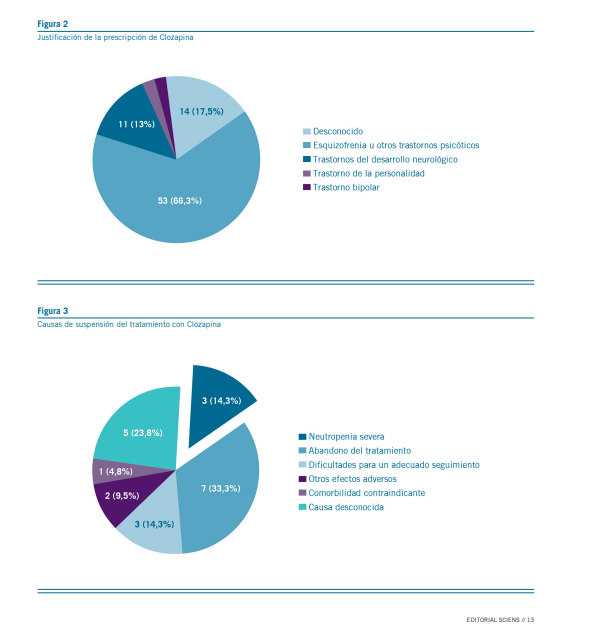
| Diagnóstico | Desconocido: 14 casos (17,28%) Esquizofrenia u otros Trastorno Psicóticos (con o sin comorbilidad, incluye Tras- torno Esquizoafectivo, Trastorno Psicótico no Especificado): 53 casos (65,43%) Trastorno del Desarrollo Neurológico (DI, TEA, inespecífico): 11 casos (13,58%) Trastorno de la Personalidad: 1 caso (1,23%) Trastorno Bipolar: 2 casos (2,46%) |
| Sexo | Mujeres: 27 casos (32,93%) Hombres: 55 casos (67,07%) |
| Edad | 35,11 ± 12,16 años |
| Suspensión de Tratamiento | 25 casos (30,49%) |
| Neutropenia | Neutropenia severa: 3 casos (3,70%) Neutropenia moderada: 1 caso (1,23%) |
| Semanas hasta suspensión | 10,23 ± 7,76 semanas |
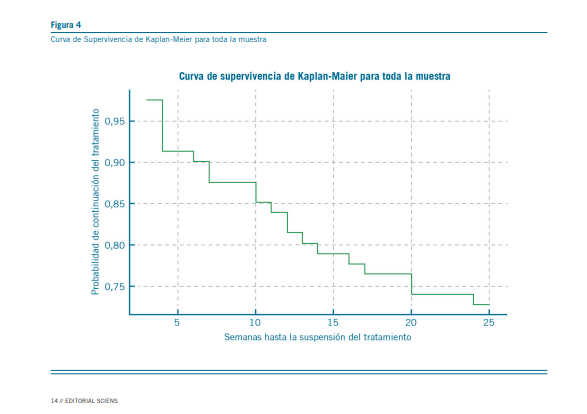
| Causa de suspensión | Neutropenia Severa: 3 casos (3,70%) Comorbilidad: 1 caso (1,23%) Abandono: 7 casos (8,64%) Ausencia de Controles adecuados: 3 casos (3,70%) Efectos Adversos: 2 casos (2,46%) Se desconoce: 5 casos (6,17%) |
| Cantidad de hemogramas | 13,36 ± 6,89 hemogramas |
| Hemograma previo al inicio | 81 casos (100%) |
| Hemograma semanal hasta la semana 18 | 10 casos (12,35%) |
| Hemograma semanal hasta la semana 26 | 1 caso (1,23%) |
| Semana de último hemograma | 20,28 ± 8,25 semanas |
tificados por variables clave como el sexo. Para comparar la duración del tratamiento entre estos grupos, utilizamos la prueba de log-rank, que facilitó la identificación de diferen- cias estadísticamente significativas.
Adicionalmente, calculamos la tasa de incidencia de sus- pensión del tratamiento. Este cálculo proporcionó una fre- cuencia de interrupción por unidad de tiempo, ofreciendo una
perspectiva cuantitativa sobre la regularidad con que los pa- cientes cesan el tratamiento a lo largo del periodo de estudio.
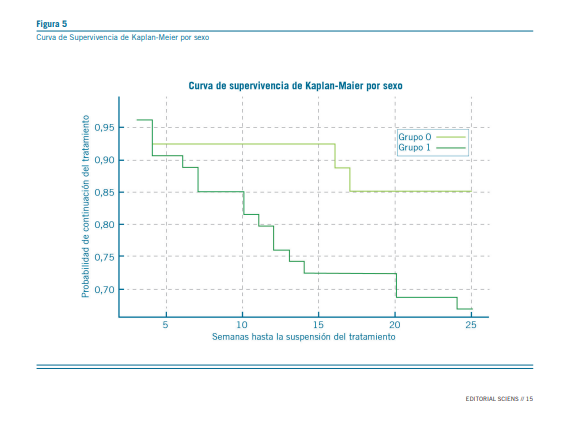
El análisis de Kaplan-Meier también se empleó para generar representaciones gráficas de la probabilidad de continuar con el tratamiento a lo largo del tiempo. Estas curvas permitieron una visualización clara de las tendencias y facilitaron la com- paración entre diferentes subgrupos de pacientes.
Para profundizar en nuestro entendimiento y controlar posi- bles sesgos, incorporamos el análisis de covariables relevantes como la edad y ajustando nuestros modelos para explorar cómo estos factores pueden influir en la suspensión del tratamiento.
Estos ajustes fueron cruciales para minimizar la influencia de factores confusos y mejorar la precisión de nuestros hallaz- gos, permitiendo conclusiones más robustas y aplicables a la práctica clínica.
Perfil de los participantes
Durante el periodo estudiado se recolectaron datos de 81 pacientes que iniciaron el tratamiento con clozapina. La muestra estuvo compuesta por 27 pacientes de sexo feme- nino (32,93%) y 55 de sexo masculino (67,07%). La edad promedio de los participantes fue de 35,11 ± 12,16 años, con edades que oscilaron entre los 19 y los 68 años.
Diagnósticos al inicio del tratamiento
El diagnóstico más común al inicio del tratamiento fue el de esquizofrenia u otros trastornos psicóticos, que incluyen trastorno esquizoafectivo y trastorno psicótico no especifica- do, con o sin comorbilidad. Este diagnóstico se registró en 53 casos (65,43%). Asimismo, se identificaron trastornos del de- sarrollo neurológico, como discapacidad intelectual, trastorno
del espectro autista y trastorno del neurodesarrollo inespecí- fico, en 11 casos (13,58%). Otros diagnósticos al inicio del tratamiento incluyeron trastorno bipolar en 2 casos (2,46%), trastorno de la personalidad en 1 caso (1,23%) y en 14 casos (17,28%) no se registró el diagnóstico (Figura 2).
Suspensión del tratamiento con clozapina
Un total de 25 casos (30,49%) suspendieron el tratamiento con clozapina antes de alcanzar las 26 semanas. Las razones para la suspensión del tratamiento fueron diversas: 3 casos (3,70%) debido a neutropenia severa, 7 casos (8,64%) por abandono del tratamiento, 3 casos (3,70%) por dificultades en el seguimiento adecuado, 2 casos (2,46%) por efectos ad- versos distintos a la neutropenia, y 1 caso (1,23%) debido a una comorbilidad contraindicante. En 5 casos (6,17%), no se pudo determinar la causa de la suspensión del tratamiento (Figura 3).
Presentación, análisis de datos y resultados
(Figura 1)
Seguimiento hematológico
El 100% de los participantes se sometió a un hemograma en los 10 días previos al inicio del tratamiento con clozapina. Solo 1 caso (1,23%) presentó datos de hemogramas sema-
nales hasta la semana 26, mientras que 10 casos (12,35%) registraron hemogramas semanales hasta la semana 18, pero no hasta la semana 26. El promedio de seguimiento hema- tológico ya sea semanal o con un intervalo mayor entre los controles, fue de 20,28 ± 8,25 semanas, con un promedio de 13,36 ± 6,89 hemogramas realizados por paciente.
Relación entre neutropenia y dosis de clozapina
No se obtuvieron datos suficientes sobre las dosis de clo- zapina utilizadas para el análisis de relación con la presencia de neutropenia.
Tasa de incidencia de neutropenia
Semanal: la tasa de incidencia semanal de neutropenia es de 0.002274 casos por semana-persona. Esto implica que, en un grupo hipotético de 439 personas observadas duran- te una semana, se esperaría identificar aproximadamente un nuevo caso de neutropenia. Este cálculo nos ayuda a entender la rareza con la que este evento se presenta en un periodo tan corto de tiempo.
Mensual: de manera similar, la tasa mensual de 0.0098 casos por mes-persona sugiere que, en un grupo de 102 per- sonas seguidas durante un mes completo, se podría prever la aparición de un nuevo caso de neutropenia. Esta tasa refleja
una baja frecuencia del evento, subrayando la importancia de un seguimiento continuo y detallado en poblaciones más grandes o durante periodos más extensos.
Por período de 18 semanas: en tratamientos que duran 18 semanas, la incidencia de neutropenia es de 0.041 casos por cada 18 semanas-persona. Esto significa que se necesitarían aproximadamente 24 ciclos completos de tratamiento de 18 semanas cada uno para observar un nuevo caso. Esta cifra nos ofrece una perspectiva sobre la probabilidad acumulativa de desarrollar neutropenia a lo largo de un tratamiento de duración media.
Por período de 26 semanas: finalmente, con una tasa de
0.059 casos por cada 26 semanas-persona en tratamientos de 26 semanas, se requerirían cerca de 17 ciclos completos de tratamiento para presenciar un nuevo caso de neutrope- nia. Esta tasa nos da una visión de la frecuencia con la que podríamos esperar este efecto adverso en tratamientos más prolongados.
Análisis e interpretación
Basado en los datos analizados, no se encontraron diferencias estadísticamente significativas en la supervivencia entre hombres y mujeres con el tamaño de muestra dado.
Discusión
La presente discusión busca profundizar en los hallazgos clave obtenidos del estudio sobre el uso de clozapina y su asociada incidencia de neutropenia.
Este estudio involucró una muestra de 81 pacientes y reveló una incidencia relativamente baja de neutropenia (4,93%), 1 caso de neutropenia moderada (1,23%) y 3 casos de neutro- penia severa (3,70%); esto que refleja una proporción signi- ficativa dado el grave potencial de este efecto adverso. En el estudio realizado en Dinamarca en el año 2022 de CF Johan- nsen et al. se estudiaron 520 pacientes, obteniendo una tasa de incidencia de 3,2 (IC 95% 2,1-4,8) casos por cada 100 personas por año por lo que, a pesar de las notables diferen- cias en el total de pacientes estudiados, la incidencia resulta semejante a la encontrada en nuestro trabajo (23).
En los 3 casos de neutropenia severa la conducta adoptada fue la de suspender el tratamiento tal como indican las guías nacionales (20). Existen publicaciones que muestran la baja incidencia de recurrencia de eventos hematológicos luego de la reinstalación de clozapina posterior a un evento de neu- tropenia que evidencian la posibilidad de que este evento no
determine la suspensión del tratamiento en forma definitiva
(24). En el estudio argentino publicado en el año 2016 por C Prokopez et al. el 70 % de los pacientes a los que se les reinstaló el tratamiento con clozapina luego de un evento de linfopenia o neutropenia no desarrollaron un nuevo evento he- matológico (25).
Sin embargo, tal como en el caso de los 3 paciente que de- sarrollaron neutropenia severa en nuestro trabajo, existe con- senso en que aquellos pacientes que han desarrollado este tipo de neutropenia, con valores de neutrófilos por debajo de los 500 mm3, son aquellos con el mayor riesgo de reiterar el evento y en los que la reinstalación del tratamiento sigue siendo controversial (24).
Es notable que el caso de neutropenia moderada se resolvió sin mayores complicaciones y ocurrió en contexto de comorbi- lidad con neumonía no determinando la suspensión del trata- miento con clozapina. Este detalle subraya la importancia de monitorear estrechamente la salud global del paciente, ya que las condiciones comórbidas pueden complicar la interpreta- ción de los efectos adversos como la neutropenia.
No se evidenciaron en nuestro estudio diferencias estadísticamente significativas en la incidencia de neutropenia entre
sexos, siendo 3 de los 4 casos de sexo masculino. Esto con- trasta con lo evidenciado en el artículo de Lau, K et al. en que dos tercios de la población que desarrollo neutropenia fue de sexo femenino. Probablemente esta diferencia pueda tener relación con el tamaño de la muestra (26).
Limitaciones en la recolección de datos
Una dificultad clave identificada en este estudio fue la falta
de registros detallados, especialmente en relación con las dosis de clozapina administradas. Esta carencia de datos precisa dificulta la obtención de conclusiones más robustas y destaca la necesidad de mantener un registro clínico riguroso y sistemático para futuras investigaciones. Tal mejora en la recolección de datos facilitaría una evaluación más precisa del vínculo entre la dosificación de clozapina y la incidencia de neutropenia.
Disparidad de género y la prescripción de clozapina
El estudio expuso una significativa disparidad de género entre los pacientes tratados con clozapina, con predominan- cia masculina. Este desbalance plantea interrogantes sobre las posibles diferencias de género en la prescripción de este tratamiento y subraya la necesidad de investigar más a fondo las razones detrás de esta tendencia. La exploración de estas diferencias podría revelar sesgos en la práctica clínica, dife- rencias intrínsecas en la susceptibilidad o respuesta al trata- miento entre géneros o variables clínicas que justifiquen un uso más frecuente de clozapina en hombres que en mujeres.
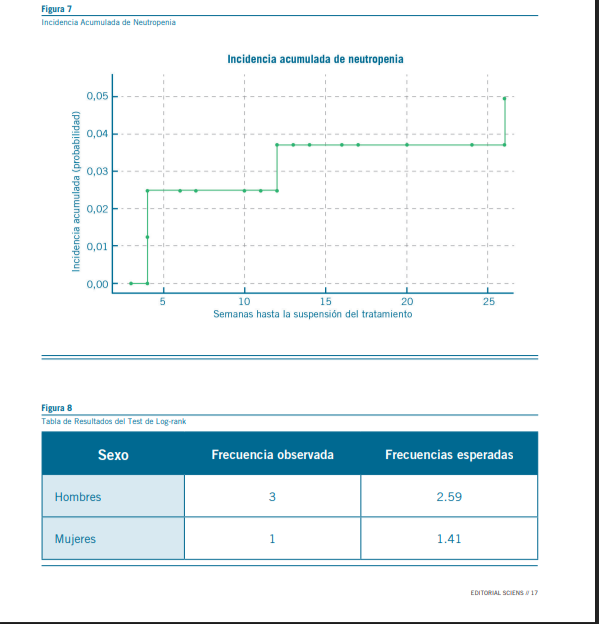
Temporalidad y monitoreo de la neutropenia
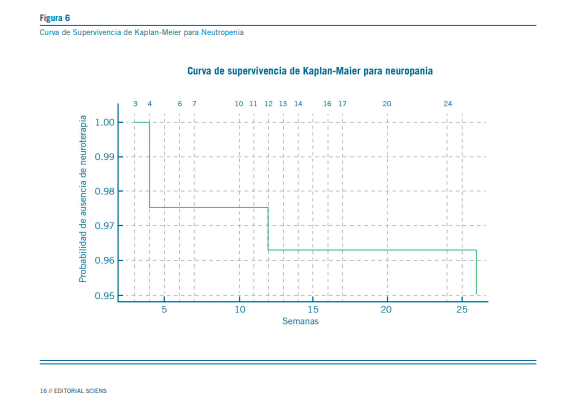
En relación con la temporalidad y monitoreo de la neutro- penia, los patrones observados en el estudio indican que la mayoría de los eventos de neutropenia tienden a concentrarse en las primeras etapas del tratamiento. Específicamente, se registraron dos casos de neutropenia en la cuarta semana y otro en la duodécima semana de tratamiento con clozapina. Este patrón sugiere que el riesgo de desarrollar neutropenia es particularmente alto durante las primeras 18 semanas, lo que subraya la importancia de implementar un monitoreo hemato- lógico intensivo durante este periodo crítico.
La recomendación de un monitoreo riguroso durante las pri- meras 18 semanas se basa en la evidencia de que los cambios hematológicos, especialmente la disminución de los niveles de neutrófilos, son más probables de ocurrir en este tiempo. Este seguimiento temprano y frecuente permite la detección precoz de cualquier signo de neutropenia, facilitando inter- venciones oportunas que pueden prevenir complicaciones gra- ves asociadas a esta condición.
Sin embargo, los datos también revelan que el riesgo de neutropenia no se limita exclusivamente a este periodo inicial. Por ejemplo, un caso de neutropenia moderada se presentó en la semana 24, destacando que los eventos adversos he- matológicos pueden surgir incluso después de superadas las primeras 18 semanas, si bien este episodio se dio en contexto de comorbilidad. Esto resalta la necesidad de no descuidar el monitoreo hematológico incluso después del periodo inicial de riesgo más elevado. En este sentido, se recomienda con- tinuar con chequeos regulares de los parámetros sanguíneos más allá de las 18 semanas, extendiendo el monitoreo hasta que se considere seguro reducir la frecuencia de las pruebas, basándose en la estabilidad clínica del paciente y los resulta- dos hematológicos previos.
Desafíos en el seguimiento hematológico
A diferencia de lo evidenciado en el estudio de JM Lucca et al., realizado en el 2021 en el que un 71,9% de los pacientes obtuvieron un seguimiento hematológico adecuado hasta la semana 18 (27), en nuestro trabajo se detectó una preocu- pante dificultad en el seguimiento adecuado de los pacientes mediante hemogramas; especialmente en entornos ambula-
torios comparados con los intrahospitalarios. Este objetivo se alcanzó únicamente en el 12,35% de los casos. Estos resul- tados son comparables con los obtenidos del estudio llevado a cabo por O Ingimarsson et al en Islandia en el que el control semanal durante las primeras 18 semanas se dio en el 14,4% de los casos estudiados (13).
En el trabajo de S Farooq et al., se entrevistó a 277 psi- quiatras acerca de las dificultades percibidas para el uso de clozapina en su práctica clínica, se consideraron aspectos clí- nicos, no clínicos y relacionados con la presencia de efectos adversos. Los dos factores más determinantes en este estudio resultaron ser la probable falta de adherencia de los pacientes a los controles hematológicos y la carga que esto supondría para los mismos (28).
El estudio realizado por la National Association of State Mental Health Program Directors (NASMHPD) en EE.UU. for- mó un equipo de 11 psiquiatras clínicos para identificar las barreras vinculadas a la infrautilización de clozapina y anali- zar las intervenciones necesarias para superarlas. Dentro de las barreras encontradas se incluyen la negación por parte de los pacientes a la realización de hemogramas, la dificultad en el cumplimiento de los protocolos, la necesidad de un seguimiento intenso, la falta de recursos para la monitorización del comienzo del uso de clozapina, la complejidad del papeleo requerido y los costes y dificultades de transporte para el cumplimiento de los protocolos (29). Esta observación sugiere que mejorar el acceso y la regularidad de los hemogramas en entornos ambulatorios podría ser crucial para mantener un control óptimo, prevenir complicaciones severas y disminuir los obstáculos percibidos por los técnicos para la prescripción de clozapina.
Tal dificultad también pone de manifiesto la necesidad de revisar las pautas de control hematológico con el fin de sim- plificar su aplicabilidad en la práctica clínica sin descuidar la vigilancia activa que permita identificar en forma oportuna la presencia de eventos adversos. Se recomienda la creación de centros especializados o la implementación de recursos inter- disciplinarios que sistematicen el seguimiento.
Implicaciones para la práctica clínica y futuras investigaciones Más allá de la neutropenia, otros factores como efectos ad- versos no relacionados con esta condición también contribu- yeron al abandono del tratamiento. Esto resalta la importancia de un enfoque global en el manejo de pacientes en trata- miento con clozapina, no solo para prevenir la neutropenia sino también para manejar otros posibles efectos adversos y mejorar la adherencia al tratamiento.
Finalmente, como en la mayoría de los estudios interna- cionales, la principal causa de indicación de clozapina fue la presencia de esquizofrenia resistente al tratamiento, otras in- dicaciones fueron trastornos del neurodesarrollo con conductas disruptivas, trastorno bipolar y trastorno de la personalidad
(27). Este amplio espectro de uso enfatiza la necesidad de considerar las características individuales y los diagnósticos específicos al decidir la terapia con clozapina, garantizando así una personalización del tratamiento que pueda maximizar beneficios y minimizar riesgos.
Existe evidencia de que la Neutropenia es un evento independiente de la dosis de clozapina, por lo que su aparición obedece a la presencia de otros factores que ya hemos analizado y probablemente a otros de los que aún no estamos en conocimiento. Esto indica que en futuros escenarios se debe- ría individualizar la pauta de monitorización a cada paciente para disminuir engorrosos controles que puedan desalentar o interferir en la continuidad del tratamiento, como vimos en este estudio. Se destaca la necesidad de desarrollar nuevas estrategias, como el estudio de biomarcadores, para predecir la posibilidad de desarrollo del evento en cada paciente (28, 30, 31).
Conclusión
Este estudio proporciona perspectivas útiles sobre la admi- nistración de clozapina, resaltando aspectos clave que me- recen una mayor atención en futuras investigaciones y en la práctica clínica diaria. Estos hallazgos apuntan a mejorar la indicación, los resultados y la seguridad del tratamiento con clozapina.
Un aprendizaje de esta investigación es la necesidad de opti- mizar el monitoreo de la neutropenia, una complicación poten- cial del tratamiento con clozapina. Aunque la incidencia obser- vada de neutropenia fue baja, los casos identificados subrayan la importancia de un monitoreo hematológico riguroso, no solo durante las primeras 18 semanas de tratamiento, cuando el riesgo es mayor, sino también más allá de este período.
El estudio también sugiere revisar las directrices para la reintroducción de clozapina tras un episodio de neutropenia.
La evidencia de que algunos pacientes pueden continuar con clozapina sin recurrencias destaca la necesidad de considerar cuidadosamente la suspensión definitiva del tratamiento, eva- luando de manera exhaustiva el equilibrio entre los riesgos y beneficios para cada paciente.
En cuanto a las prácticas de prescripción, se identifica la importancia de considerar las diferencias de género en la ad- ministración de clozapina, lo que podría justificar la adapta- ción de las estrategias de tratamiento según características individuales como el género, las comorbilidades y el historial clínico del paciente.
Además, se evidencia la necesidad de mejorar la documen- tación relacionada con la administración de clozapina. La fal- ta de datos detallados limita la capacidad de analizar con pre- cisión la relación entre las dosis administradas y la incidencia de efectos adversos, lo que podría contribuir a optimizar los resultados del tratamiento a largo plazo. Mejorar la precisión y la completitud de los registros facilitaría evaluaciones más efectivas y orientaría mejor las decisiones clínicas.
Finalmente, la valoración paraclínica actual del uso de clo- zapina, debido a su complejidad y rigor, puede dificultar el seguimiento continuo de los pacientes y, en algunos casos, desincentivar tanto a médicos como a pacientes a optar por este tratamiento. Esto resalta la necesidad de reevaluar las guías clínicas existentes, con el objetivo de adaptar las re- comendaciones de prescripción y seguimiento para que sean más accesibles y flexibles, permitiendo una personalización según las características individuales de cada paciente. La meta principal de esta reevaluación debe ser optimizar el uso seguro y eficaz de la clozapina, asegurando que las medidas de seguimiento no sean tan estrictas o complejas que com- prometan la adherencia al tratamiento o su viabilidad a largo plazo. En este sentido, es fundamental encontrar un equili- brio que permita mantener altos estándares de seguridad sin crear barreras insalvables para el acceso y la continuidad del tratamiento.
Referencias bibliográficas
- 1. Stahl SM. Clozapine: Is Now the Time for More Clinicians to Adopt This Orphan? CNS Spectr 2014;19:279–81. https://doi. org/10.1017/S1092852914000418.
- 2. Meltzer HY. Clozapine. Clin Schizophr Relat Psychoses 2012;6:134–44. https://doi. org/10.3371/CSRP.6.3.5.
- 3. McEvoy JP, Lieberman JA, Stroup TS, Davis
SM, Meltzer HY, Rosenheck RA, et al. Effecti- veness of clozapine versus olanzapine, quetia- pine, and risperidone in patients with chronic schizophrenia who did not respond to prior atypical antipsychotic treatment. Am J Psychia- try 2006;163:600–10. https://doi.org/10.1176/ ajp.2006.163.4.600.
- 4. Kane J, Honigfeld G, Singer J, Melt- zer H. Clozapine for the treatment-resistant schizophrenic. A double-blind comparison with chlorpromazine. Arch Gen Psychiatry
1988;45:789–96. https://doi.org/10.1001/ar- chpsyc.1988.01800330013001.
- 5. Howes OD, McCutcheon R, Agid O, de Bar- tolomeis A, van Beveren NJM, Birnbaum ML, et al. Treatment-Resistant Schizophrenia: Treat- ment Response and Resistance in Psychosis (TRRIP) Working Group Consensus Guidelines on Diagnosis and Terminology. Am J Psychiatry 2017;174:216–29. https://doi.org/10.1176/ appi.ajp.2016.16050503.
- 6. Bachmann CJ, Aagaard L, Bernardo M,
Brandt L, Cartabia M, Clavenna A, et al. Inter- national trends in clozapine use: a study in 17 countries. Acta Psychiatr Scand 2017;136:37–
51. https://doi.org/10.1111/acps.12742.
- 7. Meyer JM, Stahl SM. Manual de Clozapina. Madrid: Grupo Aula M{edica, S. L.; 2020.
- 8. Myles N, Myles H, Xia S, Large M, Kisely S, Galletly C, et al. Meta-analysis examining the epidemiology of clozapine-associated neutrope- nia. Acta Psychiatr Scand 2018;138:101–9. https://doi.org/10.1111/acps.12898.
- 9. Verbelen M, Collier DA, Cohen D, MacCabe JH, Lewis CM. Establishing the characteristics of an effective pharmacogenetic test for clozapi- ne-induced agranulocytosis. Pharmacogenomics J 2015;15:461–6. https://doi.org/10.1038/ tpj.2015.5.
- 10. Li X-H, Zhong X-M, Lu L, Zheng W, Wang S-B, Rao W-W, et al. The prevalence of agra- nulocytosis and related death in clozapine-trea- ted patients: a comprehensive meta-analy- sis of observational studies. Psychol Med 2020;50:583–94. https://doi.org/10.1017/ S0033291719000369.
- 11. Yang C-C, Wang X-Y, Chou P-H, Lin C-H. Valproate-related neutropenia and lithium-re- lated leukocytosis in patients treated with clo- zapine: a retrospective cohort study. BMC Psy- chiatry 2023;23:170. https://doi.org/10.1186/ s12888-023-04659-2.
- 12. Balda M V, Garay OU, Papale RM, Bignone I, Bologna VG, Brandolini A, et al. Clozapine-as- sociated neutropenia and agranulocytosis in Ar- gentina (2007-2012). Int Clin Psychopharma- col 2015;30:109–14. https://doi.org/10.1097/ YIC.0000000000000060.
- 13. Ingimarsson O, MacCabe JH, Haraldsson M, Jónsdóttir H, Sigurdsson E. Neutropenia and agranulocytosis during treatment of schizophre- nia with clozapine versus other antipsychotics: an observational study in Iceland. BMC Psy- chiatry 2016;16:441. https://doi.org/10.1186/ s12888-016-1167-0.
- 14. Legge SE, Walters JT. Genetics of clo- zapine-associated neutropenia: recent advan- ces, challenges and future perspective. Phar- macogenomics 2019;20:279–90. https://doi. org/10.2217/pgs-2018-0188.
- 15. Islam F, Hain D, Lewis D, Law R, Brown LC, Tanner J-A, et al. Pharmacogenomics of Clo- zapine-induced agranulocytosis: a systematic review and meta-analysis. Pharmacogenomics J 2022;22:230–40. https://doi.org/10.1038/ s41397-022-00281-9.
- 16. van der Weide K, Loovers H, Pondman K,
Bogers J, van der Straaten T, Langemeijer E, et al. Genetic risk factors for clozapine-induced neutropenia and agranulocytosis in a Dutch psychiatric population. Pharmacogenomics J 2017;17:471–8. https://doi.org/10.1038/ tpj.2016.32.
- 17. Chen J, Yang P, Zhang Q, Chen R, Wang P, Liu B, et al. Genetic risk of clozapine-induced leukopenia and neutropenia: a genome-wide as- sociation study. Transl Psychiatry 2021;11:343. https://doi.org/10.1038/s41398-021-01470-z.
- 18. Toledo M, Olmos I, Ricciardi C. ¡Paradoja! La clozapina y su uso marginal. Revista de Psi- quiatría Del Uruguay 2018;82:84–7.
- 19. Cetin M. Clozaphobia: Fear of Prescribers of Clozapine for Treatment of Schizophrenia. Kli- nik Psikofarmakoloji Bülteni-Bulletin of Clinical Psychopharmacology 2014;24:295–301. ht- tps://doi.org/10.5455/bcp.20141223052008.
- 20. Ministerio de Salud Pública. Ordenanza Ministerial N.o 435/2016 . Https://WwwGubUy/ Ministerio-Salud-Publica/Institucional/Normati- va/Ordenanza-n-435015-Incorporacion-Princi- pios-Activos-Sistema 2016.
- 21. Olmos I. Presentación del protocolo de utilización de clozapina en el Hospital Vilardebó
– ASSE. 2018.
- 22. Oloyede E, Dzahini O, Abolou Z, Gee S, Whiskey E, Malhotra D, et al. Clinical impact of reducing the frequency of clozapine moni- toring: controlled mirror-image cohort study. Br J Psychiatry 2023;223:382–8. https://doi. org/10.1192/bjp.2023.44.
- 23. Johannsen C-F, Petersen TS, Nielsen J, Jørgensen A, Jimenez-Solem E, Fink-Jensen A. Clozapine- and non-clozapine-associated neutro- penia in patients with schizophrenia: a retros- pective cohort study. Ther Adv Psychopharma- col 2022;12:204512532110723. https://doi. org/10.1177/20451253211072341.
- 24. Tirupati S, Gordon T. Continuation of Treatment With Clozapine After an Episo- de of Neutropenia. J Clin Psychopharmacol 2021;41:320–2. https://doi.org/10.1097/ JCP.0000000000001371.
- 25. Prokopez CR, Armesto AR, Gil Aguer MF, Balda M V., Papale RM, Bignone IM, et al. Clozapine Rechallenge After Neutrope- nia or Leucopenia. J Clin Psychopharmacol 2016;36:377–80. https://doi.org/10.1097/ JCP.0000000000000512.
- 26. Lau KL, Yim PHW. Neutropenia and Agranulocytosis in Chinese Patients Pres- cribed Clozapine. East Asian Arch Psychiatry 2015;25:164–7.
- 27. Lucca JM, Al-Turaifi FM, Safyah A-M, Ha- mad Al-Awad FA. A Comprehensive Monitoring of Clozapine and Related Components in Clinical Practices. Saudi Arabian Scenario. Psychophar- macol Bull 2021;51:40–50.
- 28. Farooq S, Choudry A, Cohen D, Naeem F, Ayub M. Barriers to using clozapine in treat- ment-resistant schizophrenia: systematic re- view. BJPsych Bull 2019;43:8–16. https://doi. org/10.1192/bjb.2018.67.
- 29. Kelly DL, Freudenreich O, Sayer MA, Love RC. Addressing Barriers to Clozapine Underuti- lization: A National Effort. Psychiatric Services 2018;69:224–7. https://doi.org/10.1176/appi. ps.201700162.
- 30. Molden E. Therapeutic drug monitoring of clozapine in adults with schizophrenia: a review of challenges and strategies. Expert Opin Drug Metab Toxicol 2021;17:1211–21. https://doi.or g/10.1080/17425255.2021.1974400.
- 31. Oloyede E, Blackman G, Whiskey E, Ba- chmann C, Dzahini O, Shergill S, et al. Cloza- pine haematological monitoring for neutrope- nia: a global perspective. Epidemiol Psychiatr Sci 2022;31:e83. https://doi.org/10.1017/ S204579602200066X.







No comments! Be the first commenter?