Tratamiento medicamentoso y no medicamentoso de los síntomas psicoconductuales de las demencias (SPCD). Algunas sugerencias
Resumen
La Demencia constituye un problema de salud pública a nivel mundial, y se espera un aumento de su prevalencia dado el envejecimiento progresivo de la población.
Afecta a 50 millones de personas, y se estima que las cifras aumenten en 2030 a 82 millones y a 152 millones en 2050; el 60% de las personas con Demencia viven en países con ingresos medianos y bajos.
Los síntomas conductuales y psicológicos de la demencia (SPCD) o síntomas neuropsiquiátricos, fueron descritos en el primer informe de la enfermedad por Alois Alzheimer. Se estima que todos los enfermos con demencia presentan uno o más síntomas neuropsiquiátricos o psicoconductuales.
Pueden estar presentes desde el inicio (72% de los pacientes los presentan 2 años antes del diagnóstico de demencia) y son inherentes al propio proceso neurodegenerativo que lleva a esta enfermedad, a pesar de que se los consideraba, hasta hace poco tiempo, un fenómeno concomitante y no una manifestación propia. Los SPCD forman parte de la expresión de la alteración de las estructuras cerebrales implicadas también en las funciones cognitivas, existiendo diferencias tanto en el momento de aparición como en su curso y en la respuesta al tratamiento.
El abordaje apropiado de los síntomas psicológicos y conductuales es decisivo, ya que éstos se asocian con consecuencias muy desfavorables para los enfermos, las personas que los asisten, las instituciones que los albergan y los sistemas de salud, provocando un aumento de la morbimortalidad, así como grandes inversiones económicas
La atención del paciente demente o portador de un déficit cognitivo se sustenta en cuatro pilares básicos:
El primero corresponde al tratamiento de los aspectos fundamentales de la enfermedad, con el propósito de revertir los efec- tos o demorar la progresión de ésta.
El segundo se refiere al tratamiento sintomático, ya sea funcional, cognitivo o neuropsiquiátrico, que incluye lo afectivo conductual.
Y el tercer y cuarto pilar corresponde al apoyo al paciente y a los cuidadores en forma sistemática basado en las evidencias científicas que muestran resultados satisfactorios en el tratamiento de esta patología con un aumento del tiempo en que los pacientes permanecen integrados socialmente.
El objetivo de esta revisión es el reflexionar sobre nuestra práctica clínica en lo referente a su tratamiento y a la vez hacer algunas sugerencias en este tan difícil abordaje.
Palabras clave
Demencia – Síntomas psicoconductuales (SPCD).
Introducción
La Demencia constituye un problema de salud pública a nivel mundial, y se espera un aumento de su prevalencia dado el envejecimiento progresivo de la población.
Afecta a 50 millones de personas, y se estima que las cifras aumenten en 2030 a 82 millones y a 152 millones en 2050; el 60% de las personas con Demencia viven en países con ingresos medianos y bajos.
Se estima que todos los enfermos con demencia presentan uno o más síntomas psicosociales y conductuales.
Su abordaje apropiado es decisivo, ya que se asocian con consecuencias muy desfavorables para los enfermos, las personas que los asisten y los sistemas de salud, son los responsables de más de la tercera parte de los costos de atención de la demencia.
Pueden aparecer en cualquier momento de la enfermedad, generan sufrimiento en el paciente, el cuidador y a todo el entorno, agravan el deterioro cognitivo y funcional, son causa de institucionalización, y son altamente prevalentes, (el 97% de los pacientes con diagnóstico de demencia). Los SPCD for-man parte de la expresión de la alteración de las estructuras cerebrales implicadas también en las funciones cognitivas, existiendo diferencias tanto en el momento de aparición como en su curso y en la respuesta al tratamiento (Tabla 1).
Algunos de los síntomas que aparecen con más frecuencia y generan más consultas son: agitación, depresión, apatía, psicosis, agresividad, trastornos del sueño, trastornos motores (actividades repetidas sin ningún propósito) y comportamientos sociales anómalos.
Su prevalencia varía entre los distintos trabajos en función de los pacientes que se incluyen en los estudios, el grado de demencia y el tipo que se investigue, así como si se estudian individuos en la comunidad (cerca del 30% los presenta) o institucionalizados (80%) siendo la agitación el síntoma más persistente, y la apatía el de aparición más temprana, más prevalente y estable (48 al 92%). La ansiedad y la depresión son comunes en las fases tempranas de la EA. La agitación y la apatía también son frecuentes y se agravan en la medida en que la demencia progresa. El delirio, las alucinaciones y la agresión son más episódicos y comunes en la demencia moderada a grave.
El 50% de los pacientes presentan síntomas depresivos in- cluso años antes de la aparición de los cognitivos, y es mayor su probabilidad en aquellos con antecedentes tanto persona- les como familiares de esta enfermedad.
La desinhibición ocurre en la tercera parte de los pacientes y es más frecuente en las demencias frontotemporales.
Dentro de las alucinaciones, las visuales son las que predo- minan (entre el 4 y el 76%) siendo más frecuentes en la En- fermedad por cuerpo de Lewy, mientras que la irritabilidad y la labilidad emocional son de mayor prevalencia en la medida que la enfermedad progresa.
Con respecto a conductas más complejas como son los actos delictivos, estos se ubican como el primer síntoma de demen- cia en el 14% de los pacientes con demencia frontotemporal; los pacientes con EA desarrollan problemas conductuales o agresividad en una etapa más avanzada de la enfermedad.
Tabla 1
Comparación entre síntomas cognitivos y psico conductuales
| Sistemas cognitivos | SPCD | |
| Aparición | En la fase de DCL, o trastorno neurocog- nitivo menor. | Debut variable; pueden manifestarse como deterioro comportamental leve (DCoL) incluso antes. |
| Síntomas de fases iniciales | Hay síntomas cognitivos que diferencian cada tipo de demencia, pero se mantie- nen homogéneos dentro de cada subtipo. | No hay una especificidad en los SPCD, con excepción de los trastornos del sueño en las sinucleinopatías y las alu- cinaciones en la demencia con cuerpos de Lewy. |
| Relación entre los síntomas | Aparecen y progresan en estrecha rela- ción con otros síntomas cognitivos. | Se han descrito grupos de síntomas que aparece juntos, No se presentan todos en todos los pacientes. |
| Curso de los síntomas | Progresión continua hasta las fases terminales de las demencias. | Pueden mantenerse, agravarse o desapa- recer conforme progresa la demencia. |
| Respuesta al tratamiento | No se eliminan. Puede mejorar o mode- rar su progresión. | Puede desaparecer o prevenirse su reaparición. |
Modificado de Psiquiatría Geriátrica de Agüera Ortiz.
Desde el año 1999 la Asociación Internacional de Psicoge- riatría (International Psychogeriatric Association IPA) incluyó los síntomas conductuales de la demencia y pasó a denomi- narlo Behavioral and Psychological Symptoms of Dementia (BPSD), síntomas psicológicos y conductuales de la demen- cia (SPCD) y finalmente fue incluido dentro de los criterios diagnósticos de demencia por cualquier causa por el National Institute of Aging y la Alzheimer´s Association (1).
Cada uno de los SPCD pueden tener un origen multifactorial siendo muy diferentes entre sí.
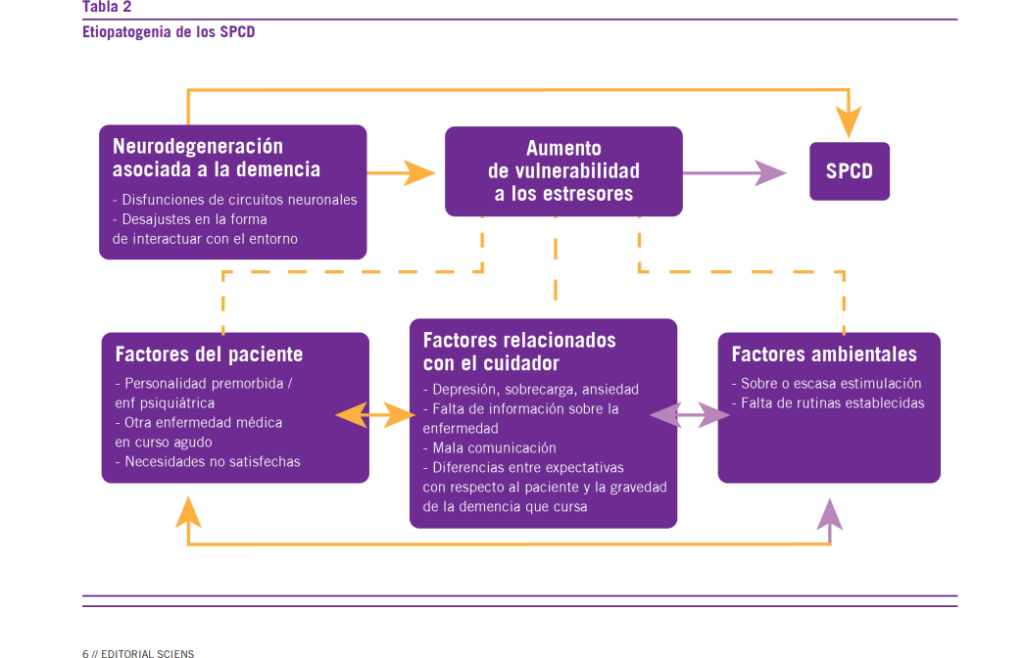
Etiopatogenia
Su etiopatogenia es el resultado de la conjunción de múltiples procesos biopsicosociales en los que se incluyen procesos neurobiológicos secundarios a factores farmacológicos, traumáticos, mecanismos neuro inflamatorios, hipo metabolismo de algunos sectores corticales, causas genéticas, lesiones vasculares, etcétera. También influyen los ambientales; en este sentido se ha planteado que los SPCD pueden relacionarse y responder a factores estresantes ambientales en los que se incluyen aquellos que dependen del cuidador (Tabla2). Estamos ante una repuesta psico comportamental de estas personas al estrés, las que tendrían una vulnerabilidad incrementada a estos factores, ya que a medida que pasa el tiempo se necesita menor intensidad de ellos para que aparezca la sintomatología.
El paciente demenciado en etapas avanzadas tiene grandes dificultades en la comunicación, no pudiendo expresar cosas tan simples como el hambre, la sed, el dolor, la necesidad de evacuación urinaria o intestinal pudiendo estar inquieto o agitado como forma de expresión de dichas incomodidades.
En lo referente al cuidador, están sometidos a la sobrecarga de los cuidados, sobre todo en pacientes con SPCD, que les pue- de producir dificultades en su bienestar tanto psicológico como físico. En ellos se observa frecuentemente sintomatología depre- siva y ansiosa que puede alterar la comunicación de este con el paciente. Por lo que al momento de instrumentar el tratamiento debemos pensar al paciente y al cuidador como un binomio.
Dentro de los factores ambientales, recordemos que los pa- cientes con un trastorno cognitivo tienen dificultad para res- ponder a los estímulos y mayor frustración ante los cambios de su entorno.
Un tercio de los pacientes pueden estar cursando otros cua- dros médicos como son las infecciones, sobre todo urinarias y respiratorias pausisintomáticas, siendo lo único detectable clínicamente la presencia de SPCD de instalación brusca. Pueden ser secundarios a dolor, constipación, deshidratación, o alteraciones que se aprecian en los exámenes de laboratorio. También ante cambios de medicamentos. De estos los más comunes son aquellos con acción anticolinérgica (algunos antidepresivos, antipsicóticos, antimuscarínicos, antiepilépti-
cos) que pueden producir alteraciones cognitivas y confusión, y también opioides y benzodiacepinas.
En su neurobiología se incluyen cambios anatómicos, fun- cionales y bioquímicos del sistema nervioso.
Los diferentes SPCD se correlacionan con anormalidades neurobiológicas, que fundamentalmente afectan a los lóbulos frontales, temporales y parietales, como se ha corroborado en estudios neuropatológicos y de neuroimágenes funcionales.
Se han observado placas neuríticas y ovillos neurofibrilares en la corteza frontal y temporal en pacientes, con apatía. La disfunción frontal, parietal y temporal se asocia con la aparición de síntomas psicóticos.
Los cambios neuroquímicos incluyen alteraciones de las neuronas colinérgicas de las cortezas frontales y temporales y cambios en los sistemas tanto serotoninérgicos como adrenérgicos. Hay niveles más altos de noradrenalina en la sustancia negra y disminución de la serotonina en sectores parahipo- campales, asociados a los síntomas psicóticos.
Desde el punto de vista genético el gen APOE con sus diferentes alelos estaría asociado a diferentes manifestaciones de la demencia tipo Alzheimer, es así como el APOE4 en homocigotes para este gen se asocia con el inicio más precoz
de los síntomas, y con desorientación, agitación y trastornos motores. El APOE3 con los trastornos del sueño y la ansiedad y el APOE2 con los síntomas depresivos. También el polimor- fismo de los receptores serotoninérgicos 5-HT2A se asocia a las alucinaciones visuales y auditivas y el de los receptores dopaminérgicos a la psicosis y a la agresión.
Finalmente, los individuos portadores de elevados niveles de neuroticismo premórbidos (ansiedad, depresión, hostili- dad, timidez, impulsividad) estarían más propensos a desarro- llar síntomas de tipo depresivos.
Diagnóstico
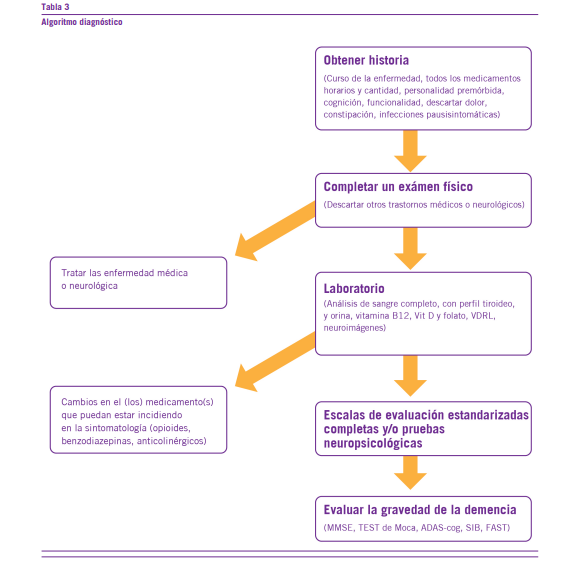
La evaluación de los SPCD implica la entrevista del pacien- te, de los cuidadores y familiares, y la comunicación con el resto de los profesionales intervinientes en la atención, ade- más de la exploración física y los exámenes de laboratorio complementarios. Estos últimos nos permitirán encontrar y descartar otras probables etiologías de los síntomas.
La aplicación de escalas de evaluación, nos servirán para de- tectar el grado del trastorno cognitivo y sus manifestaciones.
La entrevista psicogeriatría es uno de los momentos más importantes en la atención del adulto mayor. Se debe obtener información del propio paciente, cuando esto es posible, de su familia y de los cuidadores principales contrastándola con la que puede aportar otro informante, ya que esta puede estar teñida por la sobrecarga qué tenga el cuidador principal.
Se intentará evaluar el estado mental de la forma más com- pleta posible.
Es necesario valorar la personalidad y la biografía del pa- ciente buscando antecedentes personales, tanto de enferme- dades psiquiátricas como de otras enfermedades médicas.
Las más frecuentes que pueden provocar síntomas psiquiá- tricos son: insuficiencia cardíaca descompensada, período posterior al infarto de miocardio, EPOC descompensada (so- bre todo si se incrementa la dosis de broncodilatadores y cor- ticoides), infecciones, dolor crónico, constipación, aquellas que dificultan la movilidad, enfermedades degenerativas del SNC, o síntomas que son secundarios a patología neoplásica. También es importante evaluar posibles cambios en la medicación que pueden provocar estos síntomas, como son los anticolinérgicos (pueden producir confusión y alteracio- nes cognitivas), opioides y benzodiacepinas (pueden producir
trastornos en la cognición) (2, 3).
Se hará una historia detallada de toda la medicación pres- cripta, actual o precedente, pidiéndole al paciente y/o al cui- dador que traiga una lista escrita de los medicamentos que está tomando y su posología.
Hay que recordar que es frecuente en el paciente mayor el uso de analgésicos, antiinflamatorios, vitaminas, laxantes y plantas medicinales. Esta información detallada nos servirá para tener en cuenta las posibles interacciones y reacciones adversas.
Siempre indagar el uso de sustancias psicoactivas, en el que incluiremos sobre todo el alcohol, tabaco, y hoy con ma-
yor frecuencia el cannabis (Tabla 3).
Se debe considerar las circunstancias actuales de la vida del paciente, su capacidad funcional e indagar antecedentes fami- liares de trastornos psiquiátricos y especialmente cognitivos.
La evaluación familiar en su funcionalidad nos permitirá prever la viabilidad en la instrumentación de la ayuda para el anciano que esta tenga.
También la percepción que tenga el paciente del apoyo fa- miliar y su capacidad para aceptar la ayuda y también la to- lerancia que tiene la familia a la patología del adulto mayor, sobre todo cuando existen comportamientos disruptivos.
Los síntomas se analizan por separado con preguntas con- cretas como son: si el paciente se pone agresivo, si grita, si pega, si golpea, teniendo en cuenta el momento de su inicio, el contexto en donde se instalaron, su frecuencia y gravedad y los cambios a lo largo del tiempo.
Mapear la frecuencia y severidad de los síntomas durante varios días, nos permitirá evaluar las posibles situaciones de estrés que esto genera. Recordemos que algunos de los sínto- mas no suelen manifestarse como conductas disruptivas, son un ejemplo de esto los cuadros depresivos y la apatía.
Existen diferentes herramientas para la valoración de los síntomas específicos o para hacer una valoración global de
Tabla 4

Tratamiento
El tratamiento farmacológico siempre será la segunda elec- ción luego del fracaso de los tratamientos no medicamento- sos, y solo está justificado en caso de sintomatología intensa o en situaciones de peligro o riesgo para el paciente o para quienes le rodean (4, 5).
Las indicaciones deben ser individualizadas, con especial atención al enfermo, los cuidadores (las que han sido muy eficaces y deberían implementarse siempre), la familia y los factores ambientales.
En algunos casos, incluso, el beneficio de estas medidas ha sido más importante que el que se puede obtener con el tratamiento medicamentoso.
Cuando no es posible encontrar causas subyacentes o la co- rrección de estas causas no es suficiente, pueden necesitarse medicamentos que se administran de forma ocasional dada la agudeza de la situación, o de forma más sostenida como ameritan cuadros que cursan con ideas delirantes o depresión grave. Debido a la complejidad de las causas que intervienen en la etiología de estos síntomas ninguna estrategia terapéuti- ca medicamentosa es eficaz en todas las situaciones.
No es infrecuente que en el curso de la enfermedad algún SPCD no ceda con intervenciones no medicamentosas ni tam- poco medicamentosas, poniendo en riesgo la seguridad del paciente y de su entorno. Esta situación, de difícil manejo ambulatorio, puede requerir el ingreso en el hospital para rea- lizar una profunda valoración de los síntomas, de su etiología, tratar las comorbilidades, y así optimizar el tratamiento de los SPCD.
Tratamiento no medicamentoso de los sín- tomas neuropsiquiátricos; algunas suge- rencias
Las indicaciones de tratamiento deben ser individualizadas, con especial atención al enfermo, los cuidadores y a los facto- res ambientales. La primera línea de tratamiento la constituye el no medicamentoso.
No existe ninguna opción que sea eficaz para todas las si- tuaciones.
Estas medidas han tenido mejor respuesta que el que se puede obtener con el tratamiento medicamentoso. Las guías vigentes hacen hincapié en la implementación de las estrate- gias no medicamentosas, especialmente aquellas que tienen como centro a los cuidadores.
Como medidas generales se han propuesto
Con respecto a las actividades diarias del paciente:
Estimular las capacidades que aún están preservadas y
aquellas que fueron de interés previo del paciente. Muchas veces hay que ayudar al paciente a iniciar su participación.
Educar al cuidador con respecto a los síntomas:
Hay que explicar que los comportamientos no son intencio- nales y suavizar las reglas.
En cuanto a la comunicación:
Darle tiempo al paciente para responder a una pregunta y mantenerse calmado. Ofrecerle opciones simples y evitar tono negativo. Si es necesario calmar al paciente, se puede ha- cer un acercamiento físico y tocarlo en forma tranquilla y sin apretarlo.
Simplificar tareas:
Se propondrán en pasos simples, con utilización de ayudas verbales para cada paso, así como rutinas predecibles.
Simplificar el entorno:
Apartar objetos innecesarios o que puedan dañarlo. Elimi- nar los ruidos y distracciones cuando realiza una actividad. Sacar alfombras y muebles en pasillos que eviten los golpes y tropiezos. Adecuar el baño, sacar la bañera, instalar ducheros con barandas y ducha de mano y sobre inodoro para aumentar su altura
La actividad física no modifica el estado de ánimo, pero podría mejorar la calidad del sueño.
La musicoterapia es particularmente eficaz para el trata- miento de los enfermos con agresión y agitación. Muchas veces en pacientes con anomias el cantar los ayuda a comu- nicarse.
La dieta tiene que ser moderada sobre todo en la noche.
Tratamiento de síntomas particulares
Cuando el paciente en forma reiterada quiere irse del lugar que habita:
Se pueden reducir la cantidad de puertas cerradas que evi- tará la frustración que le implica no poder salir.
Pintar las puertas del mismo color que la pared ayuda a que al paciente se le dificulte el salir.
Ante la repetición de preguntas:
¿Cuándo viene mi hijo?: reconocer el sentimiento que hay detrás de esa pregunta, dar confort ante ese sentimiento.
¿Qué día es hoy? Que busque la respuesta en tarjeta que se les dan y guardan en sus bolsillos.
En las alteraciones del sueño:
No insistir con que no duerma durante el día pero que sus siestas sean cortas, durante la noche hacer higiene del sueño. Hay que tener en cuenta que todos los adultos mayores se levantan varias veces en la noche.
Con respecto al ambiente:
Prever una rápida asistencia por si fuera necesario
Tratar de mantener la independencia del paciente lo más posible sin invadir su auto validez, promover actividades y contacto social.
No confrontar el paciente, tratar de cambiar su atención a otro foco.
En lo posible no invadir su espacio personal.
Cuando no quiere tomar la medicación intentar darle solo aquello que sea de vital importancia.
Respetar su intimidad y darle tiempo en el uso del baño.
Importancia del cuidador
Los síntomas neuropsiquiátricos son el más consistente e importante predictor de trastornos psicológico tanto en los fa- miliares cuidadores.
Reducir estos síntomas puede mejorar el bienestar del cui- dador y a la inversa el alivio de la sobrecarga puede disminuir los síntomas neuropsiquiátricos considerablemente.
Mejorar la habilidad del cuidador para interactuar con la persona con demencia puede prolongar el cuidado en casa y mejorar la calidad de vida de ambos.
La intervención con cuidadores ha probado ser efectiva al aumentar el conocimiento del cuidador con respecto a esta patología y por lo tanto reducir la sobrecarga y los síntomas neuropsiquiátricos del paciente.
Tratamiento medicamentoso
No hay una indicación medicamentosa aprobada para el tratamiento de los SPCD, como ya lo hemos mencionado, y aquellos con los que contamos ofrecen riesgos que deberán ser discutidos con el paciente, los familiares y el cuidador. No olvidemos que los SPCD pueden tener un curso limitado en el tiempo y desaparecer, por lo que se revisará con frecuencia su indicación, así como su suspensión cuando no sean nece- sarios. Las opciones farmacológicas generalmente se enfocan en el grupo más problemático de síntomas. En la actualidad, hay pocos medicamentos que han demostrado cierta utilidad en el tratamiento de los SPCD y aclaramos desde ya que hay síntomas en que la medicación es ineficaz. Nos referimos a la hostilidad, falta de cuidado personal, problemas de me- moria, inatención, verbalizaciones repetitivas, deambulación errática (4). En estos la probabilidad de mejoría es menor, o se realiza a costa de importantes efectos adversos no desea- dos, especialmente sedación y rigidez como se aprecia con los antipsicóticos. Cuando no hay respuesta, no está indicado subir la dosis a rangos superiores a los aconsejados ya que su resultado es solamente la disminución de sus manifestacio- nes motrices, pero no los efectos psicológica de estos sínto- mas, existiendo el peligro de entrar en el campo de la llamada sujeción farmacológica o química (6). Esta se define como: cualquier prescripción medicamentosa para SPCD que no se haga desde un diagnóstico neuropsiquiátrico definido (evitar
la hiperactividad motora, o para que el paciente deje de hacer preguntas repetidas). También se incluyen aquellas prescrip- ciones que se hacen por causas organizativa, como son: forzar la permanencia en la cama del paciente, o para que deje de gritar o deambular, e inclusive para asegurar el descanso de los profesionales del turno de la noche de la institución o de los cuidadores.
De esta manera se logra minimizar las conductas que se consideran molestas para el entorno, sin tener en cuenta un diagnóstico de su etiología y por lo tanto un correcto trata- miento.
Si bien la recomendación es la monoterapia, muchas veces se debe probar con diferentes medicamentos para que remita el cuadro y en algunas situaciones se hará necesario la com- binación de más de uno.
Su indicación es en dosis más bajas que en la población general, y se aumentará en forma lenta hasta la remisión del síntoma, vigilando la posible aparición de efectos adversos, y su eficacia. Recordemos que los adultos mayores tienen di- ferencias con el resto de la población tanto en la absorción como en la distribución, metabolismo y eliminación de los medicamentos.
Se reevaluará la respuesta, mediante entrevista clínica en la que participe la familia o cuidadores habituales, o mediante herramientas de evaluación.
Los medicamentos más utilizados son: inhibidores de la colinesterasa y memantina, antipsicóticos, antidepresivos, estabilizadores del estado de ánimo y benzodiazepinas. El be- neficio a largo plazo de estos medicamentos no está claro, por lo que se recomienda su desprescripción teniendo en cuenta siempre, en la evaluación clínica, la no reincidencia de los síntomas.
Se recomiendan los siguientes medicamentos en base a las investigaciones y las guías de tratamiento dependiendo de que tipo de síntoma se quiera tratar.
Psicosis: delirios, trastornos de identificación y alucinaciones Inhibidores de la colinesterasa (ICE):
Los ICE o anticolinesterásicos, donepezilo, galantamina, rivastigmina y la memantina son recomendados como trata- miento específico de la progresión del deterioro cognitivo de la demencia.
Los ICE están aprobados para demencia leve-moderada y la memantina para demencia moderada o grave, o en demencia leve si hay intolerancia o contraindicación a ICE. Pueden uti- lizarse de forma combinada. Su papel para controlar los SPCD es controvertido. Se ha postulado que mejoran los síntomas preexistentes y que pueden prevenir la aparición de nuevos SPCD si se inician de forma precoz, sobre todo rivastigmina (en demencia con cuerpos de Lewy). Los ICE son más eficaces en depresión, apatía y conducta motora aberrante (7) y la me- mantina más útil en agitación, irritabilidad y delirios. Los ICE pueden ser efectivos para tratar la apatía en la Enfermedad de
Alzheimer (EA) y para disminuir o prevenir los síntomas psicó- ticos, sobre todo las alucinaciones tanto en la EA, como en la demencia con cuerpos de Lewy (8). No están recomendados en demencia frontotemporal (9) porque pueden producir agi- tación. Tampoco se ha demostrado mejoría de los SPCD en la demencia vascular (10). Mejoran las alucinaciones visuales.
Dentro de sus efectos adversos se destacan: náuseas, vómi- tos y diarrea, cefalea, mareos, bradicardia, confusión, dismi- nución del apetito, pérdida de peso.
Antipsicóticos
Han sido los medicamentos más recetados, pero producen aumento en la mortalidad y eventos adversos, por lo que no se deberían indicar a menos que el paciente tenga agitación, alucinaciones o delirios y siempre y cuando no hayan sido efectivos los ICE. Tampoco están indicados en los falsos re- conocimientos por ser inefectivos ni en los síntomas leves no perturbadores, y con cautela en las alucinaciones dado que pueden resolverse de forma espontánea El tratamiento se debe iniciar por dosis bajas, e ir revisándolo a intervalos regulares (cada 6 semanas o según necesidades clínicas) y limitándolo al menor tiempo posible (4 semanas si no hay respuesta, 4 meses si hay respuesta).
También se usan en dosis bajas en demencia vascular o mixta y en demencia con enfermedad de Parkinson ajustándo- se antes la medicación específica. Sus efectos adversos más frecuentes tanto de los típicos como los atípicos son: riesgo de mortalidad, deterioro cognitivo, sedación, dificultad en la marcha, caídas, mayor riesgo de accidente cerebrovascular, prolongación del intervalo QTc, efectos adversos metabólicos y efectos extrapiramidales, (sobre todo con dosis altas y en personas de edad avanzada que tengan un deterioro cognitivo y enfermedad vascular) (11). Su rango de dosis se calcula entre la mitad y la cuarta parte de la habitual. En los pa- cientes con riesgo cardiovascular, se debe realizar un ECG previo para poder vigilar cambios en el intervalo QTc, y más estrechamente a los pacientes con antecedentes de ictus. Si aparecen efectos adversos significativos, debe evaluarse el riesgo/beneficio y manejar la posibilidad de su retirada. La APA recomienda no utilizar antipsicótico inyectable de acción prolongada, salvo en pacientes con diagnóstico de trastorno psicótico crónico previo.
Las guías y revisiones recomiendan el uso de antipsicóticos
solo en situaciones puntuales intentando evitar su uso pro- longado.
Los atípicos
En estos los efectos extrapiramidales son menos frecuentes, pero pueden empeorar la motricidad, por lo que se deberá tener precaución en pacientes con demencia con cuerpos de Lewy y demencia por enfermedad de Parkinson (5).
Los más estudiados son la risperidona, la quetiapina, la olanzapina, la clozapina, el aripiprazol y los que están en es- tudio aún: el brexpiprazol que no afecta la esfera motora (en fase 3 de investigación) y el Lumateperone (con acción presi-
nática y posinapatica).
La risperidona y el aripiprazol serían los más indicados, mientras que la olanzapina se la recomienda para pacientes con efectos adversos a estos o con disminución del apetito y alteraciones del sueño.
El aripripazol podría ser el antipsicótico atípico más seguro y eficaz (12).
La elección del empleo de uno u otro dependerá de la va- loración individualizada entre riesgos y beneficios. Tanto la quetiapina como el aripiprazol tienen menos riesgo de eventos cerebrovasculares, producen menos efectos extrapiramidales y podrían ser los antipsicóticos más recomendados en pacien- tes con antecedentes de patología cardiovascular o con rigidez (enfermedad de Parkinson o demencia con cuerpos de Lewy). La risperidona (0,125 mg/día a 0,25 mg/día) tiene menos riesgos de producir caídas o fracturas, menor incontinencia y mortalidad; aunque está asociada, como la olanzapina, a eventos cardiovasculares. La risperidona podría estar indicado para los SPCD en demencias sin parkinsonismo asociado.
La quetiapina es la más sedativa y la que ocasiona más somnolencia (no debe usarse para el tratamiento del insom- nio) pero como efectos adversos tenemos el síndrome metabó- lico, hipotensión ortostática, cierta alteración motriz. A pesar de lo antedicho en pacientes portadores de Enfermedad de Parkinson (EP) o de deterioro cognitivo leve (DCL) la recomen- dación es usar antipsicóticos que provoquen menos bloqueo de receptores D2 como son la quetiapina y la clozapina.
El antipsicótico pimavanserina, cuyo rango terapéutico está situado entre 17 mg/día–34 mg/día (agonista inverso y anta- gonista del receptor de serotonina 5-HT2A con una alta afi- nidad de unión del receptor 5-HT2C), carece de acción a ni- vel del bloqueo de receptores dopaminérgicos, pero solo está aprobada en el tratamiento de la psicosis de la enfermedad de Parkinson. Hay algunos estudios que muestran que podría ser efectiva en algunos síntomas psicóticos de los pacientes con demencia (13). Como efecto adverso se destaca el aumento del riesgo de mortalidad y la prolongación del intervalo QTc.
La clozapina tiene poca interacción con receptores dopa- minérgicos y buen control de los SPCD, pero provoca mucha sedación, alteraciones metabólicas (junto con la olanzapina es la que más lo provoca), y está sujeta al programa de far- macovigilancia intensivo por su alta probabilidad de producir leucopenia y agranulocitosis. Está indicada, así como la que- tiapina, en psicosis en enfermedad de Parkinson.
Los típicos
El que tiene mayor cantidad de estudios es el haloperidol, pero hoy no se recomienda como primera línea de tratamiento. No hay diferencias en cuanto a eficacia frente a agitación en comparación con los atípicos en dosis de 0.25 a 6 mg/día, pero solamente la tercera parte de los pacientes tienen algún beneficio. Está indicado solo en situaciones muy especiales por la agudeza del cuadro o por no responder a otros medicamentos. Si se decide su administración, se debe tener en cuenta, evitar su uso prolongado dada la frecuencia de efectos adversos. Otros antipsicóticos típicos se usan también de for- ma puntual (clorpromazina, levomepromazina, flufenazina), pero están menos recomendados
Los antidepresivos
La evidencia sobre su eficacia es contradictoria ya que es difícil distinguir los síntomas prodrómicos de la demencia de los síntomas de la depresión.
Están indicados en el tratamiento de la depresión, de los trastornos de sueño y de la agitación, la impulsividad, la an- siedad, la irritabilidad. Los más utilizados son los inhibidores selectivos de la recaptación de serotonina (ISRS) citalopram, sertralina, trazodona, mirtazapina.
Un ensayo sobre el uso de citalopram en pacientes con Al- zheimer (3) mostró eficacia, en la agitación, en el malestar del cuidador, en el desempeño de las actividades de la vida diaria y en la reducción en el uso de medicación de rescate, pero produjo empeoramiento en el deterioro cognitivo, y alte- raciones en el intervalo QTc por lo que no se recomienda su uso por encima de los 20mgr al día. Hay algún estudio que indagó al Es citalopram en comparación con el citalopram y si bien tiene menos repercusión en el intervalo QTc igual la tiene por lo que no está exento de riesgo. (14). Algunas evidencias muestran ventajas en el uso de Trazadona en dosis de 12,5 a 25 mgr. dos veces al día para la agitación (3).
También se usan los duales y los multimodales como son la venlafaxina, desvelafaxina, duloxetina, tianeptina, vortioxetina. Con respecto a los tricíclicos, (amitriptilina, nortriptilina, imipramina, clomipramina) no están recomendados ya que producen muchos efectos deletéreos tanto en la cognición, como en otras muchas funciones, por sus efectos anticolinér- gicos (sequedad de boca, estreñimiento, retención urinaria, antagonizan los efectos de los ICE), como también lo hace la paroxetina. Sus efectos secundarios antiadrenérgicos, produ- cen hipotensión postural y mareos, por lo que aumentan el
riesgo de caídas (15).
Depresión
Los antidepresivos no deben considerarse como primera línea de tratamiento de la depresión leve o moderada en pa- cientes con demencia ya que su eficacia es muy escasa. Los recomendados son el citalopram, sin superar dosis de 20 mg por su efecto sobre el intervalo QTc y por los trastornos cog- nitivos que puede provocar y la sertralina. Hay pocos trabajos que muestran buenos resultados con el uso del es citalopram, pero también puede indicarse. Cuando se decida la utilización de un medicamento se hará teniendo en cuenta que pueda tratar varios síntomas a la vez si estos se presenten en for- ma concomitante. Un ejemplo es la depresión y/o ansiedad cuando asociada con falta de apetito, en este caso la elección puede ser la Mirtazapina o cuando hay dolor neuropático cuya indicación será la duloxetina (13).
No parece haber diferencias importantes entre los ISRS, mirtazapina, venlafaxina, antidepresivos tricíclicos y el placebo, aunque la tasa de remisión de depresión a las 6-12 se- manas es algo mayor con el uso de ellos. Estos medicamentos están relacionados con más abandonos del tratamiento y más efectos adversos (sequedad de boca, mareos). En los casos de depresión mayor severa, o cuando la depresión leve-moderada no mejora con intervenciones no medicamentosa, o hay una asociación de una patología mental previa que tuvo respuesta a antidepresivos, se recomienda su administración vigilando la aparición de efectos adversos (4, 5). En depresión leve o moderada, se sugiere vigilancia hasta las 12 semanas, ya que puede haber remisión espontánea de los síntomas e indicar intervenciones no medicamentosas como son la estimulación cognitiva, ICE e interacción social
Aquellos medicamentos con múltiples mecanismos de ac- ción como son la venlafaxina, desvenlafaxina, duloxetina, mir- tazapina y tianeptina o vortioxetina, tienen mayor eficacia que el resto en la depresión geriátrica mejorando la función cogni- tiva y siendo muy bien tolerados. Se administran a la misma dosis y en la misma duración que en pacientes sin demencia. Los síntomas depresivos pueden empeorar la progresión del deterioro cognitivo por lo que no es conveniente retrasar exce- sivamente el tratamiento medicamentoso (16).
Una vez indicado el tratamiento con antidepresivos en pa- cientes cursando una depresión, se deben mantener durante 1 año, luego del cual se retiran en forma lenta para evitar el síndrome de discontinuación sobre todo en aquellos de vida media más corta (venlafaxina, desvenlafaxina, paroxetina). Cuando aparece una recaída posterior se debe considerar su uso en forma permanente (8).
Apatía
Definida como el estado de desinterés y falta de motivación o entusiasmo en que se encuentra una persona que comporta indiferencia ante cualquier estímulo externo. En la apatía, a diferencia de la depresión, es el cuidador o la familia que hacen referencia a este síntoma, mientras que el paciente no re- porta ningún cambio en su estado. No obstante, es importante considerar que existen cierta sobreposición entre la apatía y la depresión, como son la pérdida de interés en las actividades, la anergia, el enlentecimiento psicomotor, la fatiga y la disminución de la introspección.
Es el síntoma de aparición más temprana, más prevalente y estable (48 al 92% de los pacientes la presentan). No responde a la administración de antidepresivos ISRS por lo que en el caso de que se hayan indicado por otra causa hay que evaluar la posibilidad de su retiro o la reducción de su dosis. Si se asocia apatía y síndrome depresivo, se deberá usar antidepresivos de tipo noradrenérgicos y, en especial dopaminérgicos como es el bupropión, vigilando su potencial aumento de la presión arterial y su efecto proconvulsivante. También se pue- den administrar ICE, metilfenidato, modafinilo o atomoxetina. El metilfenidato puede demostrar eficacia en el tratamiento de la apatía y puede tener beneficios leves para la cognición y el rendimiento funcional en los pacientes con EA, aunque este resultado se asocia con evidencia de baja calidad.
Trastornos del sueño
No hay muchos estudios que apoyen el uso de antidepre- sivos para los trastornos del sueño. Los que se han utilizado con mayor frecuencia, cuando fallan las medidas no medica- mentosas, son los de perfil sedativo a dosis bajas como son 15mgr. de Mirtazapina, o 50 mgr. de Trazodona. Sin embar- go, la guía NICE, 2018 no lo recomienda.
No es menor que el uso de antidepresivos mejore los aspec- tos que tienen que ver con los cuidados del paciente como se ve con la administración de Mirtazapina, mejorando la sobre- carga del cuidador y de hecho también los SPCD (17).
Agitación
Los ISRS (sertralina y citalopram) han demostrado similar o mayor eficacia que los antipsicóticos y el placebo en pacien- tes con EA, pero no en pacientes con demencia por cuerpo de Lewis.
Ansiolíticos e inductores del sueño
Lamentablemente su uso es muy extendido tanto en su frecuencia como en el tiempo de administración a pesar de que han demostrado sus efectos adversos (tolerancia, depen- dencia, síndrome de abstinencia, caídas, fracturas, deterioro cognitivo) (18).
La recomendación general es evitar su uso en pacientes con deterioro cognitivo y demencia, por lo que, cuando el paciente los tiene indicados, se intentará su retiro en forma gradual y lenta para evitar el síndrome de abstinencia que pueden generar. Su indicación se hace cuando ya se han tratado las posibles causas de insomnio y este no responde. Se deberán utilizar las de vida media corta, como el lorazepam por pe- riodos breves entre 1 a 3 semanas y en dosis bajas (0,5 mg) evitando las de vida media más larga como son el Diazepam y el Clonazepam (6).
El lorazepam o la zopiclona siempre en dosis baja puede ser útil para prevenir o reducir la agitación en situaciones es- tresantes (19) Se deben utilizar la dosis efectiva más baja posible, y siempre es mejor la vía oral que las otras formas de administración. La vía intramuscular se reserva solamente en situaciones de emergencia siempre que no hayan resultado otras alternativas como el haloperidol o la olanzapina IM.
Una nueva clase de hipnóticos se han investigado para el mantenimiento del sueño (Suvorexant y Lemborexant). Los re- sultados han mostrado cierta eficacia como con el suvorexant en dosis de 10 a 20 mgr. en pacientes con EA leve, pero puede provocar somnolencia diurna (20).
La melatonina y el ramelteón (agonista selectivo del receptor de melatonina). se ha usado para el insomnio debido a su buen perfil de seguridad, pero no demuestra ser muy eficaz (21).
La melatonina podría ser utilizada en el trastorno del sueño
REM en personas con demencia por enfermedad de Parkinson o demencia con cuerpos de Lewy (5) Es bien tolerada y no tiene efectos adversos sobre la cognición, ni sobre actividades de la vida diaria. Tiene bajo potencial de abuso y no tiene síntomas de abstinencia significativos. Sin embargo, puede producir sueños anormales, irritabilidad y sedación residual durante el día, por lo que hay que tener precaución en los pacientes con riesgo de caídas (22).
Antiepilépticos o estabilizantes del humor
Gabapentina y pregabalina se han usado en pacientes con demencia para tratar la agitación y la agresividad, pero pue- den producir mareos, somnolencia y falta de coordinación mo- tora que aumentan el riesgo de caídas. Son muy usados como alternativa para el tratamiento de la ansiedad o insomnio (75- 150 mg de pregabalina por la noche) (23).
El valproato se ha usado en el tratamiento de la agitación/ agresión (24), pero no ha mostrado eficacia y está asociado a efectos adversos. No se debe utilizar a menos que esté indica- do para otra afección concomitante como en la exaltación del humor en paciente con patología previa (5).
La carbamazepina en dosis de 300-400 mg demostró cier- ta efectividad en síntomas como la agresión (25), pero tiene muchos efectos adversos e interacciones con otros medica- mentos No se recomienda de rutina por su toxicidad hemato- lógica y las posibles interacciones con otros fármacos usados en estos pacientes.
El levetiracetam y lamotrigina se utilizan en pacientes con EA y epilepsia. La lamotrigina ha evitado el aumento de la dosis de antipsicóticos en la agitación (26).
Conclusiones
Siguiendo los modelos biopsicosociales del enfermar dire- mos que, en la génesis de los trastornos cognitivos, como en cualquier otra patología, intervienen factores genéticos, am- bientales y también psicológicos.
Aún hoy no podemos intervenir en los genéticos, pero si en los factores epigenéticos, psicológicos, ambientales y sociales Sabemos que más del 90% de los pacientes demenciados tiene algún SPCD y que su tratamiento es complejo, debiendo implementar medidas adecuadas no solo con el paciente sino
también en el binomio que forma este con su cuidador.
El primer paso de nuestra intervención incluye: diagnóstico y tratamiento de enfermedades intercurrentes, intervención en factores ambientales, físicos e intervenciones no medica- mentosas.
Estas cuentan con la mayor evidencia que apoya su utilidad para la reducción de los SPCD, y se centran sobre todo en el entrenamiento en habilidades de resolución de problemas. La Indicación del uso de medicamentos tiene que ver con la falta de respuesta a las estrategias no medicamentosas o con la intensidad de la sintomatología. Decidido esto se reco- mienda: ajustar los medicamentos al grupo de síntomas más
problemático, utilizar la dosis menor posible e intentar reducir la dosis gradualmente. Son de primera línea cuando hay idea- ción suicida, psicosis y agresión, pero no son efectivos en los problemas de la memoria, la inatención, las verbalizaciones repetitivas, ni en la deambulación errática
Dentro de los tratamientos farmacológicos, los antipsicóti- cos son ampliamente utilizados. Los estudios han demostrado cierta eficacia en el tratamiento de los síntomas psicóticos y en la agitación/agresividad, pero también efectos adversos como, el aumento en la mortalidad, los ictus y otros efectos secundarios como parkinsonismo. Los de mejores resultados los tienen la risperidona (el más estudiado de todos) el aripi- prazol y la olanzapina.
Su uso queda limitado a pacientes con agitación o psicosis grave que suponga un riesgo para la salud, tanto de ellos como para sus cuidadores.
En el caso de tener que utilizarlos se deberá explicar a la familia, el por qué se han indicado, así como los riesgos y beneficios que conllevan, informándoles además que tienen un horizonte temporal de retirada (27).
Siguiendo estas pautas, diremos que cuando a las 4 sema- nas de su administración no hay respuesta, se deberán sacar gradualmente y si hay respuesta se esperará 4 meses para su retiro que será gradual y siempre vigilando la aparición de efectos adversos o de reincidencia de las SPCD. Que hayan re- mitido no significan que no vuelva a aparecer. En este caso, y habiendo transcurrido cuatro meses desde su desprescripción se evaluará la posibilidad de indicarlos a permanencia.
Nunca utilizar antipsicóticos de depósito a no ser que el paciente los reciba con anterioridad por enfermedades psi- quiátricas previas.
Dentro de los antidepresivos los que cuentan con más estu- dios son los IRSS entre ellos la sertralina y el citalopram que han demostrado escasos resultados con respecto a placebo. No se indican en pacientes con apatía por no ser eficaces en esta. Con respecto a los ICE mostraron modestas mejorías con respecto al placebo y no hay diferencias significativas entre ellos, pero si hay que tener en cuenta sus efectos adversos.
La memantina ha mostrado cierta eficacia y su efecto adverso más corriente es la sedación.
Con respecto tanto a las BZD y los estabilizadores del hu- mor no han demostrado efectividad, pero producen muchos efectos adversos por lo que se reservan solo en situaciones puntuales (agitación aguda para las BZD o episodios de exal- tación del humor para los estabilizantes).
En síntesis
Un algoritmo de tratamiento simplificado sería:
- Usar siempre primero las estrategias no medicamentosas que se deben continuar, aunque se haya decidido agregar me- dicamentos.
- Evaluar la gravedad de la demencia. Si es leve o moderada
se tratará con ICE, si es moderada a severa, con ICE y Memen- tina. retrasando así el deterioro cognitivo y con él la presencia de los SPCD.
- Definir los grupos de síntomas que se van a tratar eligien- do en primera instancia aquellos que causen mayores moles- tias en el paciente, cuidador, familia o en su entorno.
- Tanto la depresión como la ansiedad, la agitación o la agresividad se tratarán con IRSS (citalopram o sertralina). Los antidepresivos con múltiples mecanismos de acción tienen mayor eficacia en la depresión geriátrica mejorando la función cognitiva y son bien tolerados.
- Si el paciente cursa con exaltación del humor se elegirán estabilizantes como el divalproato o la carbamazepina.
- Si el paciente tiene sintomatología psicótica se indica- rán antipsicóticos atípicos como la risperidona, aripiprazol u olanzapina.
- Para la agitación la indicación es la trazodona o ISRS.
- Si hay trastornos del sueño se tendrá en cuenta la higiene del sueño como primera medida. No usar BZD, ni quetiapina, la melatonina se indica en trastorno del sueño REM en perso- nas con demencia por enfermedad de Parkinson o demencia con cuerpos de Lewy.
- Siempre usar monoterapia.
- Cuando no hay respuesta a la medicación se retira a las 4 semanas en forma gradual, evaluando la posibilidad de apari- ción nuevamente de los síntomas.
- Si hay respuesta se retira a los 4 meses en forma paulatina teniendo presente la posibilidad de su reinstalación.
- Solo se combinan medicamentos si no hay respuesta o si el paciente tiene varios síntomas concomitantes.
- Se deberá evaluar los efetos adversos y control de los ries- gos cerebrovasculares y cardiovasculares, como la hiperten- sión arterial, la diabetes, y la fibrilación auricular.
- En el caso de que luego de 4 meses haya reaparición de la sintomatología, se volverá a indicar el tratamiento medi- camentoso evaluando la posibilidad de que este sea por un largo período.
Y para finalizar, la demencia es una enfermedad crónica e irreversible y dentro.
de sus factores de riesgo destacamos la baja educación, la obesidad, consumo de alcohol, la depresión, el aislamiento social, la inactividad física, la diabetes, problemas auditivos y motrices y hasta la polución ambiental.
Como vemos hay un 50% de los factores de riesgo que pue- den ser modificables mediante políticas preventivas en salud, pero que implican la inversión de recursos económicos que en la mayoría de nuestros países latinoamericanos no están asignados para estos rubros.
Será necesario y un desafío entonces, el implementar estra- tegias que impidan que seamos, analfabetos, pobres, viejos y “locos”.
Bibliografía
- 1. Alzheimer’s Association. (2021). 2021 Alzheimer’s Disease Facts and Figures. Alzhei- mer’s Dement. https://www.alz.org/media/Docu- ments/alzheimers-facts-and-figures.pdf
- 2. Hodgson, N. A., Gitlin, L. N., Winter, L., & Czekanski, K. (2011). Undiagnosed illness and neuropsychiatric behaviors in community residing older adults with dementia. Alzheimer disease and Associated Disorders, 25(2), 109–
115.
- 3. Gerlach, L. B., & Kales, H. C. (2020). Ma- naging behavioral and psychological symptoms of dementia. Clinics in Geriatric Medicine, 36(2), 315-327.
- 4. Herrmann N, Lanctôt KL, Hogan DB. Phar- macological recommendations for the symp- tomatic treatment of dementia: the Canadian Consensus Conference on the Diagnosis and Treatment of Dementia 2012. Alzheimers Res Ther. 2013;5 Suppl 1:S5. PubMed PMID: 24565367. Texto completo.
- 5. National Institute for Health and Care Ex- cellence (NICE). Dementia: Assessment, mana- gement and support for people living with de- mentia and their carers. London: NICE; 2018. PubMed PMID: 30011160. Texto completo.
- 6. Olazarán-Rodríguez J, López-Álvarez J, Agüera-Ortiz LF. Criterios CHROME para la acre- ditación de centros libres de sujeciones quími- cas y para una prescripción de psicofármacos de calidad. Psicogeriatría. 2016;6(3):91-8. Texto completo.
- 7. Waldemar G, Gauthier S, Jones R, Wilkinson D, Cummings J, Lopez O, et al. Effect of done- pezil on emergence of apathy in mild to modera- te Alzheimer’s disease. Int J Geriatr Psychiatry. 2011;26(2):150-7. PubMed PMID: 20597141.
- 8. Sorbi S, Hort J, Erkinjuntti T, Fladby T, Gainotti G, Gurvit H, et al. EFNS-ENS Guide- lines on the diagnosis and management of di- sorders associated with dementia. Eur J Neu- rol. 2012;19(9):1159-79. PubMed PMID:
22891773. Texto completo.
- 9. Ismail Z, Black SE, Camicioli R, Chertkow H, Herrmann N, Laforce R, et al; CCCDTD5 participants. Recommendations of the 5th Ca- nadian Consensus Conference on the diagnosis and treatment of dementia. Alzheimers De- ment. 2020;16(8):1182-95. PubMed PMID:
32725777. Texto completo.
- 10. O’Brien JT, Holmes C, Jones M, Jones R, Livingston G, McKeith I, et al. Clinical practi- ce with anti-dementia drugs: A revised (third) consensus statement from the British Associa- tion for Psychopharmacology. J Psychophar- macol. 2017;31(2):147-68. PubMed PMID: 28103749.
- 11. Sacchetti E, Turrina C, Valsecchi P. Cere- brovascular accidents in elderly people treated with antipsychotic drugs: a systematic review. Drug Saf. 2010;33(4):273-88. PubMed PMID: 20297860.
- 12. Yunusa I, Alsumali A, Garba AE, Regestein QR, Eguale T. Assessment of Reported Compara- tive Effectiveness and Safety of Atypical Antipsy- chotics in the Treatment of Behavioral and Psy- chological Symptoms of Dementia: A Network Meta-analysis. JAMA Netw Open. 2019;2(3): e190828. PubMed PMID: 30901041. Texto
completo.
- 13. McCollum L, Karlawish J. Cognitive Im- pairment Evaluation and Management. Med Clin North Am. 2020;104(5):807-25. PubMed PMID: 32773047. Texto completo.
- 14. Hasnain M, et al 2013 Escitalopram and QTc prolongation July 2013. Journal of psychiatry & neuroscience: JPN 38(4):E11 DOI:10.1503/jpn.130055 Source PubMed.
- 15. Dudas R, Malouf R, McCleery J, De- ning T. Antidepressants for treating depres- sion in dementia. Cochrane Database Syst Rev. 2018(8):CD003944. PubMed PMID:
30168578. Texto completo.
- 16. Agüera Ortiz L, Carrasco M, Sanchez Perez M (2021) Psiquiatría General Elsevier 3° Edi- ción, 223-235.
- 17. Romeo R, Knapp M, Hellier J, Dewey M, Ballard C, Baldwin R, et al. Cost-effectiveness analyses for mirtazapine and sertraline in de- mentia: randomised controlled trial. Br J Psy- chiatry J Ment Sci. 2013;202:121-8. PubMed PMID: 23258767. Texto completo.
- 18. Defrancesco M, Marksteiner J, Fleis- chhacker WW, Blasko I. Use of Benzodiaze- pines in Alzheimer’s Disease: A Systematic Review of Literature. Int J Neuropsychophar- macol. 2015;18(10):pyv055. PubMed PMID: 25991652. Texto completo.
- 19. Cummings J, Lai T-J, Hemrungrojn S, Mohandas E, Yun Kim S, Nair G, et al. Role of Donepezil in the Management of Neuropsy- chiatric Symptoms in Alzheimer’s Disease and Dementia with Lewy Bodies. CNS Neurosci Ther. 2016;22(3):159-66. PubMed PMID:
26778658. Texto completo.
- 20. Blackman J, Swirski M, Clynes J, Harding S, Leng Y, Coulthard E. Pharmacological and non-pharmacological interventions to enhance sleep in mild cognitive impairment and mild Al- zheimer’s disease: A systematic review. J Sleep Res. 2021;30(4):e13229. PubMed PMID:
33289311. Texto completo.
- 21. McCleery J, Sharpley AL. Pharmacothera- pies for sleep disturbances in dementia. Cochra- ne Database Syst Rev. 2020;(11):CD009178. PubMed PMID: 33189083. Texto completo.
- 22. Papillon-Ferland L. Should Melatonin Be Used as a Sleeping Aid for Elderly People? Can J Hosp Pharm. 2019;72(4):327-9. PubMed PMID: 31452545. Texto complete.
- 23. Supasitthumrong T, Bolea-Alamanac BM, Asmer S, Woo VL, Abdool PS, Davies SJC. Gabapentin and pregabalin to treat ag- gressivity in dementia: a systematic review and illustrative case report. Br J Clin Pharma- col. 2019;85(4):690-703. PubMed PMID:
30575088. Texto completo.
- 24. Baillon SF, Narayana U, Luxenberg JS, Clifton AV. Valproate preparations for agita- tion in dementia. Cochrane Database Syst Rev. 2018;(10):CD003945. PubMed PMID:
30293233. Texto completo.
- 25. Yeh Y-C, Ouyang W-C. Mood stabilizers for the treatment of behavioral and psychological symptoms of dementia: an update review. Kaoh- siung J Med Sci. 2012;28(4):185-93. PubMed PMID: 22453066. Texto complete.
- 26. McDermott CL, Gruenewald DA. Pharma- cologic Management of Agitation in Patients with Dementia. Curr Geriatr Rep. 2019;8(1):1-
- PubMed PMID: 31341757. Texto completo.
- 27. Canto de Hoyos, María, Garrido Araceli (2021) Tratamiento farmacológico de los sínto- mas psicológicos y conductuales de la demencia Elsevier.
Bibliografía adicional
- Abizanda Soler, P; Rodriguez Mañas, L: Trata- do de Medicina Geriátrica. 2015 Elsevier. Espa- ña; Capítulo 64, p: 501-506.
- Kabanchick A., 2022 Psicosis en la vejez fas- cículo 5 ed. Sciens.
- Kales,H; Gitlin,L; Lyketso, C: Assessment and management of behavioral and psycho- logical symptoms of dementia.: BMJ. Enero 2015;350(369): 1-17.
- Liljegren M, Naasan G, Temlett J, Perry DC, Rankin KP, Merrilees J, et al.os.6 feb. 2015 [JAMA Neurol 2015; Jan 5. [Epub ahead of print]].
- Lyketsos, C. G., Lopez, O., Jones, B., Fitzpa- trick, A. L., Breitner, J., & DeKosky, S. (2002). Prevalence of neuropsychiatric symptoms in de- mentia and mild cognitive impairment. JAMA, 288(12), 1475.
- McShane, R. (2000). What are the syndromes of behavioral and psychological symptoms of de- mentia?. International Psychogeriatrics, 12(S1), 147-153.
- Organización Mundial de la Salud. Demencia. https://www.who.int/es/news-room/fact-sheets/ detail/dementia.
- Porto V. Sarubbo L. (2019) Antipsicoticos en la Demencia: usos, riesgos y recomendaciones. Revista de Psicofarmacología, 118, 4-8.
- Seitz DP, Adunuri N, Gill SS, Gruneir A, He- rrmann N, Rochon P. Antidepressants for agita- tion and psychosis in dementia. Cochrane Da- tabase Syst Rev. 2011;(2):CD008191. PubMed PMID: 21328305. Texto completo.
- The IPA Complete Guides to Behavioral and Psychological Symptoms of Dementia (BPSD): International Psychogeriatric Association. www. ipa-online.org.
- Wancata, J., Windhaber, J., Krautgartner, M., & Alexandrowicz, R. (2003). The consequences of non-cognitive symptoms of dementia in me- dical hospital departments. The International Journal of Psychiatry in Medicine, 33(3), 257- 271.







No comments! Be the first commenter?