Trastornos del sueño. Parte III. Su tratamiento
Resumen
Desde hace algún tiempo nos han inquietado los temas relacionados con el sueño en lo que refiere a su fisiología, su fisio- patología, las consecuencias que traen aparejadas sus alteraciones, así como también lo referente a la implementación de los tratamientos que sean más efectivos teniendo en cuenta a cada individuo en particular.
Hemos expuesto, en entregas anteriores, su importancia tanto para la salud pública como también para las esferas laborales, sociales y educativas, considerando los efectos que conlleva el mal dormir en cada una de ellas.
Se ha comenzado a discutir en diferentes ámbitos, incluso en los académicos, la necesidad de acomodar las horas en que se realizan tareas que requieran de atención y concentración a los ritmos biológicos de cada individuo para favorecer un mejor desempeño.
Podemos decir, entonces, que hay en el estudio de los trastornos del sueño, muchas y diversas facetas posibles de abordar. En la segunda entrega del ciclo dedicada a estos trastornos decíamos que era necesario conocer lo referente a su neurobiolo-
gía para así poder entender mejor cuándo y cómo abordar su tratamiento.
Es por esto que, en esta tercera parte, nos dedicaremos a lo que son los ciclos biológicos y dentro de ellos, más específica- mente, los circadianos, para finalmente encarar el tratamiento de sus alteraciones.
Palabras clave
Ritmo circadiano – Sueño – Vigilia – Tratamiento de los trastornos del sueño.
Sarubbo Laura, Tamosiunas Gustavo, Bocchino Stella. “Trastornos del sueño. Parte III. Su tratamiento”. Psicofarmacología 2018;111:5-11. Puede consultar otros artículos publicados por los autores en la revista Psicofarmacología en sciens.com.ar
Introducción
El sueño es un fenómeno normal y universal asegurado y mantenido por diferentes mecanismos biológicos.
La mayoría de los seres vivos adaptan su fisiología y su com- portamiento al ciclo día – noche, lo que les asegura, entre otras cosas, la posibilidad de adaptarse a su entorno e inclu- sive preservar su seguridad.
Estudios de investigación han revelado los aspectos gené- ticos y proteicos que constituyen parte de la maquinaria mo- lecular de los relojes circadianos. Estos genes y sus proteínas producen bucles de retroalimentación y de regulación de la transcripción y traducción genética con componentes tanto excitatorios como inhibitorios, en un tiempo próximo a las 24 horas, sincronizándose con la luz. Los mecanismos de los relojes circadianos están presentes en todas las células de nuestro organismo como osciladores celulares que están guiados por un marcapaso maestro (oscilador primario) ubicado en el hipotálamo.
Se ha descripto, tradicionalmente, al sistema circadiano como un sistema unidireccional en donde la información pasa de los fotorreceptores al reloj maestro o marcapasos, este genera la señal circadiana y de aquí pasa la información a los sistemas efectores. Pero esto es solo una parte del proceso ya que también existe retroalimentación de cada uno de estos pasos para con los otros, lo que es de gran importancia cuando se plantea la terapéutica de sus alteraciones (Brusco, 2012).
Relojes biológicos
Los cambios continuos caracterizan a los organismos vivos y también a su entorno. Muchos de estos cambios no son periódicos como aquellos que son secundarios a los sistemas meteorológicos y exigirán una adaptación que no tiene que ver con una regularidad, muchos otros se repiten y se llaman ritmos biológicos, estos se definen como aquellas variaciones regulares de una función biológica que se van dando en el tiempo (Brusco, 2012).
Los llamados ritmos circadianos, como lo es el sueño y la vigilia, forman parte de estos ciclos biológicos y son aquellos que se repiten con una periodicidad de alrededor de 24 horas, (de allí su nombre en latín circa, que significa alrededor de y dies, que significa día).
En los hombres, no solo el sueño y la vigila tienen periodicidad en el tiempo, también lo tienen, por ejemplo, las variaciones en la frecuencia cardiaca, de la presión arterial, la respiración, la temperatura, la secreción endócrina. Estos relojes endógenos se sincronizan por patrones ambientales definidos como son la luz y la oscuridad, pero también por factores sociales. Entre todas las funciones que presentan una ritmicidad circadiana en el hombre, el sueño y la vigilia son las más importantes. El reloj circadiano está situado en los núcleos supraquiasmáticos (NSQ) del hipotálamo, localizados sobre la base del 3° ventrículo sobre el quiasma óptico, con un número de neuronas escaso y cuyo neurotransmisor más común es el GABA. Estos núcleos regulan la expresión rítmica del sistema cir- cadiano por medio de dos grandes vías de comunicación, el sistema endócrino y el sistema nervioso autónomo, los que cambian en función de la hora del día bajo el control de este oscilador primario.
Con respecto a cómo está conformado este bucle diremos que las aferencias más importantes que recibe el NSQ son las que provienen de la retina a través de una vía directa, la vía
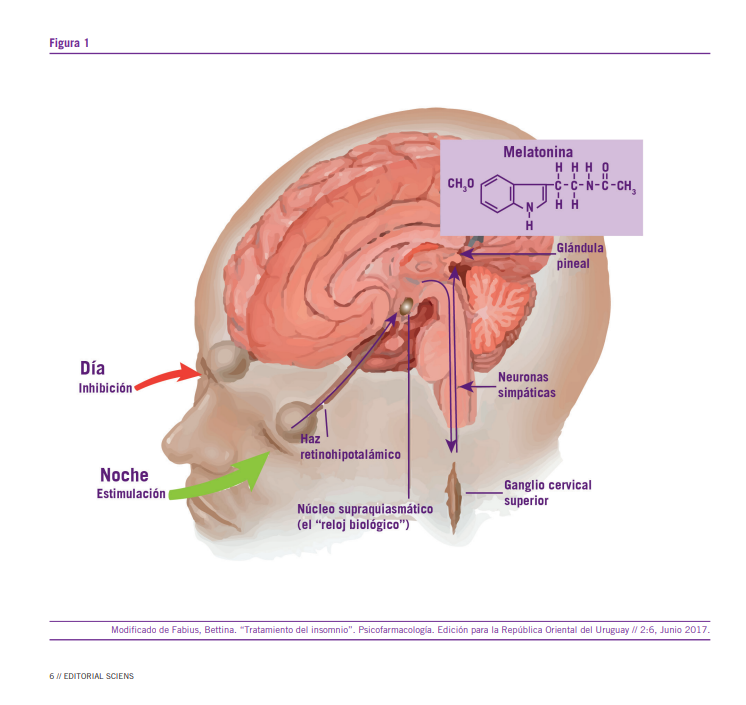
retina-hipotalámica y de una vía indirecta, la vía genículo-hipotalámica. El origen en la retina de estas proyecciones es de una población de células ganglionares que tienen, ante la luz, una respuesta con alto grado de sensibilidad, pero que no están involucradas en el análisis de la visión.
Las eferencias fundamentales de los NSQ son a otros núcleos del hipotálamo, al tálamo, a los núcleos del rafe y al área preóptica involucrados en diferentes actividades que son comandadas por el SNC.
Cuando se produce un daño en los núcleos NSQ se alteran los ritmos circadianos que tienen que ver con la ingesta de alimentos, la temperatura corporal, la actividad sexual, sueño, ritmos endócrinos (secreción de hormonas como prolactina, melatonina, corticoides) y también queda afectada la actividad locomotora. Esto nos hace suponer, y realmente ha que- dado demostrado, que los NSQ son los osciladores primarios de este complejo sistema regulatorio.
Tratamiento de las alteraciones del sueño
Un abordaje farmacológico necesariamente implicará interactuar tanto sobre aquellos neurotrasmisores que son responsables de promover la vigilia como también de aquellos responsables de inducir el sueño. Si bien nos dedicaremos principalmente al tratamiento de los trastornos más frecuentes del sueño, como es el insomnio, se hará mención también a aquellos medicamentos usados en narcolepsia o hipersomnia (Guías de insomnio, 2016; Diaz Negrillo, 2013).
Recientemente se ha puesto atención a investigaciones orientadas a que el insomnio sería más un trastorno vinculado a un aumento de mediadores de la vigilia que a una reducción o alteración de los mecanismos que provocan el sueño.
Hay datos neuroquímicos, como el aumento de noradrena- lina y cortisol en insomnes y en algunos estudios de neuroi- magen específicamente con PET realizados durante el sueño, que evidencian un mayor metabolismo de glucosa, aunque se requieren más estudios para poder confirmar esta hipótesis.
Estos hallazgos ya han llevado a la creación de nuevos fár- macos para el tratamiento del insomnio que, a diferencia de los hipnóticos clásicos que promueven aumento de sistemas inhibitorios, actúan sobre vías involucradas en la vigilia como luego veremos (Valencia, 2010; Salin, 2016).
El abordaje de los trastornos del sueño debe ser siempre integral con la inclusión de medidas de higiene del sueño, ejercicios, nutrición, apoyo psicológico o psicoterapia cuando sea necesario, entendiendo que los medicamentos son una herramienta terapéutica más, con características especiales que deben conocerse para no hacer un uso indebido de ellos. En el momento actual contamos con diferentes fármacos
Tabla 1
Recomendaciones de higiene del sueño (basado en Mastin et al., 2006)
• Evitar realizar siestas prolongadas (> 1 h) durante el día.
• Acostarse a dormir a una misma hora todos los días.
• Despertarse todos los días a una misma hora.
• Evitar consumir alcohol, cigarro y bebidas con cafeína (café, té, chocolate, refrescos de cola o bebidas energéticas) al menos 4 horas antes de dormir.
• Evitar realizar actividades sensorialmente muy estimulantes antes de acostarse (videojuegos, internet, televisión).
• Evitar irse a acostar si se está estresado, ansioso, enojado o preocupado.
• No utilizar la cama para otras actividades: leer, estudiar, comer, trabajar, etcétera.
• Dormir en una cama confortable.
• No realizar trabajo importante minutos antes de irse a dormir: trabajo, tareas, estudio.
• Evitar pensar sobre sus actividades del día u organizar y planear sus actividades futuras mientras trata de dormir.
• Dormir en una habitación con baja iluminación y poco ruido ambiental.
Modificado de Neurobiología del sueño y su importancia: antología para el estudiante universitario Carrillo P. que han demostrado su utilidad en trastornos del sueño y habitualmente sus efectos farmacológicos son rápidamente percibidos por el paciente ya que tienen rápido inicio de acción, son de elevada potencia (entendiéndose esta como la relación entre la dosis y el efecto obtenido) y es reproducible dicho efecto en sucesivas tomas. Sin embargo, hemos aprendido algunas lecciones desde su introducción en el mercado hace más de 50 años, cuando se inicia la moderna psicofarmacolo- gía. En primer lugar, debemos diferenciar el efecto hipnótico agudo del pretendido efecto terapéutico en el trastorno del sueño. El efecto hipnótico es un efecto que podríamos llamar sintomático y no aborda la causa del trastorno ni modifica su evolución, aunque su uso por meses o años no parece ser una conducta racional, lamentablemente, es aún muy frecuente.
Esto del punto de vista clínico, pero desde la perspectiva farmacológica tampoco es racional, ya que en un tiempo más o menos reducido (2 a 3 semanas) se produce tolerancia a dicho efecto y farmacodependencia.
Desde la perspectiva de la prevención cuaternaria debemos tomar en cuenta no solo el tratamiento integral y cuidar las indicaciones, sino especialmente evitar el uso prolongado, ya que ha demostrado más riesgos que beneficios.
En este sentido, al iniciar la terapia con hipnóticos debe establecerse un acuerdo con el paciente para que conozca que será un tratamiento acotado y que, incluyendo la desha- bituación, no pasará de 2 o 3 meses.
En todo momento deberá incluirse todas las medidas de higiene del sueño y descartar situaciones que ameriten un abordaje clínico específico (Chávez, 2017).
Los principales fármacos empleados en el tratamiento del insomnio son los moduladores alostéricos del receptor GABA A tanto benzodiacepínicos como no benzodiacepínicos o también conocidos como fármacos Z.
También se han utilizado otros fármacos en situaciones especiales como antihistamínicos, melatonina, algunos antidepresivos, antipsicóticos e incluso algunos antiepilépticos como la gabapentina y pregabalina. Asimismo, se utilizan extractos de hierbas como passiflora y valeriana entre las más frecuentemente empleadas. Gracias al avance en neurociencia y en psicofarmacología estamos entendiendo mejor el mecanismo de acción de estos fármacos, pero también nos ha permitido explicar por qué algunos fitoterápicos o antialérgicos son útiles en el manejo de síntomas de insomnio. Debemos comprender, además, que existen muchas situaciones que involucran problemas para conciliar o mantener el sueño sin constituir necesariamente un trastorno del sueño. Por ejemplo, el tiempo que lleva de iniciado la alteración del sueño es una variable importante ya que para hablar de insomnio crónico deben trascurrir al menos 3 meses y debe tener una frecuencia de al menos 3 veces en la semana.
Otro aspecto a considerar es que para hablar de insomnio
deben cumplirse otras condiciones, como dificultad para conseguir un sueño satisfactorio en tiempo o calidad, deterioro funcional durante el día, que por tanto interfiere en la vida funcional del sujeto (tanto sea en lo social, académico o laboral).
Por otro lado, existen muchas situaciones médicas, y de consumo de sustancias o medicamentos que alteran el dormir y tampoco constituyen un trastorno. Probablemente, el considerar al fármaco como herramienta fundamental y, especial- mente, no tomar en cuenta estos aspectos diagnósticos del insomnio ha llevado a que su uso haya sido no solo extenso sino también inadecuado.
Retomamos lo que dijimos al inicio, el abordaje debe ser integral y la elección del fármaco muy cuidadosa dado nuestro aprendizaje del mal uso de hipnóticos a largo plazo, urgencia de salud pública a nuestro entender que urge atender (Speranza, 2015).
Tenemos dificultades para encontrar el hipnótico ideal por varias razones. Razones de índole fisiológicas, fisiopatológi-
Tabla 2
Neurotrasmisores que participan en vigilia principalmente Neurotrasmisores que participan en el sueño
Noradrenalina Gaba
Dopamina Adenosina
Serotonina Melatonina
Orexinas Galanina
Histamina
Acetilcolina
cas, neuroquímicas, clínicas, diagnósticas, en las evidencias que disponemos, y farmacoterapéuticas (es decir, vinculadas al perfil farmacológico y terapéutico de los fármacos usados). Existe una gran variabilidad en relación al sueño a lo largo de la vida, a variaciones vinculadas al sexo, a la arquitectura del sueño (todos los hipnóticos la alteran). Por lo tanto, desde este nivel fisiológico no podremos hablar del hipnótico ideal sino de medicamentos que deberán ajustarse a las peculiari- dades señaladas.
Un hipnótico no será del mismo valor si se trata de un sujeto de edad avanzada con escasa actividad a otro en edad laboral activa. Igualmente, en un mismo sujeto existen cambios en su actividad física, emocional o nutricional que lo hacen dife- rente (Jufe, 2007).
Desde un punto de vista clínico y dado estas variabilidades inter e intraindividuales es que decimos que no contamos (probablemente no contemos por mucho tiempo) con el hipnótico ideal.
Ahora bien, debemos diferenciar el efecto sedante del efec- to hipnótico. La sedación es un estado de menor actividad, cierta somnolencia, disminución de la vigilia y del estado de alerta. Por el contrario, los hipnóticos producen un nivel de re- ducción de la actividad induciendo un estado de somnolencia que permite inducir y mantener el sueño. Muchos fármacos tienen efectos sedantes aunque no son hipnóticos propiamen- te dichos.
Cuando consideramos los conceptos que hoy definen el insomnio (la calidad del sueño y de la actividad diurna posterior) nos encontramos que muchos de estos sedantes no solo no llegan a producir un verdadero sueño reparador sino que sus efectos sedantes persisten al otro día. Igualmente, haremos las mismas consideraciones para los hipnóticos con acción prolongada. La elección del hipnótico debe considerar no solo las condiciones fisiológicas y fisiopatológicas, sino también la dificultad en el inicio y/o mantenimiento del sueño, los des- pertares frecuentes, o despertar en la mañana muy temprano lo que genera malestar clínicamente significativo diurno en lo social, académico o laboral (Chávez, 2017; Contreras, 2013). El otro aspecto a tener en cuenta es el neuroquímico, son muchos los mediadores y neurotransmisores que participan del ciclo sueño vigilia, por lo que también describiremos a continuación aquellos fármacos que pueden modularlos (Diaz, 2013; Franco-Perez, 2012). Al analizar los diferentes media- dores del ciclo sueño vigilia comprendemos, en primer lugar, que existe una fina regulación en donde participan numerosos neurotrasmisores que facilitan o mantienen la vigilia y otros que inducen el sueño, inhiben la vigilia o facilitan la entrada a las diferentes fases de aquel (sea etapa de sueño REM o no Rem). Además, hay un mecanismo de cooperación en don- de algunos mediadores son necesarios, pero no suficientes para mantenerse en determinada etapa o fase. Las múltiples conexiones con diferentes estructuras cerebrales, que incluyen la amígdala, el hipotálamo y la corteza, muestran una vez más las complejas redes neuronales que se emplean y en la que participan estos mediadores coparticipando, facilitando y amplificando respuestas o bien disminuyéndolas, así como modificando otras funciones, propias de las diferentes vías que se ponen en funcionamiento.
Por tanto, la tan mentada y buscada especificidad farmacológica no se adapta a estos nuevos modelos de la neurociencia y de la integración psiconeuroendócrino metabólico e inmunológico actuales. En la tabla siguiente exponemos algunos ejemplos representativos.
El sistema noradrenérgico (NA) participa en forma importante en activación y mantenimiento de la vigilia.
Desde el locus ceruleus (principales concentraciones de nú- cleos de NA) se proyectan hacia el cerebro anterior las fibras eferentes noradrenérgicas que tienen un máximo de descargas en la vigilia, mínima en la fase 3 y nula actividad en etapa de sueño REM, mostrando tener un papel importante en la vigilia y el despertar. Los agonistas NA facilitan la vigilia y, por el contrario, los antagonistas promueven generalmente el tiempo total de sueño y el sueño REM. De la misma manera, aque- llas sustancias que liberan o bloquean la recaptación de NA, como modafinilo, son empleadas en hipersomnolencia ya que ayudan a mantener la vigilia. De más está decir, que existen en la terapéutica una serie de medicamentos que modulan en forma directa o indirecta este sistema a nivel central y que, por tanto, influirá en el ciclo sueño vigilia, como algunos anti- hipertensivos o alfa bloqueantes para la hipertrofia prostática o antigripales.
El bupropión antidepresivo, utilizado frecuentemente en tratamiento de deshabituación nicotínica, presenta efectos noradrenérgicos al inhibir recaptación de aminas, como noradrenalina y dopamina, y pude generar también insomnio.
El sistema serotoninérgico, por su parte, se proyecta a diferentes zonas del cerebro a partir de los núcleos del rafe en el tallo encefálico, participando también principalmente del mantenimiento de la vigilia con mínima actividad de estos centros durante sueño profundo y REM.
Los ISRS (inhibidores selectivos de la recaptación de serotonina) como fluoxetina y citalopram se han vinculado a aumento de la vigilia y reducción del sueño REM. Más allá que estos agentes pueden mejorar el sueño en sujetos con depresión o ansiedad, es un efecto adverso que puede aparecer y debe monitorizarse.
La acetilcolina, así como la nicotina y los agonistas muscarínicos, promueven aumento de la vigilia, además de su acción sobre el aprendizaje y la memoria. Sus proyecciones desde los núcleos se dirigen a la corteza, el tálamo, el hipotálamo y el tronco encefálico. Esto explica que el uso de done- pezilo oral empleado en tratamiento de Alzheimer debido a su acción anticolinesterasa (es decir, potenciando la acetilcolina en la sinapsis) provoca aumento de la vigilia. Asimismo los antimuscarínicos, tan frecuentemente empleados en distur- bios funcionales gastrointestinales, habitualmente producen somnolencia (así como interfieren en el aprendizaje y la memoria) aunque puede también estar participando su acción sobre receptores de histamina como veremos.
La histamina es otro neurotrasmisor que partiendo sus principales núcleos desde el hipotálamo se proyectan a práctica- mente todo el cerebro. La actividad histaminérgica es prácticamente durante las horas de vigilia estando casi sin activarse durante el sueño profundo y fase REM.
Los agonistas de H1 y H2 promueven la vigilia a expensas del sueño profundo y REM de tal manera que los antagonistas H1 inducen somnolencia y aumento el tiempo de sueño REM y sueño profundo. Los antialérgicos anti H1 provocan frecuentemente sedación y, a veces, se ha utilizado por es- tos efectos no solo en cuadros alérgicos sino para favorecer el sueño. Sin embargo, más que una acción hipnótica sería un efecto sedante. Como estos medicamentos además tienen fuertes efectos antimuscarínicos probablemente los efectos sedantes se deban a una sinérgia entre efectos antimuscarí- nicos y anti H1. Recordemos que existen otros medicamentos psicotrópicos con efectos anti H1 así como antimuscarínicos como son los antipsicóticos y antidepresivos aunque con diferencias entre ellos en cuanto a la sensibilidad para modular estos sistemas.
La adenosina, no siendo un neurotrasmisor, es un mediador que modula el sueño. Aumenta su concentración en el cerebro durante la privación de sueño y restablece sus valores luego de su recuperación.
Podría explicar la somnolencia en momentos de vigilia duradera. Debido al papel modulador de la neurotrasmisión a nivel presináptico se ha hipotetizado que la adenosina promueve el sueño a través de inhibir liberación de neurotransmisores acetilcolina e histamina (que como ya vimos, facilitan la vigi- lia). De esta manera, los antagonistas de la adenosina como las xantinas que se encuentran en bebidas como té, café, mate, así como en preparaciones de dosis fijas combinadas en antigripales y antimigrañosos, producen reducción del tiempo de sueño profundo y del sueño REM promoviendo la duración del tiempo de vigilia. A fines del siglo pasado, en 1998, se descubrió un nuevo sistema de neurotrasmisión central, el sistema de las orexinas / hipocretinas a nivel hipotalámico que modulan tanto la in- gesta como el ciclo sueño vigilia.
Estos neuropéptidos que son orexígenas tienen un efecto de potenciar neuronas “de la vigilia” como son las histaminérgicas, serotoninérgicas, colinérgicas y noradrenérgicas. De esta manera, tienen un efecto de potenciar y consolidar la vigilia.
Tienen un tipo de descarga tónica durante la vigilia y redu- cen su actividad durante el sueño y vuelve a elevarse al final de fase REM.
Se ha visto mutación con reducción de este sistema en la narcolepsia (somnolencia excesiva) y se cuenta ya con agonistas (ALA11-orexin B) y antagonistas selectivos de subtipo 1 y 2 como el almorexant. Este último alcanzó la fase III y fue suspendido por el fabricante en 2011 por razones de seguridad. Sin embargo, el suvorexant (otro antagonista) sí fue aprobado recientemente como hipnótico en EE. UU. por la FDA y ya se cuenta en varios países de la región, aunque ha habido reportes de ANMAT de aumento de la ideación suicida que habrá que confirmar con farmacovigilancia activa (Valencia, 2010; Salin, 2016).
El GABA es el principal neurotrasmisor inhibitorio del SNC y es conocido por nosotros desde que es el sitio de acción de los hipnóticos más utilizados hoy como las benzodiacepinas así como los fármacos Z.
Las benzodiacepinas provocan disminución del tiempo de vigilia y aumento de sueño total, especialmente del sueño profundo con reducción de la latencia para su inicio. Sin embargo, como todos los anteriores producen alteración de la arquitectura del sueño. Especialmente, las benzodiacepinas reducen el sueño REM.
Sus efectos a largo plazo sobre la memoria, funciones cognitivas, caídas en sujetos de edad avanzada, las dificultades de su deshabituación y del rápido desarrollo de tolerancia se han constituido en un problema que, como dijimos, urge solucionar (Campagne, 2005).
Los llamados cronobióticos son medicamentos capaces de modificar los ritmos circadianos, dentro de estos el prototipo es la melatonina que, como sabemos, está involucrada en el ciclo sueño vigilia.
La luz a través de la retina y vía núcleos supraquiasmáticos inhibe la liberación de melatonina de la glándula pineal durante el día. Lo opuesto ocurre durante la noche en que se libera esta hormona. La luz bloquea nuevamente esta vía por neuronas glutaminérgicas. La melatonina induce el sueño a través de este mecanismo luz oscuridad, es decir, del ritmo circadiano, y es principalmente cuando existen circunstancias como la edad, cambios de uso horario, actividad laboral nocturna donde el uso de melatonina tiene su mayor beneficio especialmente en preparaciones de liberación prolongada.
Contamos con agonistas melatoninérgicos como el ramelteón aprobado como hipnótico y la agomelatina aprobado inicialmente como antidepresivo, indicado sobre todo en las alteraciones del sueño de los trastornos depresivos, sus efectos sobre ciclo sueño vigilia parecen ser más ventajosos.
Sin embargo, los efectos sobre la función hepática y la necesidad de su monitorización han reducido el entusiasmo inicial (Cardinali, 2007; Escames, 2009).
La dopamina es un neurotrasmisor involucrado en funciones motoras, endócrinas, oculares, en el mecanismo de recompensa y, además, en el ciclo sueño vigilia, por lo tanto, es un eslabón más a considerar.
Contamos con un grupo de psicofármacos muy empleados que bloquean los receptores D2 principalmente, los antipsicóticos tanto los típicos como los atípicos (aunque estos en una relación de dosis diferente), provocando sedación dosis dependiente; de hecho, fueron clasificados en su momento como tranquilizantes mayores.
Hoy, los de segunda generación como quetiapina, olanzapina y risperidona, principalmente, son utilizados para inducir el sueño más allá de sus efectos sobre la agresividad y la excitación, especialmente en personas mayores de edad. Sin embargo, no tienen un claro efecto hipnótico y sus efectos a largo plazo sobre el metabolismo, el riesgo cardiovascular y el
aumento de mortalidad nos alerta sobre un uso que se está extendiendo demasiado rápido. No debería considerarse la alternativa rápida a las benzodiacepinas. Recordemos que en mayor medida los típicos, pero también los atípicos, modulan en forma negativa a la histamina y la acetilcolina potenciando sus efectos depresores sobre la vigilia.
Asimismo, aquellos que aumentan la liberación de dopamina, como metilfenidato, modafinilo y derivados anfetamínicos, aumentan el tiempo de vigilia y pueden producir insomnio. El modafinilo ha sido aprobado para evitar la somnolencia excesiva en sujetos con narcolepsia y apnea obstructiva del sueño. Hemos comentado ya el efecto sobre la vigilia del bupropión a propósito de sus efectos sobre la noradrenalina, aunque también presenta efectos sobre la recaptación de dopamina.
Conclusiones
La delicada regulación a través de múltiples sistemas ho- meostáticos que involucran diferentes redes neurales que es- tán implicadas en el ciclo sueño vigilia nos impide, al estado actual del conocimiento, disponer de un hipnótico ideal.
Los más utilizados, hasta el momento los benzodiacepíni- cos, pero también muchos de los que hoy están siendo usa-
dos en sustitución de los anteriores para el tratamiento de los trastornos del sueño, muestran el desarrollo de tolerancia a sus efectos, lo que evidencia la puesta en marcha de los mecanismos de compensación del organismo.
Un abordaje terapéutico racional deberá ser cuidadoso e integral, ajustado al diagnóstico e individualizado para cada situación en particular.
Cuando se considere necesario e imprescindible se podrá recurrir a los fármacos hipnóticos por períodos cortos o en forma intermitente, a la espera de que las otras medidas tera- péuticas vayan produciendo sus efectos.
No nos cansaremos de insistir en que las alteraciones del sueño son una de las patologías que tenemos que tratar con mucha cautela, investigando sus causas y modificando todas aquellas circunstancias que puedan ser corregidas para per- mitir un buen dormir.
Su tratamiento deberá hacerse mediante el uso racional, tanto de las medidas terapéuticas no medicamentosas (psico- terapia, higiene del sueño, psicoeducación, técnicas de rela- jación), como psicofarmacológicas que se estimen adecuadas para cada caso en particular.
Bibliografía
• Bocchino S. et al. Trastornos del sueño parte 1.Rev. Psicofarmacología 2017; 8 (8-15) ed. Sciens.
• Brusco I. Trastornos del sueño y de los ritmos biológicos en la enfermedad de Alzheimer. Ed Salerno, 2012.
• Campagne DM, García Campayo J. El inadecuado uso de las benzodiacepinas. Semergen. 2005;31(7):319-24.
• Cardinali D. Melatonina: fisiología y aplicaciones clínicas. Rev. Arg. de Psiquiat. 2007, Vol. XVIII: 288-293.
• Chavez M, Navas M y cols. En busca del Hipnótico ideal. Tratamiento farmacológico del insomnio. Archivos Venezolanos de Farmacología y Terapéutica. Enero 2017.
• Contreras A. Insomnio. Generalidades y alternativas terapéuticas de última generación. Rev. Med. Clin. Condes 2013, 24 (3); 433-441.
• Díaz Negrillo A. Bases neuroquímicas implicadas en la regulación del sueño. Arch. Neurocien (Mex) 18 (1) Enero-Marzo 2013.
• Escames G, Acuña Castroviejo D. Melatonina, análogos sintéticos y el ritmo sueño/vigilia. Rev Neurol 2009; 48: 245-54.
• Franco-Pérez J, Ballesteros Zebadúa P y cols. Principales neurotransmisores involucrados en la regulación del ciclo sueño vigilia. Rev. Invest. Clín. 2012, 64 (2); 182-191.
• Hospital Universitario Vall D´Hebrón. Insomnio. Pautas de actuación y seguimiento del Colegio Médico de España y la Unidad de Sueño del Hospital Universitario Vall D´Hebrón. Barcelona 2016.
• Jufe G. Nuevos hipnóticos. Perspectivas desde la fisiología del sueño. Rev. Arg. de Psiquiat. 2007, Vol. XVIII: 294-299.
• Purves D. et al. Neurociencia 5° edición. Editorial Médica Panamericana 2012; 28: 625-646.
• Salin Pascual R. Nuevas estrategias farmacológicas para el manejo del insomnio: Suvorexant, antagonista de receptores orexígenos. Rev. Mex. Neuro- ciencias. Nov-Diciembre 2016. 17 (6); 97-105.
• Speranza N, Domínguez V y cols. Consumo de benzodiacepinas en la población uruguaya: un posible problema de salud. pública. Rev. Med. Urug. 2015 31 (2) 112-119.
• Valencia M, Cassiani C y cols. El sistema orexígeno / hipocretinérgico y su rol en los trastornos del sueño. Salud Uninorte. Barranquilla. 2010 26 (2); 285-297.
• Zieher L.M. et al. Psicofarmacología clínica y sus Bases Neurocientíficas. 3° edición 2003; 14:259-276.







No comments! Be the first commenter?