A menudo la obesidad se acompaña de múltiples comorbilidades entre las que se encuentran las enfermedades psiquiátricas. Se ha descrito que la depresión muestra un comportamiento recíproco en pacientes con obesidad mórbida. Por ello, es habitual que este grupo de pacientes consuma psicofármacos y otros medicamentos de manera prolongada. La cirugía bariátrica está indicada en pacientes obesos con comorbilidades asociadas o bien, obesidad mórbida (IMC>42kg/m2). Aunque el descenso de peso provocado por dicha intervención es visible (alrededor del 30%) en la mayoría de los casos, el uso de medicamentos asociados a patologías crónicas, rara vez disminuye o desaparece. Esta realidad sumada a los cambios anatómicos causados por la cirugía y las alteraciones farmacocinéticas que acompañan a estos supone un desafío en el manejo farmacoterapéutico de los pacientes. Además, se han descrito modificaciones de procesos farmacocinéticos en la obesidad que no necesariamente mejoran una vez intervenido el paciente o se modifican considerablemente. Todo lo cual podría redundar en fallo terapéutico y recaída de la signo sintomatología o bien, en toxicidad. En la presente reseña, se desarrollan los cambios en la farmacocinética antes y después de la cirugía y se proveen sugerencias de seguimiento de pacientes tratados con psicofármacos basadas en bibliografía.
Palabras clave
Obesidad – Psicofármacos – Cirugía bariátrica – Farmacocinética – Ajuste de dosis.
Scolari MJ. “Modificaciones farmacocinéticas de psicofármacos en pacientes obesos sometidos a cirugía bariátrica”. Psicofarmacología 2025;138:21-30. Puede consultar otros artículos publicados por los autores en la revista Psicofarmacología en sciens.com.ar
Introducción
La obesidad es, sin lugar a duda, un problema creciente de salud pública y hoy se la reconoce como una epidemia. La Organización Mundial de la Salud, la define como un ex- ceso del cúmulo de grasa en el organismo con afectación de la salud (1). Es considerada una entidad multisistémica, con
problemas asociados no solo al peso del paciente, sino tam- bién psicológicos, motores, económicos y sociales. En 2016, casi 2 billones de personas adultas tenían sobrepeso, de los cuales 650 millones eran obesos (1). Ya en 2020, 39 millo- nes de niños menores de 5 años poseían sobrepeso u obe- sidad (1). Desde un punto de vista biométrico, la obesidad se define como un valor del Índice de Masa Corporal (IMC)
igual o superior a 30kg/m2. EL abordaje inicial de la obesidad consta de modificaciones del estilo de vida, como cambios en la dieta y la cantidad de ejercicio realizada por el paciente. Sin embargo, suele asociarse con múltiples comorbilidades la cuales requieren el uso de medicamentos. Entre ellas se encuentran, hipertensión, diabetes tipo 2, hiperlipidemia, en- fermedad cardiovascular, enfermedades psiquiátricas, entre otras (2). Esta realidad, hace que el paciente obeso deba ser tratado de manera multidisciplinaria. De hecho, el aumento de la proporción de grasa puede representar un desafío para el ajuste de dosis de fármacos lipofílicos (benzodiacepinas, hor-
monas tiroideas, vitaminas, algunos antibióticos, etc.). Más aún, la coexistencia de comorbilidades hace que el paciente obeso sea un caso típico de polifarmacia, lo cual predispo- ne a interacciones medicamentosas. Yska y colaboradores (3) reportaron la siguiente proporción de uso de medicamentos en pacientes obesos: 26% para fármacos cardiovasculares y antidiabéticos, 25% para los que afectan las vías respirato- rias, 21% para antidepresivos, 12% para antitiroideos y 10% para antiinflamatorios no esteroides. Sin embargo, cuando el IMC supera los 40 kg/m2 o alcanza los 35 kg/m2 asociados a comorbilidades (diabetes, hipertensión, apnea del sueño o hi-
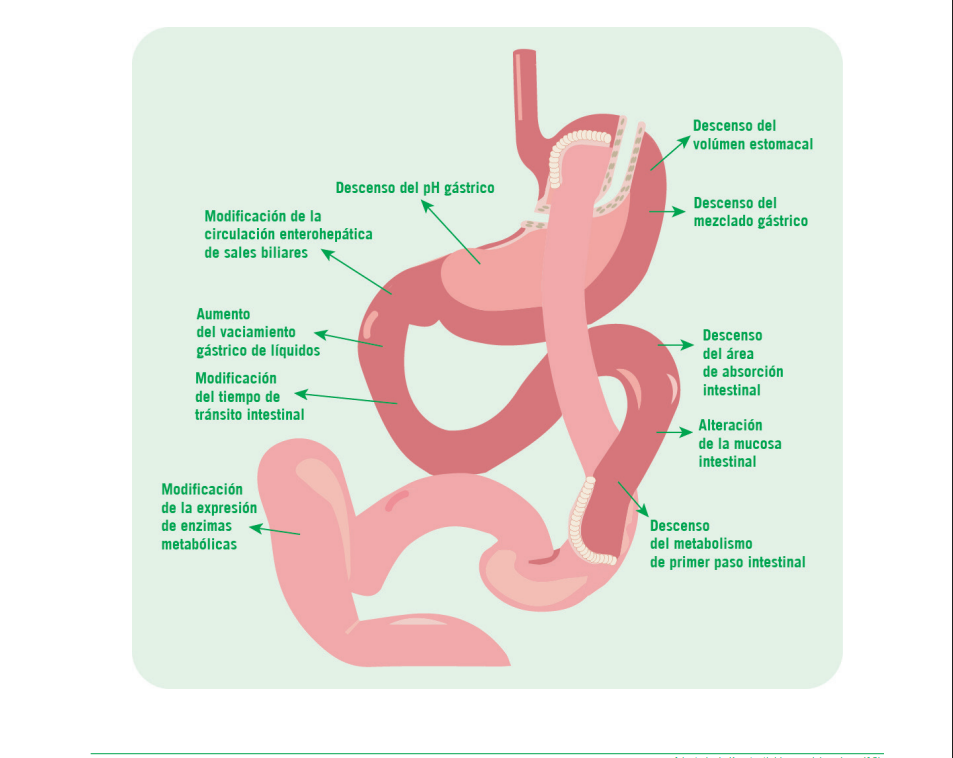
pertensión intracraneal benigna), la indicación de tratamiento es la cirugía bariátrica (CB) la cual implica la modificación del tracto digestivo del paciente (4). La CB es la madia más efectiva para la reducción del peso a largo plazo con alrededor de 32% de disminución a los 2 años postintervención. Ade- más, se asocia a menor incidencia de infarto de miocardio, accidente cerebrovascular, cáncer y diabetes, así como a la reducción de la mortalidad (5, 6, 7). Los cambios anatómicos producidos por la CB se clasifican como restrictivos, malab- sortivos o combinación de ambos (8). Los restrictivos buscan limitar la cantidad de alimentos ingeridos, en tanto que los malabsortivos reducen la superficie disponible para la absor- ción de nutrientes (8). Si bien existe una variedad de técnicas para realizar la CB, las más utilizadas son la gastrectomía en manga (GM) y el bypass gástrico Roux en Y (BGRY) (9). La GM es un procedimiento restrictivo en el cual se realiza una resección para formar una estructura “tipo manga” a lo largo de la curvatura menor del estómago. De esta manera, no solo se limita la cantidad de comida ingerida, sino también las co- larías, promoviendo sensación de saciedad (10). Por otro lado, en la BGRY se realiza una resección en el estómago, creando un pequeño saco para limitar la ingesta de alimentos. Este saco se une y anastomosa al yeyuno para disminuir la absor- ción de nutrientes (11). Por lo tanto, la BGRY es una técnica que combina cambios restrictivos con malabsortivos. Dicho esto, si bien la cirugía bariátrica produce mejoras ostensibles en el paciente, los cambios anatómicos que requiere generan alteraciones diversas en el tubo digestivo que pueden afec- tar la farmacocinética de los medicamentos ingeridos. Entre ellos podemos mencionar, cambios de pH, de la motilidad, en la absorción y distribución de los fármacos, entre otros. En la figura 1, se observan las modificaciones anatómicas y farmacocinéticas producidas por la BGRY. Tales alteraciones, suponen un desafío en los ajustes de dosis que pueden ser necesarios tras la cirugía y en la predicción de los efectos clínicos observados en los pacientes.
En la presente obra se describirá el impacto de la CB en los parámetros farmacocinéticos de psicofármacos administrados por vía oral (VO) y se realizarán sugerencias para el ajuste de sus dosis en pacientes obesos sometidos a CB.
Farmacocinética de medicamentos admi- nistrados por vía oral
La VO es la más costo efectiva de las vías disponibles para administrar medicamentos. Posee múltiples ventajas entre las que destacan el ser indolora y poder administrarse en domi- cilio sin la necesidad de personal entrenado. Sin embargo, la llegada al torrente sanguíneo o al sitio de acción de los me- dicamentos administrados por VO, depende de una serie de pasos que pueden ser afectados por diversos factores, entre ellos, la CB.
Las formas farmacéuticas sólidas (comprimidos, cápsulas) deben ser ingeridas con cantidad suficiente de líquido, para favorecer su pasaje a través del esófago y llegar al estóma- go. Una vez allí, el comprimido o la cápsula que alberga el medicamento debe desintegrarse para dar paso a la libera- ción del principio activo (PA) y su disolución. Esta serie de pasos depende de las características farmacotécnicas de la forma farmacéutica, así como de la droga. Entre las primeras se encuentra la dureza del preparado. Cuanto más duro sea un comprimido, más tiempo requerirá para desintegrarse en el estómago. Por lo que un comprimido excesivamente duro no se desintegrará apropiadamente y la motilidad gástrica hará que llegue con cierta integridad al intestino delgado con me- nos posibilidades de absorción. La presencia de cubierta en las formas farmacéuticas sólidas también afectará a la desin- tegración de un modo similar. Sin embargo, existen cubiertas específicamente diseñadas para soportar el entorno ácido del estómago, para proteger la mucosa o al medicamento. En es- tos casos, la absorción no se vería afectada por su presencia. Los movimientos del estómago favorecen la desintegración de las formas farmacéuticas y la disolución del PA. No obstante, ésta dependerá, también, de su solubilidad en medio acuoso y su capacidad de ionizarse, por lo tanto, del pH del medio. Una vez disuelto, el vaciamiento gástrico favorecerá el tránsito tanto del PA como de los excipientes al intestino delgado, donde será absorbido. El mecanismo por el cual ocurrirá la absorción dependerá del PA y de su grado de disolución. Ha- bitualmente, las moléculas solubilizadas en el medio acuoso del tubo digestivo son absorbidas por proteínas transporta- doras, en tanto que las partículas lipofílicas lo harán por di- fusión pasiva o bien por emulsificación con las sales biliares
(12). Una vez atravesada la pared intestinal, las moléculas
acceden a la circulación portal, donde pasarán por el hígado donde podrán o no ser metabolizadas en lo que se conoce como efecto del primer paso hepático, un limitante clásico de la biodisponibilidad. A este paso por el hígado le sigue la fase de distribución, proceso por el cual el PA llegará a su sitio de acción. La mayoría de los medicamentos, como el loraze- pam o la fluoxetina, viajan por el torrente sanguíneo unidos a proteínas plasmáticas, con escasa fracción libre (13). La variable característica de la fase de distribución es el volumen de distribución (Vd), el cual depende de las propiedades del medicamento. Según la lipofilicidad del fármaco, puede pasar al tejido adiposo o bien atravesar la barrera hematoencefálica y acceder al cerebro. En estos casos, el Vd suele superar el volumen plasmático, ya que el PA virtualmente “desaparece” del plasma. Inevitablemente, el medicamento llegará al hí- gado donde será o no metabolizado, pudiendo generar meta- bolitos con actividad farmacológica o bien inactivos. Si bien el metabolismo de fármacos no es exclusivo del hígado (de hecho, será muy importante recordar que ocurre, también, en el intestino para comprender más adelante que ocurre luego de la CB), allí es donde ocurrirá en mayor extensión. Existen dos grupos de enzimas que llevan a cabo el metabolismo de fármacos: los citocromos, también conocidos como CYP450
(se han identificado múltiples isoenzimas) y las enzimas de conjugación (12). Los primeros producen modificación quími- ca por mecanismos de óxido-reducción y las segundas lo ha- cen asociando moléculas hidrofílicas al PA. A su vez, ciertos fármacos (carbamezepina, diazepam, otros), pueden volver al intestino delgado a través de las sales biliares y ser reabsorbi- dos (circulación enterohepática) o bien excretados por heces. El paso farmacocinético final es la excreción. Al llegar al riñón los medicamentos o metabolitos de ellos de carácter hidrofíli- co serán excretados por orina, o en ciertos casos reabsorbidos en los túbulos renales. A través delos fenómenos de meta- bolismo y excreción, la concentración del PAse reduce pro- gresivamente con una cinética determinada, en gran medida, por la naturaleza del mismo. A medida que la concentración plasmática del PA disminuye el equilibrio químico hace que salga de los “compartimentos profundos” (segunda fase de distribución) para que pueda ser metabolizado y excretado. Es importante aclarar que los pasos farmacocinéticos ocurren de manera simultánea una vez que el PA alcanzó la circulación sistémica.
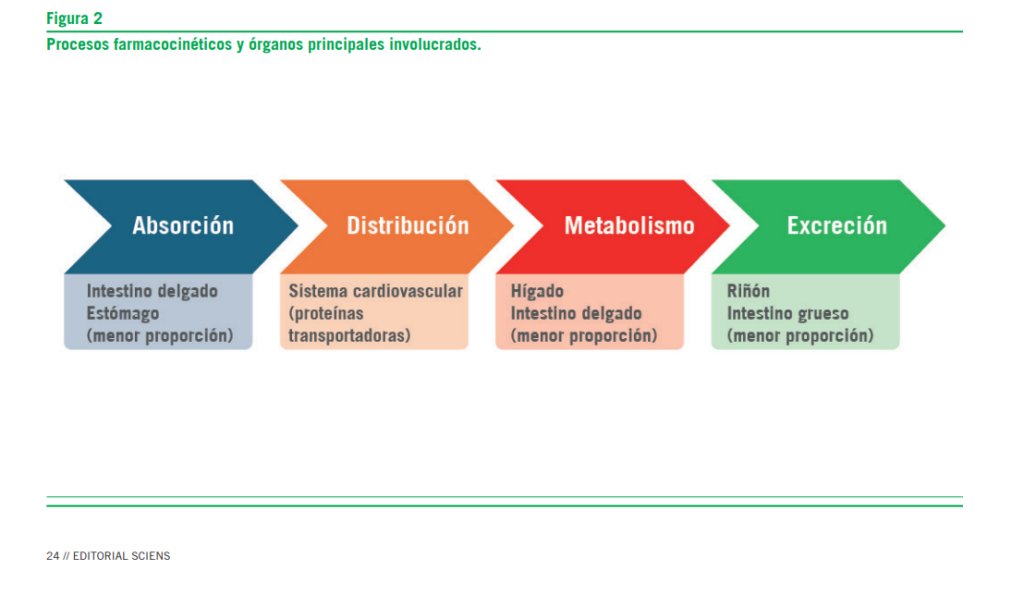
En la figura 2 se muestran losprocesos farmacocinéticos de manera secuencial.
Efectos de la obesidad en los procesos far- macocinéticos
El incremento de tejido adiposo y la inflamación crónica de bajo grado asociada a la obesidad pueden producir cambios clínicamente significativos en la farmacocinética de los me-
dicamentos. En primer lugar, es esperable que el Vd de dro- gas de alta lipofilicidad (por ejemplo, diazepam o metadona), aumente ya que tienen tendencia a acumularse en el tejido graso (14). En estos casos una revisión de las dosis indicadas puede ser necesaria para evitar fallos terapéuticos o recaída de síntomas.En el caso de drogas hidrofílicas, el Vd se man- tiene prácticamente inalterado. Sin embargo, puede esperarse un aumento de la concentración plasmática por disminución del espacio tisular para penetración de la droga (14). Por otro lado, la inflamación crónica en la obesidad produce secreción anormal de citoquinas, quimioquinas y adipoquinas, que alte- rarían la cantidad y actividad de los citocromos (12). Además, los cambios fisiopatológicos de la obesidad producen hígado graso de origen no alcohólico y esteatohepatitisno alcohóli- ca, que pueden alterar, también, la función metabólica (12). Estas observaciones, dejan en claro que los pasos de distri- bución y metabolismo podrían estar afectados en pacientes obsesos y ponen de manifiesto la necesidad de controlar de cerca a los mismos, particularmente a aquellos con obesidad mórbida, para detectar tempranamente cambios clínicos de- venidos de alteraciones en las concentraciones plasmáticas de los medicamentos que consumen. En cuanto al paso de absorción de fármacos administrados por VO, no debería espe- rarse cambios clínicamente significativos en pacientes obesos en comparación con pacientes de IMC normal (13). Final- mente, se ha descrito hiperfiltración renal en pacientes con obesidad, la cual revertiría luego de una dieta hipocalórica, que podría afectar el nivel de excreción particularmente de moléculas hidrofílicas (15), sin embargo, el impacto clínico de esta alteración no ha sido estudiado en profundidad.
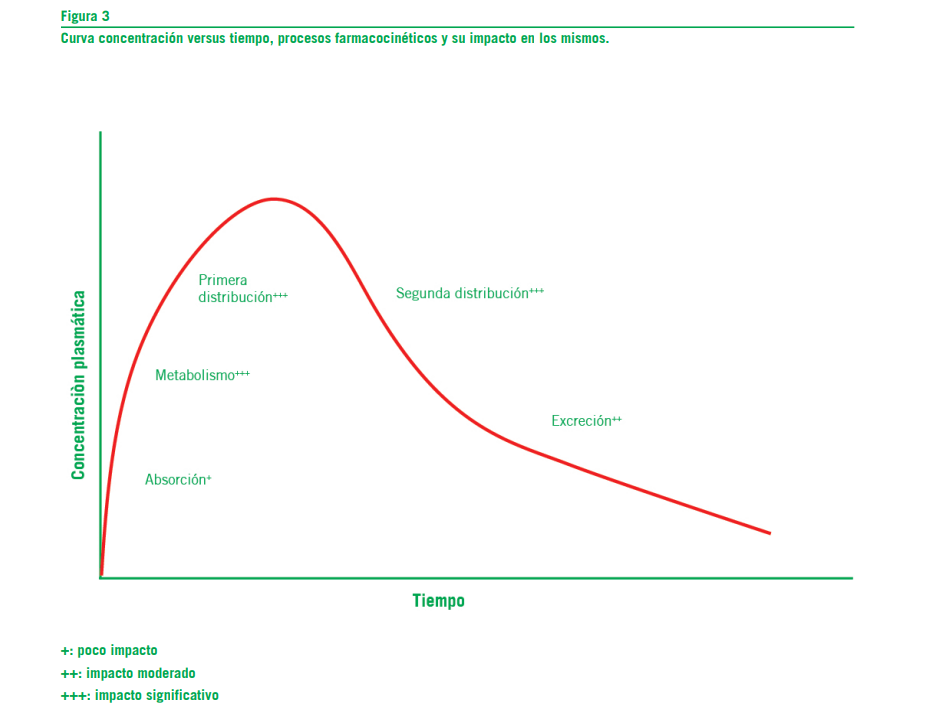
En la figura 3 se observa una curva de concentración plas- mática en función del tiempo de un PA administrado por VO y la influencia de la obesidad en los procesos farmacocinéticos.
Efectos de la cirugía bariátrica en los pro- cesos farmacocinéticos
Los cambios farmacocinéticos luego de la CB y la pérdida de peso dependerán, en gran medida del tipo de cirugía rea- lizada, el grado de reducción en el IMC y las propiedades del medicamento. Existe evidencia que indica que la absorción de fármacos podría disminuir luego de la cirugía. Este cambio podría explicarse por la restricción gástrica causada por la disminución de la superficie estomacal, con la consecuente
reducción de la secreción ácida y el aumento del pH. Esto afectaría la desintegración de los comprimidos o cápsulas con medicamentos y la disolución de PA solubles en medio ácido (16, 17). Además, se ha observado que la motilidad gástrica estaría disminuida, con el consecuente impacto en la desintegración de las formas farmacéuticas (18). Por este motivo, las formulaciones líquidas son preferidas en este tipo de pacientes. Sin embargo, esta estrategia presenta al menos 2 desventajas: Primero, gran cantidad de medicamentos con- sumidos por pacientes adultos no están disponibles en esta forma, lo cual requeriría de una formulación magistral. Segundo, con frecuencia, las formulaciones líquidas (como jarabes y suspensiones) contienen azúcares para mejorar sus características organolépticas que, en grandes cantidades, pueden generar un entorno hiperosmolar en el intestino causando
molestares como distensión, náuseas y diarrea en lo que se conoce como dumping syndrome (síndrome del vaciamiento gástrico rápido). Este es una complicación de la CB por au- sencia de píloro o disminución de su tono (19). Así mismo, los procedimientos que reseccionan o hacen bypass (BGRY) de porciones del duodeno o yeyuno proximal reducen signifi- cativamente la superficie de absorción intestinal con impacto en la biodisponibilidad. Esto ocurre ya que al disminuir la su- perficie de absorción también lo hace el número de moléculas trasportadoras de PA alojadas en la luz intestinal. Queda claro que los procedimientos malabsortivos (como BGRY y otros) modifican la longitud del tubo digestivos y esto tendría un impacto notable en la biodisponibilidad de PA administrados como formas farmacéuticas de liberaciónsostenida, extendi- da o programada. Estas formulaciones están diseñadas para viajar distancias definidas para lograr su máxima disolución y absorción, por lo que un tubo digestivo acortado podría dis- minuir la biodisponibilidad (20). Tras la CB y la consecuente disminución del IMC, el tamaño del hígado y la cantidad de grasa en su interior disminuyen. Estos fenómenos, sumados al descenso de la inflamación crónica de bajo grado, favore- cen la actividad de los citocromos hepáticos e intestinales. Sin embargo, se debe recordar que los procedimientos que reseccionan el intestino (como la BGRY) disminuyen de ma- nera permanente los citocromos del intestino delgado. Por lo tanto, los efectos en el metabolismo dependerán, también, del procedimiento empleado. Casi el 50% de los fármacos son metabolizados por el CYP3A4, el cual se haya en el hígado y el intestino delgado (12). En el caso de este citocromo, el aumento de actividad hepática evidenciada cuando la cirugía
comienza a dar frutos debería compensar la pérdida de este cuando la anatomía del intestino se altera como consecuencia de esta. En cambio, en el caso del CYP2C19, su presencia en mucho mayor en el hígado que en el intestino. Por lo tan- to, la recuperación de la función hepática podría demandar ajustes en los fármacos que son sustrato de dicho citocromo (citalopram, diazepam) (21). Finalmente, dado que en ciertos casos la obesidad puede dañar el riñón y disminuir su tasa de filtrado, al mejorar el IMC del paciente tras la cirugía, parte de la función renal perdida se recuperaría aumentando la tasa de excreción de fármacos hidrofílicos (22). Sin embargo, la implicancia clínica de estos cambios aún no ha sido estudiada en profundidad.
La tabla 1 compara la afectación de los procesos farmaco- cinéticos por la obesidad y la CB.
Psicofármacos y cirugía bariátrica
La comorbilidad psiquiátrica es frecuente en pacientes ob- sesos (fundamentalmente mujeres) candidatos a realizarse una CB (23, 24). Por ejemplo, se ha descrito que la obesidad y la depresión muestran reciprocidad. Si bien algunos pacien- tes mejoran sus síntomas depresivos luego de la intervención, existen estudios que han reportado aumento de los suicidios incluso post cirugía (25). Además, ha sido señalado que la prevalencia de depresión disminuye durante los primeros 6 meses luego de la CB, momento donde la pérdida de peso es más evidente, y aumenta cuando dicho descenso aminora o
Tabla 1
Influencia de la obesidad y la cirugía bariátrica sobre los procesos farmacocinéticos.
| Desintegración* | Absorción | Distribución | Metabolismo | Excreción | |
| Obesidad | – | + | +++ | +++ | ++ |
| Cirugía | ++ | +++ | ++ | +++ | + |
*Aplica solamente para formas farmacéuticas sólidas
-: ningún efecto
+: efecto leve
++: efecto moderado
+++: efecto significativo
existe ganancia de peso de rebote (26). De hecho, la mayoría de los pacientes en tratamiento con psicofármacos, los mantienen luego de la cirugía (27). Esto plantea un doble desafío ya que gran parte de los psicofármacos empleados para tratar la depresión, la ansiedad y otros síntomas son afectados por las modificaciones farmacocinéticas antes mencionadas y porque el impacto clínico de las mismas no es rápidamente evidenciable mediante estudios como puede ocurrir con otro tipo de medicamentos (antihipertensivos, hipolipemiantes, etc.). De manera tal que el paciente que ha atravesado una CB que se encuentra bajo tratamiento psicofarmacológico, debe ser estrictamente monitoreado para detectar cualquier necesidad de ajuste de dosis de manera precoz.
En esta sección se resumirá la evidencia disponible acer- ca de los efectos de la CB sobre los niveles plasmáticos de psicofármacos y las recomendaciones sugeridas para cada uno de ellos.
Estudios recientes
Wallerstedt y colaboradores (15), exploraron los efectos an- tes y hasta un año después de la CB sobre las concentraciones séricas de antidepresivos, antipsicóticos y antiepilépticos.In- cluyeron 85 pacientes en el estudio (86% mujeres, con edad media de 45 años e IMC medio de 42 kg/m2). Observaron una reducción significativa de las concentraciones plasmáticas post procedimiento de sertralina (51%), mirtazapina (41%), duloxetina (35%) y citalopram (19%). En tanto que las de venlafaxina, pregabalina y fluoxetina, no variaron. Los autores incluyeron otras sustancias en el estudio, aunque no pudieron extraer conclusiones debido a la falta de representatividad del número de pacientes que las consumían. Entre ellas podemos mencionar: olanzapina, quetiapina, gabapentina, lamotrigina, ácido valproico, topiramato, amitriptilina, clomipramina entre
Tabla 2
Cambios en la psicofarmacoterapia de pacientes que mostraron desmejora anímica luego de la cirugía bariátrica.
| Procedi- miento | Psicofármaco | Dosis previa (mg) | Nivel previo (nmol/L) | Día postcirugía | Dosis postcirugía (mg) | Nivel postcirugía (nmol/L) |
| BGRY | Citalopram | 10 | 137 | +252 +374 | 10 20 | 69 158 |
| BGRY | Citalopram | 10 | 89 | +178 +386 | 10 20 | 42 90 |
| BGRY | Mirtazapina Sertralina | 15 200 | 96 130 | +68 +368 +68 +368 | 15 30 200 200 | 30 203 66 78 |
| GM | Mirtazapina | 30 | 140 | +213 +393 | 30 45 | 87 119 |
BGRY: By Pass Gástrico Roux en Y GM: Gastrectomía en Manga
Adaptado de Wallerstedt y colaboradores (15).
otros. Notablemente, el estudio reportó el caso de 4 pacientes que advirtieron empeoramiento de sus síntomas psiquiátricos con requerimiento de ajustes en las dosis de sus medicamentos. Tres de ellos habían realizado bypass gástrico y el restante GM. En la tabla 2 se muestran los cambios reportados en la farma- coterapia de estos pacientes.
Garin y colaboradores (28) evaluaron el impacto de la BGRY en las concentraciones plasmáticas de antidepresivos antes y después de la misma. Incluyeron 13 pacientes (12 mujeres, edad media de 44 años e IMC medio de 41,3 Kg/m2). Ob- servaron un descenso significativo de los niveles plasmáticos de escitalopram (43%), duloxetina (33%), trazodona (16%) y de fluoxetina (9%). Notablemente, para el caso del escitalo- pram, una dosis del doble de la indicada antes de la cirugía no fue suficiente para lograr los niveles plasmáticos previos. Los autores señalaron a este medicamento como el de mayor necesidad de monitoreo terapéutico (MT).
Un hecho notable es que ha sido reportado una recupe- ración de los niveles plasmáticos o áreas bajo la curva ha- bituales de antidepresivos luego de 6 meses o más una vez realizada la CB (29). Sin embargo, aún existe inconsistencia en la bibliografía en este punto y se debe seguir estudiando. En términos generales, se entiende que el tmax (tiempo que se tarda en alcanzar la concentración plasmática máxima) se acortaría y la concentración máxima aumentaría cuando se administran fármacos por VO luego de la intervención. No obstante, el efecto sobre el área bajo la curva es menos claro pudiendo aumentar, disminuir o no alterarse (26, 30, 31).
Finalmente, un estudio in vitro reportó un aumento en la disolución estomacal, luego de la BGRY, de sales de litio y bupropion, advirtiendo sobre el riesgo de aumento de la toxi- cidad del primero (32).
Pautas de seguimiento de pacientes candi- datos a cirugía bariátrica bajo tratamiento con psicofármacos
Por lo descripto hasta aquí, queda claro que realizar suge- rencias o recomendaciones sobre el manejo del tratamiento farmacoterapéutico del paciente obeso no es tarea sencilla. En el campo de los psicofármacos la tarea es aún más com- pleja por diferentes razones. En primer lugar, la mayoría de los medicamentos de uso común en psiquiatría, no son moni- toreados en sangre de manera habitual. El litio es, claramente una excepción por tratarse de un fármaco de estrecho margen terapéutico. En segundo lugar, el impacto clínico de las al- teraciones farmacocinéticas no siempre es fácil de detectar. Un caso particular es el de los antidepresivos. El deterioro anímico devenido de una dosificación insuficiente, no se evi- dencia si no hasta después de un período en donde la red neuronal se deteriora significativamente. A su vez, la mejoría
luego del ajuste de dosis puede mostrar latencia en aparecer. El contexto del paciente sometido a la intervención bariátri- ca donde existen dolor, cambios metabólicos y emocionales, puede complejizar la evaluación integral del estado de ánimo. En tercer lugar, la gran mayoría de los psicofármacos se pre- sentan en formulaciones orales sólidas y, en algunos casos, de liberación programada.
Respecto de las formas farmacéuticas, la bibliografía indica que las formulaciones líquidas serían preferibles a los com- primidos y a las cápsulas. Debe considerarse el contenido de azúcares para prevenir la ocurrencia del efecto dumping. Las formulaciones de liberación programada, de ser posible, debe- rían evitarse dado que sus características farmacotécnicas las hacen especialmente sensibles a los cambios causados por la cirugía. Si fuera necesaria su indicación se debe aumen- tar la rigurosidad del monitoreo. En el entorno hospitalario, la posibilidad de abordar al paciente por vías parenterales, especialmente endovenosa, puede facilitar la tarea inicial con la problemática de que gran parte de los psicofármacos, par- ticularmente los antidepresivos, no poseen una formulación adecuada.
Las recomendaciones enfocadas en fármacos específicos están basadas en estudios con pocos pacientes, por lo cual deben tomarse con precaución. Lau y colaboradores (33) rea- lizaron una revisión de 56 artículos que involucraron pacien- tes sometidos a CB y evaluaron el impacto sobre parámetros farmacocinéticos de diferentes fármacos.
Sales de Litio
Si bien el litio (en argentina disponemos de el como carbo- nato), es un reconocido fármaco de estrecho margen terapéu- tico, su determinación en plasma es una práctica habitual. En principio se debe considerar una reducción de dosis de entre 30-70% y titular la dosis óptima mediante MT con una fre- cuencia semanal. Si bien, los autores sugieren considerar las formas de liberación programada, lo recomendable sea ma- nejar las formulaciones a las que el paciente esté habituado. Si fuera a realizarse un cambio de forma farmacéutica, se sugiere incrementar el MT hasta lograr estado estacionario y luego separar las determinaciones.
Se debe tener en cuenta que la mayoría de los estudios que han evaluado sales de litio hacen foco en su toxicidad luego de la cirugía. Por lo tanto, se deben observar signos de esta particularmente a nivel neurológico, considerando que su aparición no es temprana. Los síntomas incluyen: letargo, ataxia, agitación y excitación neuromuscular. Esta última, se manifiesta como temblores, fasciculaciones y/o calambres. Se debe considerar que a dosis terapéuticas de litio puede obser- varse un temblor, conocido como “temblor terapéutico”. El mismo es de características simétricas, se limita mayormente a los brazos y no es de carácter progresivo. Los signos de to- xicidad severa por sales de litio incluyen convulsiones, status
epiléptico no convulsivo y encefalopatía (34).
Antidepresivos
Los antidepresivos están entre los medicamentos mayor- mente evaluados en el contexto de la CB. Esto debe a la pre- valencia de la depresión en este grupo de pacientes y a que los tratamientos suelen ser de al menos 6 meses. La dificultad reside en que los síntomas debido a concentraciones insufi- cientes se instauran de manera paulatina. Los antidepresivos con mayor descenso reportado son citalopram, escitalopram, sertralina y duloxetina (28). La recomendación general es rea- lizar MT (de ser posible), considerar los períodos de latencia, no realizar cambios de medicamento y/o forma farmacéutica. Se debe recordar, que se ha reportado una recuperación de los niveles plasmáticos o áreas bajo la curva habituales de antidepresivos luego de 6 meses o más una vez realizada la cirugía bariátrica (29), por lo que el seguimiento del paciente debe ser estricto durante el primer año. En el trabajo de Wa- llesterdt (15) los pacientes reportaron desmejora en su estado de ánimo con: citalopram, sertralina y mirtazapina.
Ansiolíticos
Aunque la evidencia sigue siendo escasa, el medicamento mejor estudiado de este grupo es el midazolam. Brill y colabo- radores (35), realizaron dos estudios sobre los efectos del mi- dazolam, después de la CB. El primer estudio mostró que des- pués de BGRY y GM, el metabolismo hepático aumentó 1,7 veces, por recuperación de la actividad hepática de CYP3A4, pero su biodisponibilidad oral no cambió. En el segundo, mos- tró que a los 3 y 12 meses post cirugía se incrementó la tasa de absorción oral, con reducción del tmax (36). Aparentemen- te la biodisponibilidad permaneció inalterada. Es posible que se evidencie un inicio de efecto precoz, por lo que se sugiere titular la dosis, empleando la menor posible.
Otros psicofármacos
Fuera de los psicofármacos ya mencionados, los medica- mentos de los que se cuenta mejor evidencia son los antiepi- lépticos. Lau y colaboradores (33) hacen recomendaciones similares para la pregabalina, lamotrigina, carbamazepina y ácido valpróico. En todos los casos diferencian aquellos pa- cientes que son epilépticos de aquellos que usan estas drogas para el manejo del dolor neuropático. Esto se debería a que habitualmente las dosis empleadas en uno u otro escenario son diferentes (en epilepsia suelen ser mayores). Para el gru- po de pacientes epilépticos se sugiere realizar MT lo antes posible luego de la cirugía, manteniendo las formas farma-
céuticas. En el caso de otro tipo de pacientes, se sugiere el monitoreo clínico del paciente con base en la eficacia y los efectos adversos observados.
Discusión
La obesidad sigue siendo un problema de salud pública cre- ciente. Las comorbilidades asociadas a ella hacen que en gran cantidad de pacientes obesos sean necesarios medicamentos de uso prolongado. Hecho que se enfatiza por el incremento de la expectativa de vida. Dentro de las patologías observa- das en pacientes obesos, destacan las psiquiátricas como la depresión y la ansiedad (23, 24). Se ha observado, especial- mente en mujeres, una asociación entre obesidad y depresión, la cual en ciertos casos puede mejorar luego de la cirugía bariátrica o bien, empeorar cuando el descenso de peso se hace menos evidente. Los procedimientos quirúrgicos mejor estudiados son la GM y BGRY. El primero restringe la ingesta calórica en tanto que el segundo añade disminución en la su- perficie disponible para absorber nutrientes (9, 10). Más allá de eso, ambos generan cambios anatómicos persistentes que tienen la capacidad de alterar los procesos farmacocinéticos, fundamentalmente la absorción y el metabolismo. El desafío que esto plantea en el manejo del paciente con obesidad es mayor de lo que parece a primera vista. Por un lado, la calidad de la evidencia disponible en el manejo de la farmacoterapia general de este tipo de pacientes es, más bien, pobre. La mayoría de los estudios incluyen pocos pacientes y medica- mentos evaluados. Además, los resultados obtenidos no siem- pre son del todo concluyentes. Sin embargo, las revisiones realizadas en relación con los psicofármacos en este contex- to, permite hacer recomendación basadas mayormente en el MT y el estricto seguimiento del paciente. Los medicamentos con mayor cantidad de estudios son los antidepresivos inhi- bidores de la recaptación de monoaminas. Algunos estudios reportan cambios significativos en los niveles plasmáticos de: escitalopram, citalopram, duloxetina, sertralina y otros (15, 28, 29). Notablemente, se ha observado recuperación de los niveles plasmáticos luego del año postcirugía. Esto resalta la complejidad del caso y la necesidad de seguir de cerca al paciente por un tiempo prolongado. Si bien, en esta reseña se han revisado gran cantidad de estudios, a la fecha no existen guías claras ni mucho menos definitivas para el manejo psi- cofarmacológicos de los pacientes sometidos a CB, por lo que se necesitan estudios de calidad con la mayor cantidad de pacientes y moléculas estudiadas posible.
Referencias bibliográficas
- 1. World Health Organization. Obesity and overweight: World Health Organization. 2021. Available from: https://www.who. int/news-room/ fact-sheets/detail/obesity-and-overweight.Con-
sultadomarzo 2025.
- 2. Koliaki C, Liatis S, Kokkinos A. Obesity and cardiovascular disease: revisiting an old relationship. Metabolism. 2019;92:98– 107.ht- tps://doi.org/10.1016/j.metabol.2018.10.011.
- 3. Yska JP, Van Der Meer DH, Dreijer AR, et
al. Influence of bariatric surgery on the use of medication. Eur J Clin Pharmacol. 2016;72(2): 203-209. https://doi.org/10.1007/s00228-
015-1971-3
- 4. le Roux CW, Heneghan HM. Baria- tric surgery for obesity. Med Clin North
Am. 2018;102(1):165–82. https://doi.or- g/10.1016/j. mcna.2017.08.011
- 5. Sjöström L. Review of the key results from the Swedish Obese Subjects (SOS) trial—a pros- pective controlled intervention study of bariatric surgery. J Intern Med. 2013;273(3):219-234. https://doi.org/ 10.1111/joim.12012
- 6. Zenténius E, Andersson-Assarsson JC, Car- lsson LMS, Svensson PA, Larsson I. Self-repor- ted weight-loss methods and weight change: ten-year analysis in the Swedish Obese Subjects Study control group. Obesity. 2018;26(7):1137- 1143. https://doi.org/10.1002/oby.22200
- 7. Reges O, Greenland P, Dicker D. Asso- ciation of bariatric surgery using laparoscopic banding, Roux-en-Y gastric bypass, or laparos- copic sleeve gastrectomy vs usual care obesity management with all-cause mortality. JAMA. 2018;319(3):279-290. https://doi.org/10.
1001/jama.2017.20513
- 8. Geraldo M, Feder D, Affonso Fonseca FL, de Fatima Veiga Gouveia MR .The use of drugs in patients who have undergone bariatric surgery. Int J Gen Med. 2014;7:219-224
- 9. Angrisani L, Santonicola A, Iovino P, Vitiello A, Higa K, Himpens J, et al. IFSO worldwide survey 2016: primary, endo- luminal, and revisional procedures. Obes Surg. 2018;28(12):3783– 94. https://doi. org/10.1007/s11695-018-3450-2.
- 10. Rosenthal RJ. International sleeve gas- trectomy expert panel consensus statement: best practice guidelines based on experien- ce of >12,000 cases. Surg ObesRelat Dis. 2012;8(1):8-19.
- 11. Higa KD. Laparoscopic Roux-en-Y gas- tric bypass for morbid obesity. Arch Surg. 2000;135(9):1029-1033.
- 12. Angeles PC, Robertsen I, Seeberg LT, Krogstad V, Skattebu J, Sandbu R, et al. The influence of bariatric surgery on oral drug bioa- vailability in patients with obesity: a systematic review. Obes Rev. 2019;20(9):1299–311.ht- tps://doi.org/10.1111/obr. 12869
- 13. Konstantinidou SK, Argyrakopoulou G, Da- lamaga M, Kokkinos A. The Effects of Bariatric Surgery on Pharmacokinetics of Drugs: a Re- view of Current Evidence. Curr Nutr Rep. 2023 Dec;12(4):695-708. doi: 10.1007/s13668- 023-00498-5. Epub 2023 Oct 20. PMID:
37857987; PMCID: PMC10766679.
- 14. De Baerdemaeker LEC, Mortier EP, Struys MMRF. Pharmacokinetics in obese pa- tients. Contin Educ Anaesth Crit Care Pain. 2004;4(5):152–5. https://doi.org/10.1093/bja- ceaccp/mkh042.
- 15. Wallerstedt SM, Nylén K, Axelsson MAB. Serum concentrations of antidepressants, an- tipsychotics, and antiepileptics over the baria- tric surgery procedure. Eur J Clin Pharmacol. 2021 Dec;77(12):1875-1885. doi: 10.1007/ s00228-021-03182-1.
- 16. Padwal R, Brocks D, Sharma A. A systema- tic review of drug absorption following bariatric
surgery and its theoretical implications. Obesity. 2010;11(1):41-5
- 17. Azran C, Wolk O, Zur M, et al. Oral drug therapy following bariatric surgery: an overview of fundamentals, literature and clinical recom- mendations. Obes Rev. 2016;17(11):1050- 1066.
- 18. Van Prooyen AM, Hicks JL, Lin E, et al. Evaluation of an inpatient pharmacy consult on discharge medications in bariatric surgery pa- tients. J Pharm Pract. 2021.
- 19. Goday Arno A, Farré M, Rodríguez-Mora- tó J, et al. Pharmacokinetics in morbid obesity: influence of two bariatric surgery techniques on paracetamol and caffeine metabolism. Obes Surg. 2017;27(12): 3194-3201.
- 20. Miller AD. Medication and nutrient admi- nistration considerations after bariatric surgery. Am J Heal Pharm. 2006;63(19):1852-1857.
- 21. Mitrov-Winkelmolen L, van Buul-Gast MC, Swank DJ, Overdiek HW, van Schaik RH, Touw DJ. The effect of Roux-en-Y gastric bypass surgery in morbidly obese patients on pharmacokinetics of (acetyl) salicylic acid and omeprazole: the ERY-PAO study. Obes Surg. 2016;26(9):2051–8. https://doi.org/10.1007/ s11695-016-2065-8.
- 22. Porat D, Dahan A. Medication manage- ment after bariatric surgery: providing optimal patient care. J Clin Med. 2020;17:9(5):1511. https://doi.org/10.3390/jcm9051511
- 23. Rajan TM, Menon V. Psychiatric disorders and obesity: a review of association studies. J Postgrad Med. 2017;63(3):182–90. https://doi. org/10.4103/jpgm.JPGM_712_16.
- 24. Sarwer DB, Cohn NI, Gibbons LM, Magee L, Crerand CE, Raper SE, Rosato EF, Williams NN, Wadden TA (2004) Psychiatric diagnoses and psychiatric treatment among bariatric sur- gery candidates. Obes Surg 14(9):1148–1156. https://doi.org/10.1381/ 0960892042386922
- 25. Tindle HA, Omalu B, Courcoulas A. Risk of suicide after long-term follow-up from bariatric surgery. Am J Med. 2010;123(11):1036–42
- 26. Courcoulas AP, King WC, Belle SH. Se- ven-year weight trajectories and health out- comes in the Longitudinal Assessment of Bariatric Surgery (LABS) Study. JAMA Surg. 2018;153(5):427–34.
- 27. Hawkins M, Leung SE, Lee A, Wnuk S, Cassin S, Hawa R, Sockalingam S. Psychia- tric medication use and weight outcomes one year after bariatric surgery. Psychosomatics 2020;61 (1): 56–63. https://doi.org/ 10.1016/j. psym.2019.10.009
- 28. Garin P, Favre L, Vionnet N, Frantz J, Eap CB, Vandenberghe F. The Influence of a Roux-en-Y Gastric Bypass on Plasma Concen- trations of Antidepressants. Obes Surg. 2023 May;33(5):1422-1430. doi: 10.1007/s11695- 023-06526-1.
- 29. Roerig JL, Steffen KJ, Zimmerman C, Mitchell JE, Crosby RD, Cao L. A comparison of duloxetine plasma levels in postbariatric
surgery patients versus matched nonsurgi- cal control subjects. J Clin Psychopharmacol. 2013;33(4):479–84. https://doi.org/10. 1097/ JCP.0b013e3182905ffb
- 30. Directives pour le traitement chirurgical de l’obésité: Swiss Society for the Study of Morbid Obesity and Metabolic Disorders; 2021 [upda- ted 01.07.2021. Disponible en: https://www. smob. ch/fr/directives/medicales. Consultado marzo 2025.
- 31. Azran C, Wolk O, Zur M. Oral drug therapy following bariatric surgery: an overview of fun- damentals, literature and clinical recommenda- tions. Obes Rev. 2016;17(11):1050–66
- 32. Seaman JS, Bowers SP, Dixon P, Schind- ler L. Dissolution of common psychiatric medi- cations in a Roux-En-Y gastric bypass model. Psychosomatics. 2005;46(3):250–3. https:// doi.org/10. 1176/appi.psy.46.3.250.
- 33. Lau C, van Kesteren C, Smeenk R, Hui- tema A, Knibbe CAJ. Impact of Bariatric Sur- gery in the Short and Long Term: A Need for Time-Dependent Dosing of Drugs. Obes Surg. 2023 Oct;33(10):3266-3302. doi: 10.1007/ s11695-023-06770-5.
- 34. Oakley PW, Whyte IM, Carter GL. Lithium toxicity: an iatrogenic problem in suscepti- ble individuals. Aust N Z J Psychiatry. 2001 Dec;35(6):833-40. doi: 10.1046/j.1440- 1614.2001.00963.x.
- 35. Brill MJ, van Rongen A, van Dongen EP, van Ramshorst B, Hazebroek EJ, Darwich AS, Rostami-Hodjegan A, Knibbe CA. The Pharma- cokinetics of the CYP3A Substrate Midazolam in Morbidly Obese Patients Before and One Year After Bariatric Surgery. Pharm Res. 2015 Dec;32(12):3927-36. doi: 10.1007/s11095- 015-1752-9.
- 36. Brill MJ, van Rongen A, van Dongen EP, van Ramshorst B, Hazebroek EJ, Darwich AS, et al.. The Pharmacokinetics of the CYP3A Subs- trate Midazolam in Morbidly Obese Patients Be- fore and One Year After Bariatric Surgery. Pharm Res. 2015 Dec;32(12):3927-36. doi: 10.1007/ s11095-015-1752-9.







No comments! Be the first commenter?