El nervio vago en el eje microbiota–intestino–cerebro: implicancias neuropsiquiátricas
Resumen
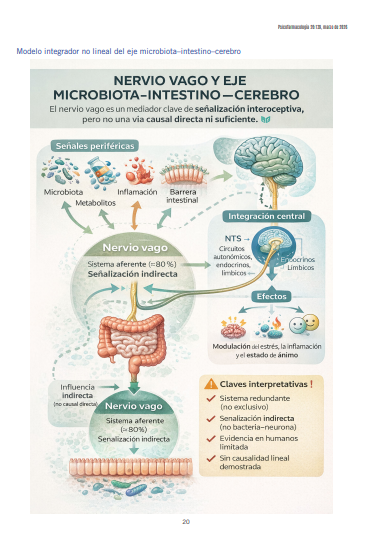
El eje microbiota–intestino–cerebro se ha consolidado como un marco integrador para comprender la interacción entre procesos gastrointestinales, inmunológicos y neuropsiquiátricos. Dentro de este eje, el nervio vago ocupa un lugar central como una de las principales vías neurales aferentes de comunicación entre el intestino y el sistema nervioso central. Este artículo revisa crítica- mente el rol del nervio vago como mediador de señalización interoceptiva, analizando su anatomía funcional, los tipos de señales que transmite y su integración en circuitos centrales implicados en la regulación del estrés y del estado de ánimo. Se discuten los mecanismos propuestos mediante los cuales la microbiota intestinal podría modular la actividad vagal de forma indirecta, así como la evidencia experimental y clínica disponible, con especial énfasis en sus límites y en los riesgos de extrapolaciones simplificadoras. Finalmente, se exploran las implicancias neuropsiquiátricas de la estimulación del nervio vago y su valor como modelo indirecto para comprender la relevancia clínica de esta vía en los trastornos afectivos.
Objetivo
Analizar de manera crítica y actualizada el rol del nervio vago dentro del eje microbiota–intestino–cerebro, diferenciando la evidencia robusta de las hipótesis plausibles y de los modelos aún especulativos, y discutir sus implicancias en un entorno colaborativo para la práctica clínica en psiquiatría.
Palabras clave
Nervio vago; eje microbiota–intestino–cerebro; señalización interoceptiva; inflamación; depresión; estrés; psicofarmacología.
Psicofarmacología 26:139, marzo de 2026
INTRODUCCIÓN
En las últimas dos décadas, el eje microbiota–intestino–ce- rebro se ha consolidado como un marco integrador para comprender la interacción entre el sistema nervioso central, el tracto gastrointestinal, el sistema inmune y la microbiota intestinal. Este modelo ha permitido reinterpretar fenómenos clínicos previamente considerados periféricos —como la infla- mación de bajo grado, las alteraciones de la barrera intestinal o los trastornos funcionales digestivos— dentro de redes neu- robiológicas complejas con relevancia psiquiátrica.
Dentro de este eje, el nervio vago ha emergido como una de las principales vías de comunicación bidireccional entre el in- testino y el cerebro. Su papel como canal aferente de informa- ción interoceptiva lo posiciona como un mediador clave entre señales viscerales periféricas y en interacción con circuitos centrales implicados en la regulación emocional. A diferencia de las vías humorales, cuya señalización es más lenta y difusa, la vía vagal permite una transmisión rápida y organizada de in- formación relevante para la regulación del estrés, la respuesta inflamatoria y el estado de ánimo.
El creciente interés por el nervio vago en psiquiatría se ha visto impulsado tanto por estudios experimentales en modelos ani- males como por la evidencia clínica derivada del uso de la esti- mulación del nervio vago en depresión resistente. Sin embargo, este entusiasmo ha favorecido, en algunos contextos, interpre- taciones simplificadoras, en las que el nervio vago es presenta- do como una vía causal directa capaz de explicar por sí sola la influencia de la microbiota sobre los síntomas afectivos.
Desde una perspectiva clínica y psicofarmacológica, resulta imprescindible diferenciar qué aspectos del rol del nervio vago cuentan con evidencia sólida, cuáles se apoyan en modelos fisiopatológicos plausibles y cuáles permanecen aún en el te- rreno de la especulación. En particular, es necesario evitar ex- trapolaciones directas entre hallazgos preclínicos y la práctica clínica en humanos, así como confusiones entre mecanismos demostrados y asociaciones indirectas.
En este contexto, el presente artículo propone una revisión crítica del nervio vago como vía de señalización neuropsiquiá- trica dentro del eje microbiota–intestino–cerebro. Se analizan su anatomía funcional básica, los mecanismos aferentes y efe- rentes implicados, la interacción con procesos inflamatorios y de estrés, y la evidencia experimental y clínica disponible, con el objetivo de aportar un marco conceptual riguroso y clínica- mente útil para el lector especializado.
1 Nervio vago como vía de señalización neuropsiquiátrica
Dentro del eje microbiota–intestino–cerebro, el nervio vago ocupa un lugar central como una de las principales vías neurales de comunicación entre el intestino y el sistema nervioso central. Su relevancia no radica únicamente en su función autonómica clásica, sino en su rol como sistema aferente in- teroceptivo capaz de integrar señales mecánicas, químicas e inmunológicas provenientes del medio visceral.
En el campo de la neuropsiquiatría, esta vía ha sido propuesta como un posible nexo entre procesos periféricos —incluida la actividad de la microbiota intestinal— y la modulación de circuitos centrales implicados en el estrés, la inflamación y el estado de ánimo.
Este apartado aborda el nervio vago desde una perspectiva fisiológica y crítica, diferenciando los mecanismos demostrados de aquellos aún hipotéticos dentro del eje microbiota–intestino–cerebro.
1.1 Por qué el nervio vago importa en el eje micro- biota–intestino–cerebro
El nervio vago representa una de las principales vías neurales más rápida y directa que conecta el intestino con el cerebro, mediante la cual el intestino transmite información al sistema nervioso central dentro del eje microbiota–intestino–cerebro. A diferencia de las vías humorales —como la circulación de citoquinas, hormonas o metabolitos microbianos—, la vía va- gal permite una señalización rápida, organizada y dependiente de aferencias viscerales específicas, lo que la convierte en un componente clave de la comunicación intestino–cerebro [1].
Desde el punto de vista funcional, el nervio vago actúa prin- cipalmente como un sistema sensorial interoceptivo. Aproxi- madamente el 80 % de sus fibras son aferentes, encargadas de detectar el estado fisiológico del tracto gastrointestinal y transmitir esa información al tronco encefálico para su inte- gración central [2]. Esta característica distingue al nervio vago de otras vías del eje microbiota–intestino–cerebro y explica su relevancia como canal de información, más que como simple efector autonómico.
En el marco del eje microbiota–intestino–cerebro, las hipó- tesis actuales sostienen que el nervio vago participa en la transmisión de señales intestinales que pueden influir en la regulación del estrés, la respuesta inflamatoria y ciertos aspec- tos del comportamiento. Estas señales no provienen de una interacción directa entre bacterias y fibras nerviosas, sino que son mediadas por mecanismos de transducción periférica que incluyen metabolitos microbianos, células enteroendocrinas y señales inmunológicas locales [1,3].
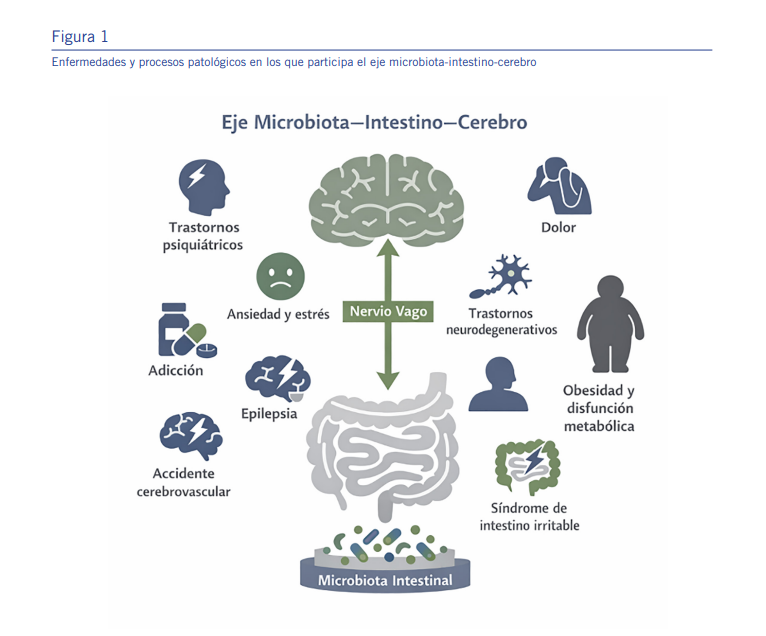
Sin embargo, es importante delimitar con claridad qué no sostiene la evidencia disponible. El nervio vago no constituye una vía causal única ni suficiente para explicar la influencia de la microbiota sobre los trastornos psiquiátricos. El eje microbiota–intestino–cerebro opera como una red compleja y redundante, en la que coexisten vías neurales, endocrinas e inmunológicas. La señalización vagal debe entenderse como un componente relevante de este sistema, pero no como un mecanismo exclusivo ni determinista (Ver Figura 1) [4].
En este sentido, además de la vía neural a través del nervio vago y/o la médula espinal, participan otras vías de comuni- cación, entre ellas la vía endocrina —a través del eje hipo- tálamo–hipófiso–adrenal (HPA)—, la vía inmune (citocinas) y la vía metabólica, que incluye metabolitos como los ácidos grasos de cadena corta (SCFA) y derivados del triptófano [2].
La relevancia clínica del nervio vago en psiquiatría se ve refor- zada por la evidencia indirecta proveniente de la estimulación del nervio vago en depresión resistente, así como por estudios experimentales que muestran la atenuación de ciertos efectos conductuales tras vagotomía o bloqueo vagal. No obstante, la extrapolación de estos hallazgos a la práctica clínica en hu- manos requiere cautela, ya que muchos de los efectos obser- vados dependen del contexto experimental y no se reproducen de manera uniforme [3,5].
En síntesis, el nervio vago importa en el eje microbiota–in- testino–cerebro porque constituye una vía neural rápida y fisiológicamente bien caracterizada de señalización intero- ceptiva. Su rol es relevante y necesario dentro del sistema, pero debe interpretarse en el marco de una red integradora más amplia, evitando reduccionismos que sobreestimen su alcance explicativo.
1.1 Anatomía funcional mínima imprescindible
Para interpretar adecuadamente el rol del nervio vago dentro del eje microbiota–intestino–cerebro, resulta imprescindible repasar algunos aspectos básicos de su anatomía funcional. Este encuadre evita extrapolaciones incorrectas y permite comprender tanto el alcance real como las limitaciones de la señalización vagal en neuropsiquiatría.
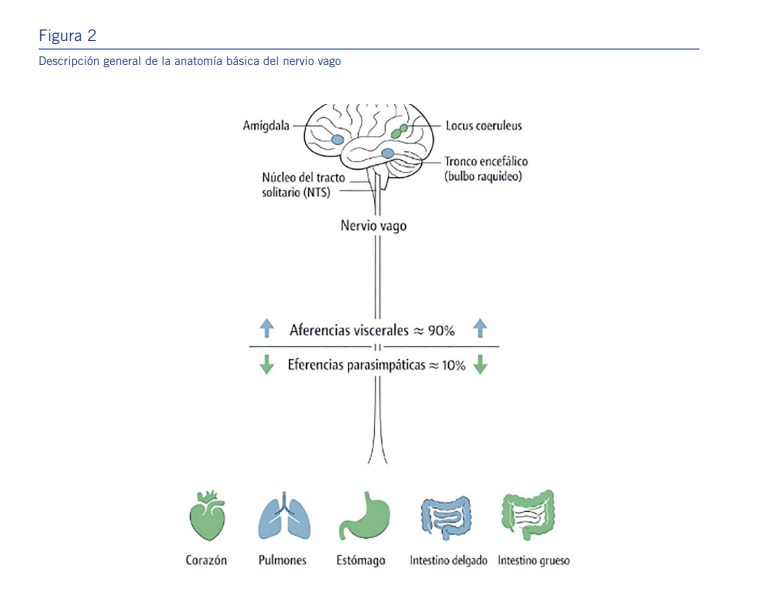
El nervio vago es un nervio mixto, pero con un marcado predo- minio aferente. Aproximadamente el 80 % de sus fibras son aferentes sensoriales, mientras que solo el 20 % corresponde a fibras eferentes parasimpáticas [1]. Este dato es central, ya que posiciona al nervio vago principalmente como un sen- sor interoceptivo visceral, más que como una vía motora o reguladora directa del intestino. Desde esta perspectiva, su función principal es informar al sistema nervioso central sobre el estado fisiológico del medio interno, coordinado a través del núcleo del tracto solitario (NTS) en el bulbo raquídeo.
Territorios viscerales relevantes
Las aferencias vagales inervan con una densidad decreciente que se extiende caudalmente desde el duodeno proximal, el íleon y la unión ileocecal, así como el resto del intestino del- gado y grueso hasta el nivel del colon transverso [1]. Por lo tanto, su distribución a lo largo del intestino no es homogénea, lo que sugiere una contribución diferencial de las vías neuro- nales según el segmento intestinal involucrado.
Desde un punto de vista funcional, esto implica que numero- sos procesos asociados a la microbiota intestinal —incluidos aquellos frecuentemente implicados en estados de disbiosis— pueden modular la función cerebral a través de mecanismos no exclusivamente vagales, tales como vías humorales, inmunológi- cas y metabólicas. En consecuencia, la participación del nervio vago en el eje microbiota–intestino–cerebro debe interpretarse como selectiva y dependiente del contexto regional y funcional, más que como una vía de señalización global y uniforme.
Nodos centrales de integración
Las aferencias vagales hacen sinapsis primaria en el núcleo del tracto solitario (NTS), ubicado en el bulbo raquídeo. El NTS constituye el principal centro de integración de la infor- mación viscerosensorial y representa un nodo clave dentro de la denominada red autonómica central. Desde allí, la infor- mación se transmite a otros núcleos del tronco encefálico y a estructuras del prosencéfalo (Ver Figura 2) [1].
A nivel neuroquímico, la transmisión vagal hacia el NTS es predominantemente glutamatérgica, con neuronas de segundo orden que expresan receptores de Þ-amino-3-hidroxi-5-metili- soxazol-4-propionato (AMPA), N-metil-D-aspartato (NMDA) y glutamato metabotrópico (mGlu). A ello se suma la expresión de diversos neuropéptidos, como la colecistoquinina y pépti- dos derivados de la proopiomelanocortina, que contribuyen a la especialización funcional de las neuronas del NTS. Estos perfiles neuroquímicos permiten que distintas poblaciones neuronales participen selectivamente en la regulación de res- puestas fisiológicas, emocionales y conductuales [1].
Psicofarmacología 26:139, marzo de 2026
Desde el NTS, la información interoceptiva se distribuye ha- cia múltiples circuitos cerebrales implicados, por ejemplo, en el control de la ingesta, la ansiedad, la respuesta al estrés y la modulación de la memoria, a través de proyecciones hacia estructuras como el núcleo parabranquial, el hipotálamo y la amígdala. Además, el NTS influye indirectamente sobre siste- mas neurotransmisores centrales clave, incluidos los circuitos noradrenérgicos, dopaminérgicos y serotoninérgicos. Esta po- sición estratégica le permite actuar como un nodo integrador fundamental para la señalización bidireccional entre el intesti- no y el cerebro dentro del eje microbiota–intestino–cerebro [1].
Implicancias para el eje microbiota–intestino– cerebro
Desde una perspectiva clínica y neuropsiquiátrica, la ana- tomía funcional del nervio vago obliga a interpretar su rol dentro del eje microbiota–intestino–cerebro como el de un mediador necesario en ciertos contextos, pero no como una vía suficiente ni exclusiva. La dependencia de territorios específicos, la convergencia central de señales y la coexis- tencia de vías alternativas refuerzan la idea de un sistema redundante y altamente integrado.
Comprender estas bases anatómicas resulta esencial para eva- luar críticamente estudios experimentales, interpretar corre- latos fisiológicos como el denominado “tono vagal” y evitar atribuciones causales excesivas en la práctica clínica.
1.1 Señal aferente: del intestino al tronco encefálico
La función principal del nervio vago dentro del eje microbio- ta–intestino–cerebro es la transmisión aferente de información visceral hacia el tronco encefálico.
De este modo, el sistema nervioso autónomo (SNA) proporcio- na al intestino la respuesta neurológica más directa disponi- ble, lo que provoca cambios rápidos en la fisiología intestinal mediante la inervación del órgano diana, tanto en condiciones de salud como de enfermedad, así como en la respuesta al dolor y al estrés [1].
Qué “tipo” de información viaja por el nervio vago
Las aferencias vagales no transportan información inespecífi- ca, sino señales bien definidas que pueden agruparse en tres grandes categorías:
- Información mecánica, relacionada con la distensión gás- trica e intestinal y los patrones de motilidad.
- Información química, vinculada a la presencia de nutrien- tes, metabolitos y cambios en el microambiente luminal.
- Información inmunológica, derivada de procesos inflama- torios locales y señales asociadas a la activación inmune pe- riférica. Este intercambio de moléculas a través de la capa mucosa y el epitelio facilita la comunicación entre el intestino
y el sistema inmune, a través del reconocimiento de antígenos propios y ajenos, y contribuye a la preparación del sistema in- mune para identificar patógenos potencialmente dañinos [1].
Este perfil funcional refuerza el rol del nervio vago como un sistema interoceptivo, más que como una vía directa de comu- nicación “microbiota–cerebro” en sentido estricto [1,2].
Rol de las células enteroendocrinas como sen- sores
Las fibras aferentes vagales se distribuyen a todas las capas de la pared digestiva, pero no cruzan la capa epitelial, por lo que no están en contacto directo con la microbiota luminal intestinal. Para detectar estas señales, deben hacerlo a través de la difusión de compuestos bacterianos o metabolitos, o mediante la intervención de otras células localizadas en el epitelio que retransmiten señales luminales. En este contex- to, las células enteroendocrinas (EEC) cumplen un rol cen- tral como mediadoras [2].
Las EEC son quimiosensores polimodales que integran señales extrínsecas e intrínsecas dentro del intestino y transmiten esta información al sistema nervioso [2].
Un punto clave para evitar interpretaciones erróneas es que las fibras vagales no contactan directamente con bacterias intestinales. En cambio, la detección de señales luminales ocurre a través de mecanismos de transducción periférica, en los que las células enteroendocrinas cumplen un rol central.
Estas células actúan como sensores especializados capaces de responder a:
- Nutrientes, liberando su contenido en presencia de car- bohidratos luminales, triglicéridos y proteínas, y modulando funciones gastrointestinales como la motilidad, la secreción y la ingesta de alimentos [2].
- Metabolitos microbianos (por ejemplo, ácidos grasos de cadena corta). Los metabolitos derivados de microbios intes- tinales más examinados son los SCFA, de los cuales más del 95 % consiste en acetato, propionato y butirato. Estos se han implicado en una variedad de procesos del huésped, inclu- yendo la función gastrointestinal, la regulación de la presión arterial, el ritmo circadiano y la función (neuro)inmune [1]. Estos metabolitos actúan principalmente a través de recep- tores acoplados a proteína G, como FFAR2 (GPR43) y FFAR3 (GPR41), así como mediante mecanismos epigenéticos como la inhibición de histona-desacetilasas (HDAC). Los receptores tipo Toll (TLR), en cambio, reconocen patrones moleculares asociados a microorganismos —como los lipopolisacáridos (LPS)— y participan en la señalización inmunológica, pero no constituyen la vía primaria de acción de los SCFA [2].
- Cambios en el entorno inflamatorio local. Al dirigirse las aferencias vagales al cerebro, la microbiota intestinal podría modular este reflejo inflamatorio a través de mecanismos peri- féricos que influyen sobre la actividad vagal [2].
Psicofarmacología 26:139, marzo de 2026
Por lo tanto, las células enteroendocrinas son actores clave en la detección del contenido bacteriano luminal y de productos bacterianos que pueden regular la motilidad gastrointestinal, la secreción y la ingesta de alimentos, a través de su efecto indirecto sobre las fibras aferentes vagales [2].
Como respuesta, liberan péptidos y neurotransmisores que ac- tivan aferencias vagales adyacentes, convirtiendo una señal luminal o metabólica en una señal neural organizada [6,7]. Este mecanismo representa uno de los puntos de convergen- cia más sólidos entre microbiota, intestino y sistema nervioso central dentro del eje microbiota–intestino–cerebro.
Señalización indirecta: microbiota ➔ metaboli- tos ➔ sensores intestinales ➔ nervio vago
La participación de la microbiota en la señalización vagal debe entenderse, en la mayoría de los casos, como indirecta. Los modelos más aceptados proponen que la microbiota influye sobre el sistema nervioso central a través de la producción de metabolitos —como los ácidos grasos de cadena corta— que modulan la actividad de células enteroendocrinas y otros sen- sores intestinales [1,4].
Además, procesos de inflamación de bajo grado o alteraciones de la barrera intestinal pueden amplificar la señal aferente va- gal, aumentando la transmisión de información inmunológica hacia el tronco encefálico. Este mecanismo resulta particular- mente relevante en contextos de estrés crónico, trastornos fun- cionales digestivos y condiciones asociadas a disbiosis [2,8].
Integración central de la señal aferente
Las señales aferentes vagales alcanzan el núcleo del tracto solitario (NTS), donde se integran con información proceden- te de otras vías viscerales y del estado autonómico general. Desde el NTS, esta información se distribuye hacia redes cen- trales que regulan la respuesta al estrés, la actividad neuroen- docrina y la homeostasis autonómica [1].
A través de conexiones anatómicas directas o indirectas me- diadas por el NTS, el nervio vago mantiene conexiones estruc- turales con diversas áreas cerebrales límbicas y corticales que participan en la regulación del estado de ánimo [7].
Si bien estas proyecciones explican cómo señales periféricas pueden influir en circuitos relacionados con el estado de áni- mo. En este sentido, el nervio vago transmite información in- teroceptiva primaria, cuya significación afectiva depende de procesos de integración cortical y límbica superiores.
Implicancias clínicas y conceptuales
Desde una perspectiva neuropsiquiátrica, la señal aferente vagal representa un mecanismo necesario, pero no exclusi- vo, para la traducción de señales intestinales al cerebro. Su funcionamiento depende del contexto fisiológico, del estado inflamatorio, del estrés y de la integridad de otros sistemas de señalización paralelos.
Comprender esta organización permite interpretar con mayor precisión tanto los hallazgos experimentales como los límites de su aplicación clínica, evitando atribuir a la microbiota o al nervio vago un rol causal directo en la génesis de síntomas psiquiátricos complejos.
1.2 Señal eferente: del sistema nervioso central al intestino
Aunque el nervio vago es predominantemente aferente, sus fibras eferentes parasimpáticas —que representan aproxima- damente el 20 % del total— cumplen un rol relevante en la modulación de funciones gastrointestinales clave dentro del eje microbiota–intestino–cerebro. Estas proyecciones permi- ten al sistema nervioso central influir activamente sobre el entorno intestinal, cerrando el circuito bidireccional que ca- racteriza a este eje.
Modulación autonómica de la función intestinal
Las señales inflamatorias detectadas por aferencias vagales, tras su integración en el núcleo del tracto solitario, pueden activar circuitos bulbares que generan una respuesta eferen- te vagal en el denominado reflejo antiinflamatorio colinérgico [2]. Las fibras eferentes se originan principalmente en el nú- cleo motor dorsal del vago, desde donde pueden modular los niveles circulantes de citocinas proinflamatorias [1].
Las fibras eferentes vagales participan en la regulación de:
- la motilidad gastrointestinal, ajustando el tránsito intesti- nal en función del estado autonómico;
- la secreción digestiva, incluyendo secreciones gástricas y pancreáticas;
- la integridad de la barrera intestinal, modulando la per- meabilidad epitelial.
Estas fibras participan en la regulación de la motilidad gas- trointestinal y de la integridad de la barrera intestinal, modu- lando la inflamación y la permeabilidad y, por extensión, el microambiente intestinal y la composición microbiana. Esta regulación no opera a nivel de especies bacterianas especí- ficas, sino que modula condiciones fisiológicas generales — como el tono autonómico, la inflamación local y la permea- bilidad epitelial— que favorecen o dificultan determinados perfiles microbianos [1,2].
Psicofarmacología 26:139, marzo de 2026
Señal eferente vagal e inflamación intestinal
Uno de los aspectos mejor caracterizados de la señal eferente vagal es su participación en la modulación de la respuesta inflamatoria periférica. A través de mecanismos colinérgicos, la activación vagal puede atenuar la producción de citoquinas proinflamatorias y contribuir al mantenimiento de la homeos- tasis inmunológica intestinal [2,3].
Este efecto resulta particularmente relevante en contextos de inflamación subclínica, donde la actividad vagal se ha asocia- do con la modulación de respuestas inmunológicas periféri- cas, las cuales pueden influir en la señalización aferente hacia el sistema nervioso central [1,2].
Estrés, eje HPA y tono vagal
La literatura revisada indica que el estrés puede influir sobre la actividad del nervio vago. Existe evidencia de que estados de estrés sostenido se asocian con un tono vagal reducido y con efectos inmunomoduladores alterados. Este fenómeno for- ma parte de la interacción entre vías neuronales, endocrinas e inmunológicas dentro del eje microbiota–intestino–cerebro, en el que el nervio vago puede desempeñar un papel modulador significativo [1–3].
Desde el punto de vista funcional, este cambio autonómico puede traducirse en:
- alteraciones de la motilidad intestinal;
- aumento de la permeabilidad intestinal;
- mayor activación inmunológica periférica.
Estos efectos crean un contexto fisiológico que favorece la amplificación de señales inflamatorias hacia el sistema ner- vioso central, estableciendo un posible vínculo entre estrés, disfunción intestinal y cambios en el estado de ánimo y el comportamiento [4,8].
El estrés favorece estados proinflamatorios, en contraste con el papel modulador antiinflamatorio atribuido a las fibras afe- rentes y eferentes del nervio vago. La exposición continua a múltiples estresores contrarresta la recuperación del tono pa- rasimpático, favoreciendo una mayor carga alostática. En este sentido, el estrés podría contrarrestar el efecto antiinflamato- rio general del nervio vago sobre la barrera epitelial y, de este modo, favorecer la disbiosis [2].
Conexión con depresión y trastornos relaciona- dos con el estrés
En pacientes con depresión y otros trastornos relacionados con el estrés se ha descrito, de forma consistente, un tono vagal reducido. Si bien esta asociación no implica causalidad directa, sugiere que la disfunción de la señal eferente vagal podría contribuir a un círculo vicioso entre estrés, inflamación periférica y alteraciones gastrointestinales [5,8].
Los cambios cerebrales en respuesta al estrés pueden aso- ciarse a una reducción del tono vagal y a un predominio de la actividad simpática y del eje HPA, lo que favorece la hiper- permeabilidad intestinal y la inflamación periférica, fenómeno relevante en el contexto de la depresión [8].
Este modelo es relevante porque sitúa al nervio vago como un modulador del contexto fisiológico, más que como una diana aislada responsable de síntomas específicos.
Implicancias conceptuales
La señal eferente vagal permite comprender cómo el sistema nervioso central influye activamente sobre el intestino y su en- torno inmunológico. Sin embargo, al igual que en la señaliza- ción aferente, su rol debe interpretarse como parte de una red reguladora compleja, en interacción con el sistema nervioso simpático, el eje HPA y los sistemas inmunológicos locales.
Reconocer estas interacciones es fundamental para evitar in- terpretaciones reduccionistas que atribuyan al nervio vago un control directo y exclusivo sobre la microbiota o los síntomas psiquiátricos.
1.3 El “reflejo antiinflamatorio colinérgico” y su relevancia psiquiátrica
Uno de los mecanismos mejor caracterizados que vinculan al nervio vago con la regulación inmunológica es el denominado reflejo antiinflamatorio colinérgico. Este circuito neuroinmu- nológico describe la capacidad del sistema nervioso central para modular activamente la respuesta inflamatoria periférica a través de vías vagales eferentes, constituyendo un ejemplo paradigmático de integración entre los sistemas nervioso e in- mune.
Bases biológicas del reflejo antiinflamatorio
Las aferencias vagales activan las eferencias vagales en un reflejo inflamatorio conocido como vía antiinflamatoria coli- nérgica. Este reflejo se activa cuando señales inflamatorias periféricas son detectadas por aferencias vagales y transmiti- das al tronco encefálico. Como respuesta, se genera una salida eferente vagal que, mediante la liberación de acetilcolina y su interacción con receptores nicotínicos Þ7 expresados en cé- lulas inmunes periféricas, inhibe la producción de citoquinas proinflamatorias [1,2].
Además, se ha propuesto que determinadas células gliales contribuyen a la preservación de la barrera epitelial intesti- nal frente al ataque de bacterias intestinales, aumentando la expresión de proteínas de unión estrecha —como la ocludina y ZO-1— a través de la secreción de S-nitrosoglutatión [2]. En consecuencia, la actividad vagal cumple una función pro- tectora sobre la barrera epitelial intestinal, mientras que una actividad vagal baja se asocia con un aumento de la permea- bilidad intestinal, favoreciendo la inflamación sistémica y la enfermedad crónica [2].
Psicofarmacología 26:139, marzo de 2026
Este mecanismo ha sido demostrado de forma consistente en modelos experimentales. Sus efectos no solo son relevantes para la neurodegeneración y la reparación tisular, sino que también podrían estar involucrados en la manifestación de trastornos psiquiátricos. En el contexto del eje microbiota– intestino–cerebro, este reflejo adquiere especial relevancia, dado que la inflamación de bajo grado es un componente frecuente tanto en trastornos gastrointestinales funcionales como en diversas condiciones psiquiátricas [2,3].
Nervio vago, inflamación y eje microbiota–intes- tino–cerebro
La activación del reflejo antiinflamatorio colinérgico puede in- fluir indirectamente sobre el entorno intestinal al:
- reducir la inflamación local;
- contribuir al mantenimiento de la integridad de la barrera intestinal;
- modificar el contexto inmunológico en el que interactúa la microbiota.
Estos efectos no implican una regulación directa de la compo- sición microbiana, sino una modulación del medio fisiológico que puede favorecer estados de mayor homeostasis intestinal [1,3].
Desde esta perspectiva, el nervio vago no actúa como un controlador directo de la microbiota, sino como un regulador del tono inflamatorio que condiciona la señalización aferente hacia el sistema nervioso central.
Relevancia psiquiátrica: qué es robusto y qué es inferido
Desde el punto de vista psiquiátrico, la biología del reflejo antiinflamatorio colinérgico es robusta y se encuentra bien es- tablecida. Sin embargo, su impacto directo sobre los síntomas afectivos debe interpretarse con cautela.
La evidencia disponible apoya que:
- la inflamación periférica puede modular circuitos cerebra- les implicados en el estado de ánimo;
- el nervio vago participa en la regulación de dicha inflama- ción.
Lo que no está demostrado de forma concluyente es que la activación del reflejo antiinflamatorio colinérgico, por sí sola, produzca una mejoría clínica directa y sostenida de los sínto- mas psiquiátricos en humanos [4,5].
En este sentido, el reflejo antiinflamatorio debe entenderse como un mecanismo integrador, potencialmente relevante dentro de un modelo multifactorial de depresión y trastornos relacionados con el estrés, pero no como una explicación cau- sal única.
Implicancias clínicas y conceptuales
La identificación del reflejo antiinflamatorio colinérgico ha contribuido a reforzar el interés por estrategias terapéuticas que modulen el tono vagal, como la estimulación del nervio vago.
Si bien modular el nervio vago puede tener efectos terapéu- ticos, principalmente asociados a sus propiedades antiinfla- matorias y moduladoras del estrés [3], desde una perspectiva psicofarmacológica resulta esencial evitar la extrapolación di- recta entre:
- modulación inflamatoria demostrada, y
- mejoría clínica afectiva asumida.
Reconocer esta distinción permite integrar el reflejo antiin- flamatorio dentro de un marco neurobiológico coherente, sin sobredimensionar su alcance terapéutico en psiquiatría.
1.1 Microbiota ➔ nervio vago: mecanismos pro- puestos
El interés creciente por la relación entre la microbiota in- testinal y el nervio vago ha llevado a proponer diversos me- canismos mediante los cuales señales de origen microbiano podrían influir sobre la actividad vagal. Sin embargo, es fun- damental subrayar que, en la mayoría de los casos, estos mecanismos son indirectos, contextuales y moduladores, y no establecen una relación causal simple entre microbiota y función cerebral.
Metabolitos microbianos como moduladores in- directos
Estos metabolitos no estimulan directamente las fibras vaga- les, sino que modulan la actividad de células enteroendocrinas y otros sensores intestinales, que a su vez activan aferencias vagales y envían información intestinal al sistema nervioso central, donde se integra en la red autonómica central para generar una respuesta adaptativa o, en algunos casos, desa- daptativa [1,2].
Esto se debe a que las fibras aferentes vagales se distribuyen por todas las capas de la pared digestiva, pero no están en contacto directo con la microbiota luminal intestinal, ya que no atraviesan la capa epitelial. En este sentido, las fibras solo pueden detectar indirectamente las señales de la microbiota, mediante la difusión de compuestos o metabolitos bacteria- nos, o a través de otras células ubicadas en el epitelio que transmiten señales luminales [2].
Por esta razón, las células enteroendocrinas son clave en la detección del contenido bacteriano luminal y de productos bacterianos, a través de su efecto indirecto sobre las fibras aferentes vagales [2].
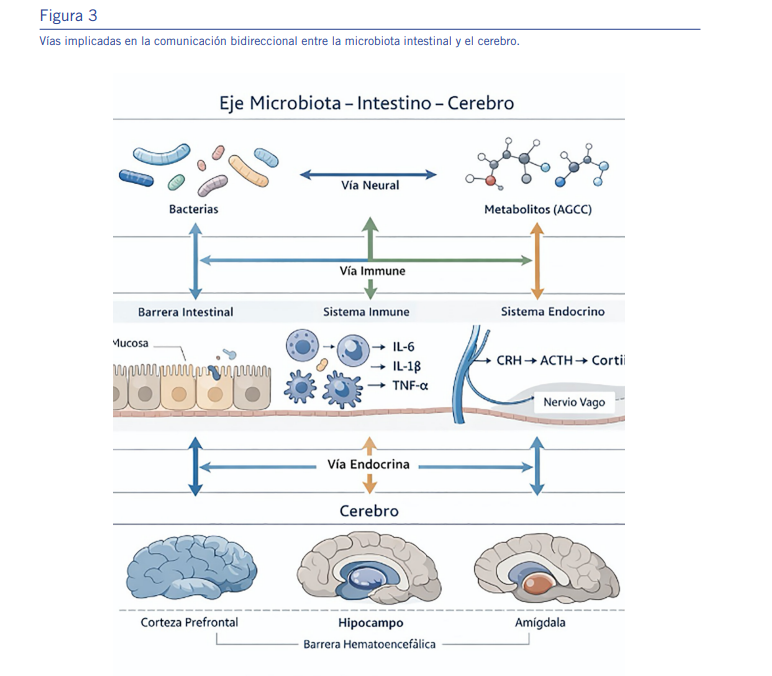
Este modelo permite comprender cómo cambios en la compo- sición o actividad metabólica de la microbiota pueden tradu- cirse en variaciones en la señalización interoceptiva, sin asu- mir una comunicación directa “bacteria–neurona” (Ver Figura 3). Desde una perspectiva neuropsiquiátrica, este punto es clave para evitar interpretaciones reduccionistas sobre el rol de probióticos o psicobióticos.
Señalización inflamatoria periférica como dispa- rador aferente
Otro mecanismo plausible es la activación aferente vagal se- cundaria a inflamación periférica. Alteraciones de la microbio- ta pueden asociarse a un aumento de mediadores inflamato- rios locales o sistémicos, los cuales pueden activar aferencias vagales directa o indirectamente, a través de mediadores infla- matorios como citoquinas y prostaglandinas [3].
En este contexto, el nervio vago actúa como un sensor del estado inmunológico periférico, transmitiendo al tronco en- cefálico información sobre la intensidad y persistencia de la respuesta inflamatoria. Este mecanismo ha sido bien caracte- rizado desde el punto de vista fisiológico, aunque su traduc- ción directa a síntomas psiquiátricos sigue siendo indirecta y dependiente de múltiples factores [4].
Cambios en la barrera intestinal y señalización vagal
Las alteraciones de la integridad de la barrera intestinal re- presentan otro mecanismo propuesto de interacción microbio- ta–vago. El epitelio intestinal constituye una barrera esencial
Psicofarmacología 26:139, marzo de 2026
para prevenir la translocación de bacterias y otros agentes [2]. El aumento de la permeabilidad intestinal puede facilitar el pasaje de componentes microbianos o mediadores inflamato- rios al compartimento subepitelial, amplificando la activación de sensores inmunológicos y, secundariamente, de aferencias vagales [2,8].
La actividad vagal cumple un rol protector sobre la barrera epi- telial intestinal. Una actividad vagal baja se asocia con mayor permeabilidad intestinal, promoviendo inflamación sistémica y enfermedad crónica [2].
Este modelo es plausible y coherente con la fisiopatología de los trastornos funcionales digestivos y con estados de estrés crónico. Sin embargo, la evidencia disponible no permite afir- mar que los cambios en la barrera intestinal conduzcan de manera directa y específica a alteraciones neuropsiquiátricas mediadas por el nervio vago.
Un marco integrador sin causalidad lineal
En conjunto, los mecanismos propuestos describen un sis- tema en el que la microbiota modula el contexto fisiológico en el que opera el nervio vago, influyendo sobre metabolitos, inflamación y barrera intestinal. El nervio vago, a su vez, trans- mite esta información al sistema nervioso central como señal interoceptiva.
Desde una perspectiva clínica y psicofarmacológica, resulta fundamental enfatizar que estos modelos no demuestran una causalidad directa microbiota ➔ nervio vago ➔ síntomas psi- quiátricos. Más bien, describen un entramado de interaccio- nes en el que el nervio vago puede actuar como mediador ne- cesario en ciertos contextos, pero no como un factor suficiente ni exclusivo.
Reconocer estas limitaciones conceptuales es esencial para una interpretación crítica de la literatura y para evitar extrapo- laciones terapéuticas no sustentadas.
1.2 Nervio vago y circuitos del ánimo: traducción neuropsiquiátrica desde la fisiología
La relación entre el nervio vago y los circuitos del ánimo no debe interpretarse como una transmisión directa de estados emocionales desde el intestino al cerebro, sino como la modu- lación neural de redes centrales implicadas en la regulación del estrés, la reactividad emocional y la homeostasis autonó- mica. Esta modulación ocurre a través de circuitos bien defi- nidos del tronco encefálico, integrados jerárquicamente con centros hipotalámicos y límbicos [1,2].
El núcleo del tracto solitario como nodo de inte- gración interoceptiva
Las aferencias vagales provenientes del tracto gastrointestinal convergen en el núcleo del tracto solitario (NTS), que consti- tuye el principal centro de integración de señales viscerales
mecánicas, químicas e inmunológicas. El NTS no constituye un generador primario de estados afectivos conscientes, sino que procesa información interoceptiva y la redistribuye hacia múltiples nodos del sistema nervioso central [1,4].
Desde el NTS, la información se proyecta hacia:
- el núcleo motor dorsal del vago (DMV), modulando la sali- da parasimpática eferente;
- núcleos del tronco encefálico implicados en el control au- tonómico;
- el hipotálamo y, de forma indirecta, circuitos límbicos y corticales.
Esta organización anatómico-funcional explica cómo señales viscerales pueden influir sobre sistemas centrales relevantes para la psiquiatría sin constituir mensajes emocionales espe- cíficos [2].
Modulación de sistemas monoaminérgicos
A través de sus conexiones con el locus coeruleus y los nú- cleos del rafe, la actividad integrada en el NTS puede modular la reactividad de los sistemas noradrenérgico y serotoninérgi- co, ambos centrales para la regulación del estado de ánimo, la ansiedad y la respuesta al estrés [1,3].
Esta influencia se expresa como un ajuste del tono funcional y de la sensibilidad al estrés, más que como una determinación directa de síntomas afectivos. Desde esta perspectiva, el nervio vago actúa como un modulador del contexto neurobiológico, y no como un generador primario de estados emocionales [3,8].
Interacción con el eje del estrés
El circuito NTS–DMV se encuentra bajo una fuerte modulación descendente por parte del hipotálamo, la amígdala y regiones prefrontales. En condiciones de estrés crónico, la activación sostenida del eje hipotálamo–hipófiso–adrenal (HPA) se asocia con una inhibición del tono vagal y un predominio simpático [4,5].
Cabe destacar que numerosos trastornos del comportamien- to y del cerebro se relacionan con la exposición a estresores exógenos, la desregulación del eje HPA y los mecanismos in- dividuales de afrontamiento o resiliencia al estrés, todos ellos componentes de la respuesta al estrés que, en modelos experi- mentales y en algunos estudios clínicos, se han descrito como potencialmente modulados por la microbiota [1].
Este patrón autonómico se ha vinculado con:
- mayor reactividad inflamatoria periférica;
- menor capacidad de amortiguación fisiológica frente al estrés;
- mayor vulnerabilidad a trastornos del estado de ánimo.
Psicofarmacología 26:139, marzo de 2026
No obstante, estas asociaciones deben interpretarse dentro de un modelo multifactorial, sin asumir causalidad directa [5,8].
Marco integrador y límites interpretativos
Desde una perspectiva neuropsiquiátrica, el nervio vago debe conceptualizarse como un ejecutor de regulaciones centrales, cuya actividad depende de la integración sensorial en el NTS y de la modulación por centros superiores. El nervio vago no “decide”, no “produce emociones” ni actúa de forma autóno- ma; ejecuta respuestas parasimpáticas en función del estado global del organismo [2,4].
Este marco permite comprender por qué la señalización va- gal puede influir en procesos relevantes para la psiquiatría — como el estrés y la inflamación— sin constituir una vía causal suficiente para explicar síntomas afectivos complejos [3,8].
Implicancias para la psicofarmacología
Entender al nervio vago como un regulador neural activo, pero no como un productor primario de estados afectivos, resulta particularmente relevante para la psicofarmacología. Mientras los psicofármacos actúan directamente sobre sistemas de neurotransmisión centrales, el nervio vago modula el contexto autonómico e inmunológico en el que dichos sistemas operan. Esta distinción resulta clave para interpretar de forma crítica la evidencia sobre estimulación vagal y eje microbiota–intes- tino–cerebro [2,5].
1.3 Evidencia experimental clave: qué demuestra realmente
Gran parte del interés por el nervio vago dentro del eje micro- biota–intestino–cerebro se apoya en evidencia experimental obtenida principalmente en modelos animales, en los que se han utilizado estrategias como la vagotomía, el bloqueo far- macológico vagal o la estimulación vagal. Estos estudios han sido fundamentales para delimitar el rol del nervio vago, pero también imponen límites claros a la extrapolación clínica.
Estudios con vagotomía o bloqueo vagal: qué efectos “se apagan”
En modelos animales, la sección del nervio vago o la inhibi- ción de su señalización aferente puede abolir o atenuar deter- minados efectos conductuales y neurobiológicos inducidos por algunas manipulaciones microbianas específicas, tales como:
- cambios conductuales asociados a la administración de determinadas cepas bacterianas;
- modulación de respuestas al estrés;
- alteraciones en marcadores neuroinflamatorios centrales.
Estos hallazgos indican que el nervio vago puede ser nece-
sario para la expresión de algunos efectos intestino–cerebro, particularmente aquellos mediados por señales interoceptivas rápidas [1,2].
Sin embargo, un punto crítico es que no todos los efectos des- aparecen tras la vagotomía. Numerosos estudios muestran que:
- persisten respuestas centrales mediadas por vías humo- rales;
- se mantienen efectos dependientes de citoquinas circu- lantes o metabolitos;
- intervienen aferencias espinales no vagales.
Esto demuestra que el eje microbiota–intestino–cerebro es re- dundante y que el nervio vago no constituye la única vía de comunicación funcional [1,4].
Qué resultados no se “apagan” y por qué importa
La persistencia de efectos centrales tras la vagotomía es un hallazgo clave, ya que refuta modelos lineales del tipo micro- biota ➔ nervio vago ➔ cerebro. En particular:
- los cambios inflamatorios sistémicos pueden influir sobre el cerebro independientemente del nervio vago;
- las alteraciones endocrinas y metabólicas mantienen efec- tos centrales aun con la señalización vagal interrumpida.
Desde una perspectiva neuropsiquiátrica, esto refuerza la idea de que el nervio vago actúa como un mediador relevante en ciertos contextos, pero no como un requisito universal para toda señalización intestino–cerebro [3,4].
Lectura crítica de la evidencia experimental
La mayoría de los estudios que apoyan un rol central del nervio vago presentan limitaciones metodológicas que deben consi- derarse:
- uso de modelos animales jóvenes y genéticamente homo- géneos;
- intervenciones agudas que no reflejan condiciones clínicas crónicas;
- vagotomías que alteran profundamente la fisiología gas- trointestinal, generando efectos secundarios no específicos.
Además, la vagotomía no es una intervención selectiva: al seccionar el nervio se interrumpen múltiples funciones auto- nómicas, lo que dificulta atribuir los efectos observados a un mecanismo puntual [2,8].
Limitaciones de extrapolación a humanos
En humanos, la vagotomía no constituye un modelo experi- mental viable para estudiar la relación microbiota–cerebro.
Psicofarmacología 26:139, marzo de 2026
Por lo tanto, gran parte de la evidencia disponible es indirecta y se apoya en:
- correlatos fisiológicos del tono vagal;
- estudios de estimulación vagal;
- asociaciones clínicas entre inflamación, estrés y disfun- ción autonómica.
Esto implica que los hallazgos experimentales deben inter- pretarse como pruebas de plausibilidad biológica, y no como demostraciones causales directas aplicables a la clínica psi- quiátrica [3,5].
Implicancias conceptuales
La evidencia experimental permite afirmar que:
- el nervio vago puede ser necesario para ciertos efectos in- testino–cerebro;
- no es suficiente para explicar la totalidad de la comunica- ción entre microbiota, intestino y cerebro.
Desde un punto de vista conceptual, estos datos respaldan un modelo en el que el nervio vago actúa como un componente modulador dentro de una red de señalización redundante, más que como una vía causal exclusiva.
Esta lectura crítica resulta esencial para interpretar adecua- damente tanto la literatura preclínica como las expectativas terapéuticas en psiquiatría.
1.4 Evidencia en humanos: qué tenemos y qué falta
A diferencia de la evidencia experimental en modelos ani- males, el estudio del nervio vago dentro del eje microbiota– intestino–cerebro en humanos presenta limitaciones meto- dológicas importantes. No es posible realizar intervenciones invasivas como vagotomías experimentales, por lo que el co- nocimiento disponible se basa en medidas indirectas de la función vagal, estudios observacionales y ensayos clínicos con estimulación vagal.
Correlatos fisiológicos del “tono vagal”
En humanos, el concepto de tono vagal se evalúa habitual- mente mediante marcadores indirectos, siendo el más utiliza- do la variabilidad de la frecuencia cardíaca (HRV). Una mayor HRV se asocia con mayor modulación vagal cardíaca, mientras que una HRV reducida sugiere un menor control vagal cardía- co [1,2].
Diversos estudios han mostrado asociaciones entre:
- bajo tono vagal (HRV reducida);
- mayor inflamación sistémica;
- mayor carga de síntomas depresivos y ansiosos.
Estas asociaciones son consistentes, pero no implican cau- salidad. La HRV refleja principalmente la modulación vagal cardíaca y no permite inferir de manera directa la actividad vagal intestinal ni la señalización aferente relacionada con la microbiota [2,3].
Utilidad y límites de los marcadores indirectos
El uso de la HRV como proxy del tono vagal presenta varias limitaciones relevantes:
- evalúa predominantemente la rama cardioinhibitoria del nervio vago;
- está influida por múltiples factores, como la edad, la acti- vidad física, el uso de fármacos y el sueño;
- no distingue entre aferencias y eferencias vagales.
Por lo tanto, aunque la HRV aporta información útil sobre la modulación autonómica cardíaca, no constituye una medida específica de la comunicación microbiota–nervio vago–cerebro [3,8].
¿Existe evidencia directa microbiota ➔ nervio vago ➔ síntomas en humanos?
Hasta el momento, la evidencia directa que demuestre una secuencia causal microbiota ➔ activación vagal ➔ mejoría o empeoramiento de síntomas psiquiátricos en humanos es in- suficiente. La mayoría de los estudios disponibles muestran:
- asociaciones entre composición de la microbiota y sínto- mas afectivos;
- cambios en HRV o en marcadores inflamatorios en contex- tos de depresión o estrés;
- respuestas clínicas variables y generalmente de pequeño tamaño de efecto a intervenciones sobre la microbiota.
Sin embargo, estos estudios no permiten aislar de manera concluyente el rol específico del nervio vago frente a otras vías del eje microbiota–intestino–cerebro, como la señalización in- mune o endocrina [3,5].
Estudios de intervención y su interpretación
Algunos ensayos clínicos que evalúan intervenciones sobre la microbiota —como probióticos o intervenciones dietarias con potencial impacto sobre la microbiota— han reportado cambios modestos en variables psicológicas o autonómicas. No obstante:
- los efectos suelen ser pequeños y heterogéneos;
- los mecanismos subyacentes no están claramente estable- cidos;
- no puede asumirse que los cambios observados estén me- diados predominantemente por el nervio vago.
Psicofarmacología 26:139, marzo de 2026
Desde una perspectiva psicofarmacológica, estos hallazgos deben interpretarse como exploratorios, más que como evi- dencia confirmatoria de una vía vagal causal [4,5].
Qué falta para avanzar
Para clarificar el rol del nervio vago en humanos dentro del eje microbiota–intestino–cerebro, se requieren:
- el desarrollo de biomarcadores más específicos que permi- tan estimar la actividad vagal intestinal en humanos;
- diseños experimentales que integren medidas autonómi- cas, inflamatorias y neuropsiquiátricas;
- estudios longitudinales que permitan evaluar direccionali- dad y contexto.
Hasta tanto estos datos estén disponibles, el nervio vago debe considerarse un mediador plausible, pero no demostrado, de la relación entre microbiota y síntomas psiquiátricos en hu- manos.
Implicancias clínicas
Desde la práctica clínica, la evidencia actual no justifica:
- inferir causalidad directa a partir de correlaciones auto- nómicas;
- utilizar marcadores de tono vagal como predictores aisla- dos de respuesta terapéutica.
Sí permite, en cambio, integrar la función vagal dentro de un modelo más amplio de regulación autonómica, inflamatoria y del estrés, relevante para la comprensión de la vulnerabilidad psiquiátrica.
1.5 Puente clínico: estimulación del nervio vago (VNS) y psiquiatría
La estimulación del nervio vago (VNS, por sus siglas en in- glés) constituye el principal punto de contacto clínico entre el nervio vago y la psiquiatría, aunque su desarrollo inicial estuvo vinculado al tratamiento de la epilepsia refractaria. Su posterior aprobación para depresión resistente al tratamiento ha contribuido de manera significativa al interés por el rol del nervio vago en los trastornos del estado de ánimo.
Fundamentos y desarrollo de la VNS
Desde el punto de vista neurobiológico, la estimulación vagal, aplicada a nivel cervical, activa predominantemente fibras afe- rentes que proyectan hacia el núcleo del tracto solitario (NTS), desde donde se distribuyen señales hacia múltiples regiones cerebrales, incluidas áreas involucradas en la regulación emo- cional, el estrés y la respuesta autonómica [1,3].
Evidencia clínica en depresión resistente
Los estudios clínicos sobre VNS en depresión resistente han mostrado resultados heterogéneos. Si bien algunos pacientes experimentan mejorías clínicas sostenidas, los efectos suelen ser graduales, variables y dependientes del tiempo de estimu- lación [5].
Es importante señalar que:
- la VNS no produce efectos antidepresivos inmediatos;
- las tasas de respuesta varían ampliamente entre estudios;
- gran parte de la evidencia proviene de estudios abiertos o con limitaciones metodológicas.
Hasta el momento, se dispone de datos observacionales y de seguimiento a largo plazo que sugieren beneficios en subgru- pos seleccionados.
Si bien existe abundante investigación preclínica que explora los mecanismos neurobiológicos de la VNS, la evidencia clíni- ca en depresión resistente proviene principalmente de ensayos clínicos y estudios observacionales en humanos, aunque con limitaciones metodológicas [5].
Qué demuestra realmente la VNS
Desde una perspectiva crítica, la VNS demuestra que la mo- dulación crónica del nervio vago puede influir sobre circuitos cerebrales relevantes para la psiquiatría. Sin embargo, no va- lida una relación causal directa entre microbiota intestinal, actividad vagal y mejoría clínica afectiva.
La VNS actúa como una intervención neuromoduladora cen- tral, cuyo mecanismo de acción involucra:
- activación de circuitos del tronco encefálico;
- modulación de sistemas monoaminérgicos;
- posibles efectos moduladores sobre la inflamación y el eje del estrés, cuya relevancia clínica específica en depresión aún se encuentra en estudio.
Estos mecanismos no implican que el nervio vago funcione como un mediador exclusivo ni suficiente de los trastornos del estado de ánimo [3,4].
Límites del “puente” microbiota–VNS
Un error conceptual frecuente consiste en extrapolar los efec- tos de la VNS a intervenciones periféricas sobre la microbiota. La estimulación eléctrica directa del nervio vago no es equi- valente a la modulación indirecta de señales intestinales, y no puede utilizarse como prueba de que cambios en la microbiota produzcan efectos clínicos mediadas por la vía vagal.
Desde este punto de vista, la VNS debe interpretarse como un modelo experimental y terapéutico de neuromodulación cen-
Psicofarmacología 26:139, marzo de 2026
tral, y no como una validación clínica del eje microbiota–ner- vio vago–cerebro en sentido causal [2,5].
Implicancias para la práctica clínica y concep- tuales
Para el clínico, la VNS representa una opción terapéutica es- pecífica, indicada en depresión mayor resistente al tratamien- to tras el fracaso de múltiples intervenciones farmacológicas y psicoterapéuticas convencionales. Su existencia refuerza la relevancia del nervio vago como modulador neurobiológico, pero también subraya la necesidad de prudencia al interpretar su significado para otras intervenciones no invasivas o perifé- ricas.
En síntesis, la VNS aporta evidencia de que la modulación vagal puede influir en circuitos centrales del ánimo, pero no justifica inferencias directas sobre el rol de la microbiota ni sobre intervenciones dirigidas a ella como estrategias antide- presivas equivalentes.
1.6 Riesgos de simplificación y errores en la in- terpretación clínica
El creciente interés por el nervio vago dentro del eje micro- biota–intestino–cerebro ha favorecido, en los últimos años, la proliferación de interpretaciones simplificadoras que exceden la evidencia disponible.
El nervio vago no es una vía directa “microbio- ta–cerebro”
Uno de los errores conceptuales más frecuentes consiste en asumir que el nervio vago transmite señales directas desde la microbiota intestinal hacia el cerebro. Como se ha desarro- llado previamente, las fibras vagales no atraviesan el epitelio intestinal ni establecen contacto directo con bacterias lumi- nales. Su activación ocurre de manera indirecta, mediada por células enteroendocrinas, metabolitos microbianos y señales inmunológicas [1,2].
Reducir este sistema complejo a una comunicación directa “bacteria–neurona” conduce a interpretaciones erróneas sobre los mecanismos implicados y sobre el potencial terapéutico de intervenciones dirigidas a la microbiota.
Confusión entre correlación y causalidad
La coexistencia de alteraciones en la microbiota, cambios en marcadores autonómicos y síntomas psiquiátricos no implica una relación causal directa ni unidireccional.
En particular, asociaciones entre menor modulación vagal cardíaca (inferida a partir de HRV), inflamación y depresión deben interpretarse como correlaciones dentro de un sistema multifactorial, en el que múltiples variables interactúan de
manera dinámica. Asumir que la modulación de una de estas variables producirá necesariamente un efecto clínico específi- co representa una simplificación excesiva [3,5].
En humanos, el tono vagal, suele inferirse a partir de la varia- bilidad de la frecuencia cardíaca (HRV), que refleja principal- mente la modulación vagal cardíaca.
Como se ha señalado, la HRV no constituye una medida direc- ta de la actividad vagal intestinal ni permite inferir de manera específica la señalización aferente relacionada con la micro- biota. Utilizarla como marcador específico de la comunicación microbiota–intestino–cerebro puede conducir a conclusiones erróneas y a sobreinterpretaciones clínicas [2,3].
Extrapolación indebida de modelos animales
Muchos de los datos que sustentan el interés por el nervio vago provienen de estudios en modelos animales. Si bien es- tos estudios aportan información valiosa sobre plausibilidad biológica, presentan limitaciones significativas cuando se ex- trapolan a humanos.
Las diferencias en la organización cortical superior, la com- plejidad inmunológica y el contexto ambiental, así como la naturaleza aguda de muchas intervenciones experimentales, limitan la validez externa de estos hallazgos. La extrapolación directa de resultados obtenidos en roedores a la clínica psi- quiátrica humana debe realizarse con extrema cautela [4,8].
Riesgos terapéuticos de la simplificación
La simplificación excesiva del rol del nervio vago puede favore- cer la promoción de intervenciones terapéuticas no validadas, basadas en supuestos mecanísticos incompletos. Esto incluye la prescripción indiscriminada de probióticos, suplementos o técnicas de estimulación vagal no reguladas o sin validación clínica adecuada.
Desde una perspectiva clínica, resulta esencial mantener una lectura crítica de estos modelos, diferenciando claramente entre plausibilidad teórica, evidencia experimental y eficacia clínica demostrada.
Necesidad de un marco interpretativo riguroso
Reconocer estos riesgos no implica descartar el rol del nervio vago dentro del eje microbiota–intestino–cerebro, sino inte- grarlo de manera adecuada dentro de un marco conceptual riguroso y multifactorial. Este enfoque permite aprovechar los aportes del modelo sin caer en reduccionismos ni promesas terapéuticas infundadas.
1.7 Conclusión integradora
El análisis del nervio vago dentro del eje microbiota–intesti- no–cerebro permite integrar múltiples niveles de organización
Psicofarmacología 26:139, marzo de 2026
biológica, desde la señalización periférica intestinal hasta la modulación de circuitos centrales relevantes para la regula- ción del estrés, la inflamación y el estado de ánimo. A lo largo de esta revisión se ha puesto de manifiesto que el nervio vago constituye una vía neural fisiológicamente bien caracterizada, con un rol relevante como mediador de señalización interocep- tivan, pero no como una vía causal exclusiva ni determinista.
Desde el punto de vista anatómico y funcional, el predominio aferente del nervio vago y su convergencia en el núcleo del tracto solitario (NTS) lo posicionan como un sensor del esta- do fisiológico visceral, capaz de integrar señales mecánicas, químicas e inmunológicas. Esta información es redistribuida hacia redes centrales que regulan la respuesta autonómica, el eje del estrés y procesos neuroendocrinos, sin codificar de manera directa estados emocionales.
La evidencia experimental respalda que el nervio vago puede ser necesario para la expresión de determinados efectos intestino–cerebro, particularmente aquellos mediados por señales rápidas e interoceptivas. Sin embargo, la persistencia de efectos centrales tras la interrupción de la señalización vagal y la coexistencia de vías humorales, endocrinas e inmunológicas refuerzan la noción de un sistema redundante y multifactorial.
En humanos, la evidencia disponible es mayoritariamente indirecta. Los correlatos fisiológicos del tono vagal, como la variabilidad de la frecuencia cardíaca, aportan información relevante sobre la modulación autonómica cardíaca, pero no permiten inferir de manera específica la actividad vagal intestinal ni establecer relaciones causales con la microbiota o con los síntomas psiquiátricos. Del mismo modo, la estimulación del nervio vago aporta un modelo clínico de neuromodulación central, pero no valida extrapolaciones directas hacia intervenciones periféricas sobre la microbiota.
En conjunto, estos hallazgos sostienen que el nervio vago debe conceptualizarse como un mediador necesario en ciertos contextos del eje microbiota–intestino–cerebro, pero no como una vía suficiente ni exclusiva para explicar la complejidad de los trastornos psiquiátricos. Su relevancia radica en su capacidad potencial para modular el contexto autonómico e inflamatorio en el que operan los circuitos cerebrales, más que en actuar como un generador primario de estados afectivos.
Desde una perspectiva clínica y psicofarmacológica, este marco integrador permite interpretar con mayor precisión tanto la evidencia experimental como las expectativas terapéuticas asociadas al nervio vago, evitando reduccionismos y promoviendo una lectura crítica de los modelos emergentes. Reconocer los límites de la evidencia disponible resulta tan importante como valorar sus aportes, especialmente en un campo en rápida expansión y con alto impacto translacional.