Neurobiología de la adicción a la
nicotina: receptores nicotínicos,
neuroadaptaciones y circuitos de
recompensa y aversión
Resumen
La adicción a la nicotina constituye uno de los trastornos por uso de sustancias más prevalentes y persistentes a nivel global, con una elevada carga de morbimortalidad. Su base neurobiológica se sustenta en la interacción entre la farmacocinética de la nicotina, la activación de los receptores nicotínicos de acetilcolina (nAChR) y una serie de neuroadaptaciones que afectan múltiples circuitos cerebrales.
La nicotina actúa principalmente sobre receptores nAChR de alta afinidad, en particular el subtipo Þ4ß2, modulando la ac-tividad de neuronas dopaminérgicas en el área tegmental ventral y promoviendo la liberación de dopamina en el núcleo ac-cumbens. Este mecanismo constituye el núcleo del refuerzo positivo asociado al consumo. Sin embargo, la evidencia actual indica que la adicción a la nicotina no puede explicarse exclusivamente por la activación dopaminérgica, sino que involucra una interacción compleja entre sistemas de recompensa y aversión, incluyendo circuitos mediados por la habenula medial y el núcleo interpeduncular.
La exposición crónica a nicotina induce procesos de neuroadaptación, tales como la desensibilización y regulación positiva de los nAChR, alteraciones en la neurotransmisión glutamatérgica y gabaérgica y cambios en la plasticidad sináptica, que favore-cen la transición desde el consumo ocasional hacia la dependencia.
Desde una perspectiva psicofarmacológica, el conocimiento de estos mecanismos ha permitido el desarrollo de estrategias terapéuticas dirigidas a los nAChR, como los agonistas parciales y la terapia de reemplazo nicotínico. No obstante, las tasas de recaída continúan siendo elevadas, lo que refleja la complejidad de los procesos neurobiológicos involucrados.
El presente artículo revisa de manera integrada y actualizada los mecanismos moleculares, celulares y circuitales implicados en la adicción a la nicotina, destacando su relevancia clínica y terapéutica.
Palabra clave
Nicotina; adicción; receptores nicotínicos; dopamina; neuroadaptación; psicofarmacología
INTRODUCCIÓN
La adicción a la nicotina constituye uno de los trastornos por uso de sustancias más prevalentes a nivel global y una de las principales causas de morbimortalidad evitable. A pesar de décadas de investigación y de la implementación de políti-cas de control del tabaco, el consumo de nicotina —tanto en productos combustibles como en dispositivos electrónicos—continúa representando un desafío significativo para la salud pública y la práctica clínica [1].
Desde una perspectiva neurobiológica, la adicción a la nicoti-na resulta de la interacción entre propiedades farmacocinéti-cas que facilitan su rápido acceso al sistema nervioso central, la activación de receptores nicotínicos de acetilcolina (nAChR) y una serie de neuroadaptaciones que afectan múltiples cir-cuitos cerebrales implicados en la recompensa, la motivación, el aprendizaje y el control inhibitorio [2,3].
Clásicamente, el modelo explicativo se ha centrado en la acti-vación del sistema dopaminérgico mesolímbico, particularmente en la liberación de dopamina desde el área tegmental ventral hacia el núcleo accumbens. Este mecanismo subyace al refuerzo positivo asociado al consumo. Sin embargo, la evidencia reciente indica que este modelo es incompleto y que la adicción debe entenderse como el resultado de una interacción dinámica entre circuitos de recompensa y de aversión, incluyendo estructuras como la habenula medial y el núcleo interpeduncular, que mo-dulan la respuesta negativa al consumo y la abstinencia [3,4].
Asimismo, la exposición crónica a nicotina induce procesos complejos de neuroadaptación, tales como la desensibiliza-ción y regulación positiva de los nAChR, alteraciones en la neurotransmisión glutamatérgica y gabaérgica y cambios en la plasticidad sináptica que favorecen la transición desde el con-sumo ocasional hacia la dependencia y la recaída [2,5]. Estos procesos no son homogéneos y se encuentran modulados por factores individuales, incluyendo la vulnerabilidad genética, la edad de inicio del consumo y variables relacionadas con el sexo biológico [6].
En este contexto, la comprensión de los mecanismos neurobio-lógicos de la adicción a la nicotina adquiere una relevancia cen-tral para el desarrollo de estrategias terapéuticas más eficaces. Si bien intervenciones como la terapia de reemplazo nicotínico y los agonistas parciales de los nAChR han demostrado eficacia clínica, las tasas de recaída continúan siendo elevadas, lo que refleja la complejidad de los mecanismos involucrados [1,7].
El presente artículo tiene como objetivo revisar de manera in-tegrada y actualizada los mecanismos moleculares, celulares y circuitales implicados en la adicción a la nicotina, con es-pecial énfasis en el papel de los receptores nicotínicos, las neuroadaptaciones inducidas por el consumo crónico y su re-levancia en la práctica psicofarmacológica.
Farmacocinética de la nicotina y acceso al siste-ma nervioso central
La farmacocinética de la nicotina constituye un determinante central de su potencial adictivo, ya que condiciona la velocidad,
intensidad y duración de su acción sobre el sistema nervioso central. A diferencia de otras sustancias psicoactivas, la nicotina presenta una absorción extremadamente rápida cuando es inhalada a través del humo del tabaco, alcanzando el cerebro en aproximadamente 10 a 20 segundos tras cada inha-lación [1,2].
Esta rápida distribución está facilitada por su alta liposolubilidad y su capacidad para atravesar eficientemente la barrera hematoencefálica. Como consecuencia, se generan picos rá-pidos de concentración arterial que favorecen un patrón de refuerzo intermitente altamente eficaz, similar al observado con otras drogas de abuso de acción rápida [2,3].
Una vez en el sistema nervioso central, la nicotina se une a los receptores nicotínicos de acetilcolina (nAChR), activándolos de manera transitoria pero repetida con cada inhalación. Este patrón de administración pulsátil resulta clave para el desarrollo de la dependencia, ya que promueve fenómenos de aprendizaje asociativo y refuerzo conductual vinculados a señales ambientales y contextuales [3].
La vida media plasmática de la nicotina es relativamente corta, aproximadamente de 2 horas, lo que contribuye a la aparición de síntomas de abstinencia en períodos breves tras el cese del consumo. Este descenso rápido en los niveles plas-máticos favorece la administración repetida a lo largo del día para mantener la ocupación de los receptores y evitar el malestar asociado a la abstinencia [1,4].
El principal metabolito de la nicotina es la cotinina, cuya vida media más prolongada (aproximadamente 16–20 horas) la convierte en un biomarcador útil de exposición tanto en fuma-dores activos como en individuos expuestos al humo de tabaco ambiental [4].
Desde una perspectiva psicofarmacológica, la combinación de un inicio de acción rápido, una vida media corta y un patrón de administración repetitivo configura un perfil farmacocinético altamente reforzante. Este perfil favorece la transición desde el consumo experimental hacia la dependencia, al potenciar los mecanismos de refuerzo positivo y negativo que sostienen la conducta adictiva [2,3].
Asimismo, la velocidad de administración influye en la intensidad del efecto reforzador. Formas de consumo que permiten una absorción más lenta, como la terapia de reemplazo nicotínico, generan niveles plasmáticos más estables y menores picos de concentración, lo que reduce su potencial adictivo y explica su utilidad terapéutica en la cesación tabáquica [5].
Receptores nicotínicos de acetilcolina: subtipos, función y regulación
Los receptores nicotínicos de acetilcolina (nAChR) son cana-les iónicos activados por ligando pertenecientes a la familia de receptores ionotrópicos pentaméricos, cuya activación permite el flujo de cationes —principalmente sodio y calcio— generando despolarización neuronal y facilitando la liberación de neurotransmisores [2,8].
Estos receptores se distribuyen ampliamente en el sistema nervioso central y periférico, donde desempeñan un papel fundamental en la modulación de la neurotransmisión, la plasticidad sináptica y los procesos cognitivos. En el contexto de la adicción a la nicotina, los nAChR constituyen el princi-pal blanco molecular responsable de sus efectos psicoactivos [2,3].
Subtipos de nAChR y relevancia funcional
Los nAChR centrales están formados por combinaciones de subunidades α (α2–α10) y ß (ß2–ß4), cuya composición de-termina sus propiedades farmacológicas, cinéticas y funcionales. Entre los distintos subtipos, los receptores de alta afinidad que contienen las subunidades α4 y ß2 (α4ß2) son los más relevantes en la neurobiología de la adicción, ya que median gran parte de los efectos reforzadores de la nicotina [2,8].
Estos receptores se expresan densamente en regiones clave del sistema de recompensa, incluyendo el área tegmental ven-tral, el núcleo accumbens y la corteza prefrontal. Su activa-ción por nicotina incrementa la frecuencia de descarga de las neuronas dopaminérgicas y promueve la liberación de dopa-mina en el núcleo accumbens, constituyendo un mecanismo central del refuerzo positivo [3,8].
Otros subtipos también cumplen funciones relevantes. Los receptores que contienen la subunidad α6 participan en la modulación de la liberación dopaminérgica en el sistema mesolímbico, mientras que aquellos que contienen la subunidad
α5 se han vinculado con la regulación de la respuesta aversiva a la nicotina, particularmente en circuitos que incluyen benula medial y el núcleo interpeduncular [4,6,8].
Esta organización funcional sugiere que distintos subtipos de nAChR contribuyen de manera diferencial a los componentes de recompensa y aversión, estableciendo un equilibrio dinámico que influye en la conducta de consumo [4,8].
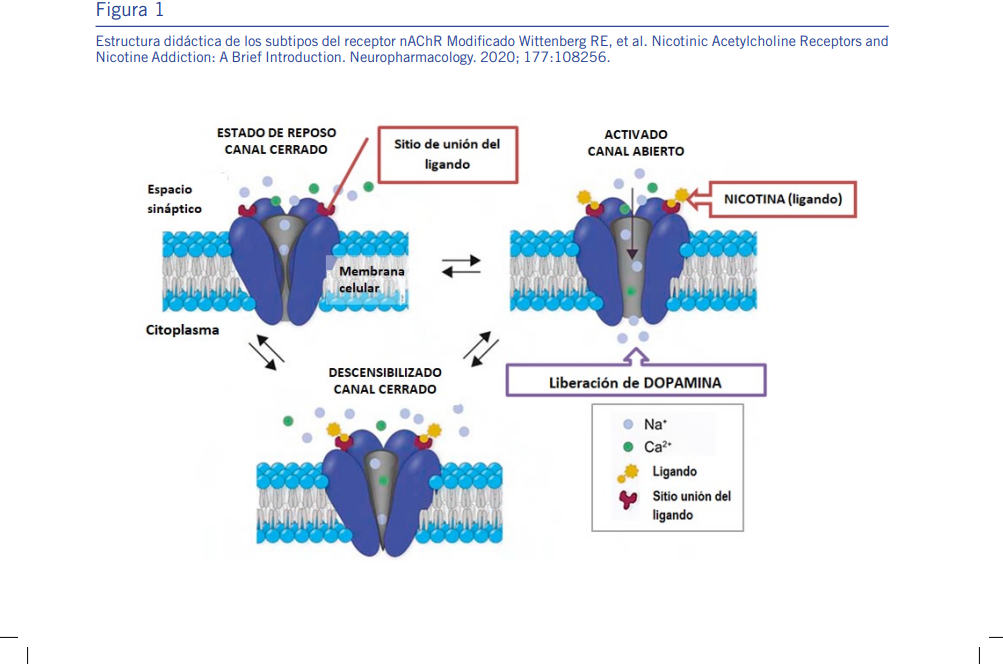
Activación, desensibilización y regulación de los receptores
La interacción de la nicotina con los nAChR presenta características que la diferencian del ligando endógeno acetilcolina. Mientras que esta última es liberada de manera transitoria y damente degradada, la nicotina persiste en el espacio sináptico, generando una activación más sostenida de los receptores [2].
Esta estimulación prolongada induce un fenómeno de des-ensibilización, en el cual los receptores entran en un estado funcionalmente inactivo a pesar de la presencia del ligando. De manera concomitante, la exposición crónica a nicotina pro-duce un aumento del número de receptores (upregulation), particularmente del subtipo α4ß2, lo que incrementa la sensi-bilidad del sistema a exposiciones posteriores [4,5].
Estos procesos constituyen una base molecular central de la tolerancia y la dependencia, al alterar la homeostasis colinér-gica y favorecer la necesidad de consumo repetido para man-tener la función neuronal basal [4].
Modulación de sistemas neurotransmisores
Los nAChR no actúan de manera aislada, sino que modulan múltiples sistemas de neurotransmisión. Su activación en el área tegmental ventral no solo estimula directamente las neu-ronas dopaminérgicas, sino que también influye sobre inter-neuronas gabaérgicas y aferencias glutamatérgicas, generando un efecto neto de aumento de la liberación de dopamina [3,5].
Además del sistema dopaminérgico, la nicotina modula la liberación de otros neurotransmisores relevantes, incluyendo glutamato, ácido y-aminobutírico, serotonina y noradrenali-na. Esta acción multimodal contribuye tanto a los efectos cognitivos y conductuales del consumo como a los síntomas de abstinencia [5].
Variabilidad genética y vulnerabilidad a la adicción
Las diferencias individuales en la susceptibilidad a la adic-ción a la nicotina están influenciadas, en parte, por variacio-nes genéticas en los genes que codifican las subunidades de los nAChR. En particular, variantes en el gen CHRNA5, que codifica la subunidad α5, se han asociado con un mayor riesgo de dependencia, mayor consumo y alteraciones en la respuesta a la nicotina [6].
Estos hallazgos sugieren que la función de los nAChR no solo determina los efectos farmacológicos de la nicotina, sino tam-bién la vulnerabilidad individual a desarrollar conductas adicti-vas, con implicancias relevantes para la medicina personaliza-da y el desarrollo de nuevas estrategias terapéuticas [6].
Circuitos neuronales de la adicción: recompen-sa, aversión y control inhibitorio
La adicción a la nicotina no puede comprenderse únicamente a partir de la activación dopaminérgica y mecanismos mole-culares o receptoriales, sino que emerge de la interacción di-námica entre múltiples circuitos neuronales que regulan la re-compensa, la aversión, el aprendizaje y el control conductual, implicando una interacción compleja entre múltiples sistemas neurotransmisores y circuitos neuronales [5]. En este contex-to, la nicotina actúa como un modulador farmacológico que al-tera el equilibrio funcional entre estos sistemas, favoreciendo la conducta de consumo y la persistencia de la adicción [3,8].
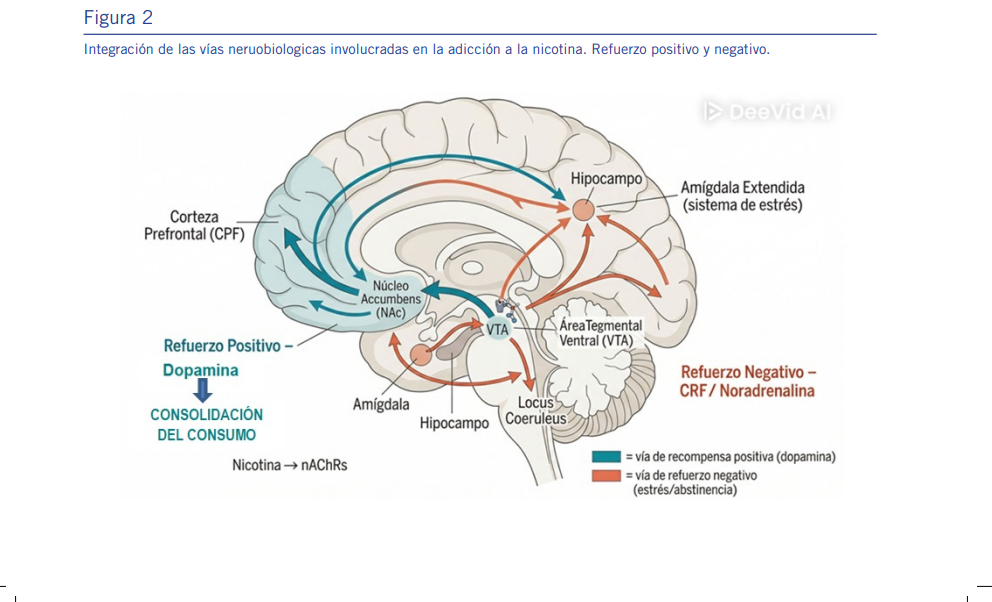
Circuito de recompensa mesolímbico
El circuito mesolímbico dopaminérgico constituye el núcleo del refuerzo positivo asociado al consumo de nicotina. Este circuito se origina en las neuronas dopaminérgicas del área tegmental ventral, que proyectan hacia el núcleo accumbens, la corteza prefrontal y otras estructuras límbicas [3,8].
La nicotina, al activar los nAChR en el área tegmental ven-tral, incrementa la frecuencia de descarga de estas neuronas y promueve la liberación de dopamina en el núcleo accum-bens. Este aumento se asocia con la codificación de estímulos salientes y con la atribución de valor motivacional a señales relacionadas con el consumo [3].
Sin embargo, la liberación dopaminérgica inducida por nicotina
depende de la interacción con aferencias glutamatérgicas exci-tatorias y gabaérgicas inhibitorias, que modulan la señal dopa-minérgica y su plasticidad. Estos sistemas son esenciales para la consolidación del refuerzo y la transición hacia la conducta adictiva [5,9].
Circuitos de aversión y regulación del consumo
Además de sus efectos reforzadores, la nicotina activa circuitos que generan respuestas aversivas y limitan la ingesta. Estos circuitos involucran principalmente la habenula medial y el núcleo interpeduncular, estructuras ricas en nAChR que con-tienen subunidades α5, α3 y ß4 [4,8].
La activación de estos circuitos produce señales negativas que contrarrestan el refuerzo, funcionando como un sistema de regulación del consumo. La evidencia actual indica que la sensibilidad de estos circuitos influye en la vulnerabilidad a la adicción, ya que su disfunción reduce la respuesta aversiva y facilita el consumo sostenido [4,6,9].
Este modelo de equilibrio entre recompensa y aversión repre-senta un cambio conceptual relevante en la comprensión de la adicción a la nicotina, superando los modelos centrados exclu-sivamente en la dopamina [8,9].
Control inhibitorio y corteza prefrontal
La corteza prefrontal desempeña un papel central en la regu-lación del comportamiento dirigido a objetivos, el control inhi-bitorio y la toma de decisiones. En el contexto de la adicción, esta región modula la capacidad para suprimir la conducta de consumo frente a estímulos asociados [3,10].
La exposición crónica a nicotina se asocia con alteraciones funcionales en estos circuitos, incluyendo cambios en la co-nectividad y en la eficiencia del control ejecutivo. Estas mo-dificaciones contribuyen a la pérdida de control conductual y a la persistencia del consumo a pesar de sus consecuencias negativas [5,10].
Además, la corteza prefrontal interactúa con el sistema meso-límbico, modulando la respuesta a señales de recompensa y participando en la regulación del craving y la recaída [3,10].
Integración funcional de los circuitos
En conjunto, la adicción a la nicotina puede entenderse como el resultado de una interacción dinámica entre circuitos de recompensa, sistemas de aversión y mecanismos de control inhibitorio. El predominio relativo de cada uno de estos siste-mas determina la conducta de consumo, la progresión hacia la dependencia y la vulnerabilidad a la recaída [3,5,8,9].
Aprendizaje, memoria y señales asociadas
La adicción a la nicotina implica la formación de asociaciones entre el consumo y estímulos ambientales, procesos que de-penden de circuitos que incluyen el hipocampo, la amígdala y la corteza prefrontal [5,11].
La nicotina potencia los mecanismos de plasticidad sinápti-ca en estas regiones, facilitando el aprendizaje asociativo y la
consolidación de memorias relacionadas con el consumo. Como consecuencia, estímulos contextuales pueden desenca-denar craving intenso y recaída incluso tras períodos prolonga-dos de abstinencia [11,12].
Asimismo, la nicotina actúa como un amplificador del valor incentivador de estímulos asociados, reforzando la saliencia de señales ambientales vinculadas al consumo [11].
Modelo integrador de la adicción a la nicotina
La evidencia actual indica que la adicción a la nicotina debe entenderse como un proceso que involucra múltiples sistemas interconectados. El refuerzo positivo mediado por dopamina, la regulación aversiva, la disfunción del control inhibitorio y los procesos de aprendizaje asociativo interactúan de manera dinámica para sostener la conducta adictiva [3,5,8,12].
Este modelo integrador permite explicar la persistencia del consumo, la dificultad para mantener la abstinencia y la ele-vada tasa de recaída, incluso en presencia de motivación para abandonar el hábito.
Neuroadaptaciones inducidas por la exposición crónica a nicotina
La exposición repetida a la nicotina induce una serie de neu-roadaptaciones a nivel molecular, celular y circuital que trans-forman el consumo ocasional en un patrón de uso compulsivo. Estos cambios reflejan procesos de plasticidad neuronal que alteran la homeostasis de los sistemas de neurotransmisión y constituyen la base biológica de la tolerancia, la dependencia y la recaída [4,8].
Figura 2
Desensibilización y regulación positiva de los nA-ChR
Uno de los mecanismos centrales de la neuroadaptación a la nicotina es la desensibilización de los receptores nicotínicos de acetilcolina (nAChR). La exposición sostenida induce un estado en el cual los receptores permanecen funcionalmente inactivos a pesar de la presencia del ligando [2,4].
De manera aparentemente paradójica, la exposición crónica también produce un aumento en el número de receptores (upregulation), particularmente del subtipo α4ß2. Este fenómeno incrementa la sensibilidad del sistema a la nicotina y contribuye a la dependencia, ya que el sistema colinérgico requiere niveles continuos de estimulación para mantener su funcionamiento basal [4,5].
Estos procesos alteran el equilibrio entre activación y desensibilización, favoreciendo la necesidad de consumo repetido y contribuyendo al desarrollo de tolerancia [4].
Plasticidad sináptica y cambios en circuitos de recompensa
La nicotina induce modificaciones en la plasticidad sináptica, particularmente en el sistema mesolímbico. Se han descrito cambios en la potenciación a largo plazo (LTP) y en la depresión a largo plazo (LTD) en circuitos dopaminérgicos, glutamatérgicos y gabaérgicos [8,12].
Estas adaptaciones fortalecen las conexiones sinápticas asociadas al consumo y a las señales ambientales relacionadas, facilitando el aprendizaje asociativo y consolidando patrones conductuales adictivos [5,11].
Además, la exposición crónica a nicotina se asocia con altera-ciones en la conectividad funcional entre regiones como el área tegmental ventral, el núcleo accumbens y la corteza prefrontal, lo que contribuye a la persistencia del comportamiento de bús-queda de la sustancia [10].
Tolerancia y dependencia
La tolerancia a la nicotina se desarrolla como resultado de las adaptaciones en los nAChR y en los circuitos neuronales. Con el tiempo, se requieren mayores niveles de nicotina para alcan-zar los mismos efectos subjetivos, lo que favorece el aumento del consumo [4].
La dependencia refleja un estado en el cual el sistema nervioso se adapta a la presencia continua de la sustancia. En ausen-cia de nicotina, estas adaptaciones generan un desequilibrio neuroquímico que se manifiesta como síntomas de abstinen-cia, incluyendo irritabilidad, ansiedad, disforia y alteraciones cognitivas [1,13].
El pasaje desde un predominio de refuerzo positivo (placer) hacia mecanismos de refuerzo negativo (evitación del ma-lestar) constituye un elemento central en la progresión de la adicción [13].
Abstinencia y estados afectivos negativos
Durante la abstinencia, la disminución de la actividad dopa-minérgica en el sistema mesolímbico, junto con la activación de sistemas relacionados con el estrés, contribuye a la apari-ción de estados afectivos negativos (Refuerzo o recompensa negativa) [13].
El locus coeruleus (LC) principal núcleo noradrenérgico. Se ac-tiva durante la abstinencia de nicotina, provocando síntomas y signos físicos.
Estos estados incluyen disforia, ansiedad y aumento de la re-actividad al estrés, y están mediados por la interacción entre sistemas neurotransmisores y neuropeptídicos, incluyendo el sistema corticotropo y otras vías vinculadas a la respuesta al estrés [13].
La intensidad de estos síntomas constituye un factor determi-nante en la recaída, ya que el consumo de nicotina alivia tran-sitoriamente estos estados, reforzando el ciclo adictivo [13].
Recaída y persistencia de la adicción
La recaída constituye una característica central de la adic-ción a la nicotina y refleja la persistencia de las neuroadap-taciones inducidas por el consumo crónico. Incluso tras pe-ríodos prolongados de abstinencia, la exposición a señales asociadas, el estrés o pequeñas cantidades de nicotina pue-den reactivar los circuitos de recompensa y desencadenar el consumo [11,13].
Estos fenómenos se explican por la consolidación de memo-rias asociativas y por cambios duraderos en la plasticidad si-náptica, que mantienen la vulnerabilidad a la recaída a largo plazo [5,11].
Vulnerabilidad del cerebro adolescente y riesgo de adicción
La adolescencia constituye un período crítico del neurodesa-rrollo caracterizado por una elevada plasticidad sináptica y una maduración aún incompleta de los circuitos prefrontales impli-cados en el control inhibitorio y la toma de decisiones [10,14].
En este contexto, la exposición a nicotina se asocia con una mayor sensibilidad a sus efectos reforzadores y con un incre-mento en la probabilidad de desarrollar dependencia. Estos efectos han sido vinculados a cambios en la expresión y fun-ción de los receptores nicotínicos, así como a modificaciones en la actividad de circuitos relacionados con la recompensa y el aprendizaje [10,14].
Asimismo, la menor maduración funcional de la corteza pre-frontal durante la adolescencia se asocia con una menor capa-cidad de control inhibitorio, lo que puede favorecer la impulsi-vidad y la vulnerabilidad a conductas adictivas [10].
En conjunto, estos hallazgos respaldan la noción de que la ex-posición a nicotina durante etapas tempranas del desarrollo ocurre en un contexto neurobiológico particularmente suscep-tible, en el que los efectos de la sustancia pueden tener un impacto más pronunciado sobre los sistemas que regulan la conducta motivada.
Implicancias psicofarmacológicas y terapéuticas
A pesar de la disponibilidad de tratamientos farmacológicos eficaces, la cesación sostenida del consumo de nicotina conti-núa siendo difícil de alcanzar. Metaanálisis recientes indican que, incluso bajo tratamiento farmacológico, una proporción significativa de los individuos recae durante el primer año tras un intento de abandono, con tasas que oscilan entre el 60% y el 80% [7]. Estos datos reflejan la persistencia de las neuro-adaptaciones inducidas por la nicotina y subrayan la compleji-dad del tratamiento de la dependencia.
Terapias dirigidas a los receptores nicotínicos
Los receptores nicotínicos de acetilcolina (nAChR), en particu-lar el subtipo α4ß2, constituyen el principal blanco farmacoló-gico en la cesación tabáquica.
La vareniclina, un agonista parcial de estos receptores, ha de-mostrado una eficacia superior al placebo y a otras interven-ciones farmacológicas en múltiples metaanálisis [7]. Su me-canismo combina una estimulación parcial del receptor —que reduce los síntomas de abstinencia— con un efecto antagonis-ta funcional que disminuye el refuerzo asociado al consumo.
En algunos contextos, limitaciones en el acceso a tratamientos de primera línea han motivado la exploración de alternativas terapéu-ticas. Entre ellas, la citisina, un alcaloide vegetal con acción como agonista parcial de los nAChR, ha mostrado eficacia en estudios clínicos, con un perfil farmacológico similar al de la vareniclina [15]. Su mecanismo de acción combina la atenuación de los sín-tomas de abstinencia con la reducción del efecto reforzador de la nicotina mediante bloqueo competitivo de los receptores.
Desde el punto de vista farmacocinético, la vareniclina presen-ta una vida media más prolongada que permite esquemas de dosificación más simples, mientras que la citisina requiere una administración más frecuente. Estudios recientes sugieren que la optimización de los esquemas de dosificación podría mejorar las tasas de cesación [15].
La terapia de reemplazo nicotínico, en sus distintas formula-ciones, proporciona niveles más estables de nicotina, evitando los picos rápidos asociados al cigarrillo. Este perfil farmaco-cinético reduce los síntomas de abstinencia y facilita la tran-sición hacia la abstinencia, aunque su eficacia es moderada y frecuentemente insuficiente para prevenir recaídas a largo plazo [7].
Modulación de sistemas dopaminérgicos y noradre-nérgicos
El bupropión, un inhibidor de la recaptación de dopamina y noradrenalina, constituye una alternativa terapéutica eficaz, particularmente en pacientes con síntomas afectivos asociados a la abstinencia. Su acción sobre los sistemas catecolaminérgi-cos contribuye a reducir el craving y mejorar el estado de ánimo durante el proceso de cesación [1,7].
La eficacia de estos tratamientos refuerza el concepto de que la adicción a la nicotina no depende exclusivamente de la activación colinérgica, sino de la interacción entre múltiples sistemas neurotransmisores, incluyendo aquellos implicados en la regulación del refuerzo, el estrés y el afec-to negativo [5,12].
Estrategias emergentes y modulación de la neuro-plasticidad
El reconocimiento de la adicción como un trastorno de la plas-ticidad neuronal ha impulsado el desarrollo de nuevas estrate-gias terapéuticas orientadas a modular estos cambios.
En este contexto, se han explorado intervenciones combi-nadas que incluyen farmacoterapia y técnicas de neuromo-dulación, (aprender habilidades nuevas, realizar actividad física, mantener una vida social activa, priorizar el sueño reparador y alimentación saludable) y la estimulación trans-craneal por corriente directa aplicada a la corteza prefrontal dorsolateral. Estudios recientes sugieren que estas inter-venciones pueden mejorar las tasas de abstinencia cuando se combinan con tratamientos farmacológicos, probable-mente mediante la modulación del control inhibitorio y de la plasticidad cortical [12].
Asimismo, el desarrollo de fármacos dirigidos a subtipos espe-cíficos de nAChR, así como la modulación de sistemas gluta-matérgicos y gabaérgicos, representa un campo emergente con potencial para mejorar la eficacia terapéutica [5,12].
Limitaciones terapéuticas y persistencia de la recaída
A pesar de los avances, los tratamientos actuales no logran revertir completamente las neuroadaptaciones inducidas por el consumo crónico de nicotina. La persistencia de memorias
asociativas, la sensibilización a señales ambientales, la activa-ción de circuitos de estrés durante la abstinencia y la disfun-ción del control inhibitorio contribuyen a una vulnerabilidad sostenida a la recaída [5,11,13].
Estos mecanismos explican por qué incluso intervenciones far-macológicas eficaces presentan limitaciones en su impacto a largo plazo, y refuerzan la necesidad de enfoques terapéuticos integrales que combinen estrategias farmacológicas, conduc-tuales y neurobiológicas.
Implicancias para la prevención
La dificultad para revertir las neuroadaptaciones inducidas por la nicotina subraya la importancia de las estrategias preventi-vas. La exposición temprana, especialmente durante la ado-lescencia, se asocia con cambios duraderos en los circuitos neuronales implicados en la recompensa, el aprendizaje y el control conductual, aumentando la vulnerabilidad a la depen-dencia [14].
En este contexto, la prevención del inicio del consumo adquie-re un papel central, ya que evita la instauración de procesos neurobiológicos que, una vez establecidos, resultan difíciles de modificar incluso con intervenciones terapéuticas eficaces.
Perspectivas futuras
Los avances en la comprensión de la neurobiología de la adic-ción a la nicotina sugieren que futuras estrategias terapéuticas podrían orientarse hacia:
- moduladores selectivos de subtipos específicos de nAChR
- intervenciones dirigidas a circuitos de aversión y estrés
- estrategias que modulen la plasticidad sináptica
- enfoques personalizados basados en perfiles genéticos
Estas aproximaciones podrían mejorar la eficacia de los tra-tamientos y reducir las tasas de recaída, particularmente en poblaciones de mayor vulnerabilidad [6,12].
Conclusión
La adicción a la nicotina constituye un trastorno complejo que emerge de la interacción entre mecanismos moleculares, circuitales y conductuales. La activación de los receptores nicotínicos de acetilcolina, junto con las neuroadaptaciones inducidas por la exposición crónica, conduce a una reorganización funcional de los sistemas de recompensa, aversión, aprendizaje y control inhibitorio que sostienen la conducta adictiva.
La evidencia actual indica que estos procesos no pueden explicarse exclusivamente por la activación dopaminérgica, sino que implican una interacción dinámica entre múltiples sistemas neurotransmisores y circuitos neuronales. Estas adaptaciones subyacen tanto a la transición hacia la dependencia como a la persistencia de la vulnerabilidad a la recaída.
Desde el punto de vista clínico, a pesar de la disponibilidad de intervenciones psico-conductuales y farmacológicas eficaces, la cesación sostenida continúa siendo limitada, con elevadas
tasas de recaída incluso bajo tratamiento. Este hecho pone de manifiesto que las estrategias actuales no logran revertir com-pletamente las neuroadaptaciones inducidas por la nicotina.
En este contexto, la integración entre los hallazgos neurobiológicos y la práctica clínica resulta fundamental para el desarrollo de abordajes terapéuticos más eficaces. Esto incluye no solo la optimización de los tratamientos existentes, sino también el desarrollo de intervenciones dirigidas a circuitos específicos,
la modulación de la plasticidad neuronal y la identificación de perfiles de vulnerabilidad individual.
En conjunto, estos avances refuerzan la necesidad de abordar la adicción a la nicotina como un trastorno neurobiológico per-sistente, en el que la prevención —particularmente en etapas tempranas del desarrollo— y el diseño de intervenciones más precisas constituyen desafíos centrales para la psicofarmacología contemporánea.






