Avances en el tratamiento de la agitación asociadaa la enfermedad de Alzheimer
Resumen
La mayoría de los pacientes con Enfermedad de Alzheimer padecen de algún trastorno neuropsiquiátrico, entre los cuales destaca la agitación. El abordaje de esta entidad representa un desafío, dada la complejidad de su patogénesis y de su presentación. El mismo incluye medidas no farmacológicas y también el uso de medicamentos. Los antipsicóticos fueron los fármacos mayormente usados en el tratamiento “fuera de rótulo” de la agitación con éxito modesto y problemas de seguridad. En 2023, la Food and Drugs Administration dio aprobación al brexpiprazol, siendo el primer medicamento autorizado para el abordaje de la agitación en Enfermedad de Alzheimer. En esta reseña se detallan sus características fundamentales y se las compara con su predecesor: el aripiprazol.
Palabras clave
Brexpiprazol – Alzheimer – Agitación – Antipsicóticos.
Scolari MJ. “Agitación en la enfermedad de Alzheimer”. Psicofarmacología Uruguay 2024;23:4-7.
Puede consultar otros artículos publicados por los autores en la revista Psicofarmacología en sciens.com.ar
Introducción
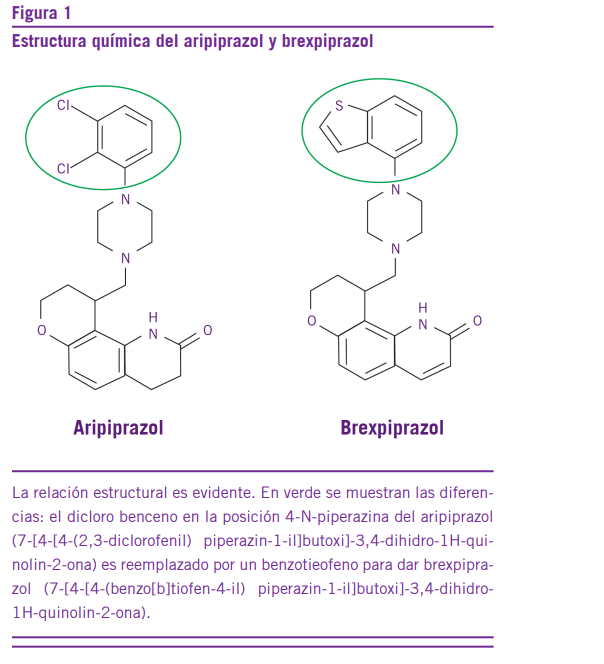
La prevalencia mundial de demencia, mayormente causada por la Enfermedad de Alzheimer (EA), se estima en alrededor de 50 millones de pacientes. Se espera que en 20 años este valor se duplique, poniendo de relieve la importancia de dicha entidad (1). Si bien la EA fue caracterizada, inicialmente, por deterioro cognitivo y demencia en pacientes con edad avanzada, está establecida su asociación a una gama de desórdenes neuropsiquiátricos entre los que se incluye ansiedad, apatía, trastornos del sueño, depresión, agitación, entre otros (2). Se estima que alrededor del 98% de los pacientes con EA manifestarán al menos uno de estos trastornos. Particularmente, la agitación posee una manifestación compleja que incluye agresión física (lanzamiento de objetos, empujones, tirones) y verbal (hablar en voz muy alta, gritos, insultos) por parte del paciente y aumento de la actividad motora (pacing, balanceo, inquietud, entre otras). Así, la agitación representa un síndrome altamente estresante para el paciente y su entorno, con aumento de los costos de asistencia y de la morbimortalidad (3). El abordaje inicial de la agitación hace referencia a medidas no farmacológicas, orientadas a la educación del cuidador del paciente en la detección de necesidades no satisfechas, como dolor, hambre, sed, temor al abandono, entre otras y en la implementación de estrategias como actividades de relajación y ejercicios de distracción orientados a evitar dichos disparadores (4). Aunque este tipo de abordaje ha demostrado cierta eficacia, sus beneficios se limitan a las formas más leves de agitación. Además, el entrenamiento del cuidador y/o familiar del paciente representa una limitación que, en algunos casos, ha llevado a los médicos tratantes a discontinuar las medidas no farmacológicas (4). Durante las últimas décadas no han existido fármacos aprobados por la Food and Drugs Administration (FDA) para abordar esta condición, por lo que se han empleado una variedad de medicamentos de manera off label, o fuera de rótulo, entre los que se encuentran: antipsicóticos, ansiolíticos, hipnóticos y antidepresivos. Sin embargo, los beneficios observados fueron modestos, a lo que suman problemas de adherencia y de seguridad (5). Si bien los antipsicóticos, sean típicos o no, han representado la piedra angular del abordaje de los trastornos de agitación, también han sido asociados a desenlaces indeseados como aumento de peso, caídas, mareos e incremento en la mor- talidad, especialmente en pacientes con edad avanzada (6). Brexpiprazol (BREX), es un antipsicótico estructural y farmacológicamente relacionado con el aripiprazol (ARI) (Figura 1), aprobado por la FDA para el tratamiento de la agitación aso- ciada a demencia en EA, en mayo de 2023.
Indicaciones aprobadas
Según la administración nacional de medicamentos, ali- mentos y tecnología médica (ANMAT), BREX se encuentra aprobado para:
Tratamiento de la esquizofrenia (DSMIV) y como tratamien- to complementario a los antidepresivos en el abordaje de tras- tornos depresivos mayores (DSM IV-TR) en pacientes adultos.
Nótese que, la aprobación por la FDA, antes mencionada, aún no ha llegado a la Argentina. El presente artículo se enfo- cará en dicha aprobación por considerarse novedosa.
Bases neurocientíficas y mecanismo de acción
Para comprender la eficacia del BREX debemos recurrir a conceptos elementales de farmacología y realizar un esfuerzo, en honor a la brevedad, por simplificar la neurobiología de la esquizofrenia. BREX es un antipsicótico atípico que actúa a nivel de distintos receptores sobre los cuales ejerce diferentes acciones. Se comporta como agonista parcial de los recep- tores 5-HT1A, D2 y D3, y como antagonista de los recepto- res 5-HT2A, 5-HT2B, 5-HT7, 1A, 1B, 1D y 2C (7). Al
igual que el ARI, el agonismo parcial sobre los receptores D2,
5-HT1A y el antagonismo 5-HT2A, podrían explicar los efec- tos antipsicóticos del BREX. El antagonismo serotoninérgico y 1B, justificaría la disminución de síntomas extrapirami- dales observados con estos medicamentos. Por otro lado, BREX no se asocia a sedación excesiva por su escasa unión a receptores H1.
Consideremos, de modo simplificado, la neurobiología de la esquizofrenia. Podría resumirse que los síntomas positivos de enfermedad (“lo que el paciente hace”) se producirían por
aumento del flujo de dopamina en el sistema mesolímbico (hipótesis dopaminérgica) y que, los síntomas negativos (“lo que el paciente deja de hacer”) / cognitivos se explicarían por incremento del tono de serotonina cortical. Se entiende, entonces, que existe un exceso del agonista endógeno en las respectivas áreas. Cuando se introduce un agonista parcial en presencia de un agonista total (en este caso dopamina y/o serotonina), el agonista parcial se comporta como antagonis- ta. De esta manera, BREX se comporta como antagonista en presencia de exceso de dopamina, en el sistema mesolímbico, y de la serotonina, a nivel cortical. Una diferencia importante entre BREX y ARI es que el primero posee menor actividad intrínseca como agonista parcial.
Dado que los sistemas serotoninérgico, dopaminérgico y no- radrenérgico participarían en la génesis de la agitación asocia- da a demencia, se ha propuesto que el BREX podría ser una alternativa farmacológica eficaz para su abordaje.
Desde el punto de vista farmacocinético, BREX muestra una biodisponibilidad cercana al 95%, con un pico máximo a las 4 horas. El estado estacionario se alcanza luego de la administración diaria durante 10 a 12 días. Se presenta en comprimidos recubiertos de 0,5, 1, 2, 3 y 4mg.
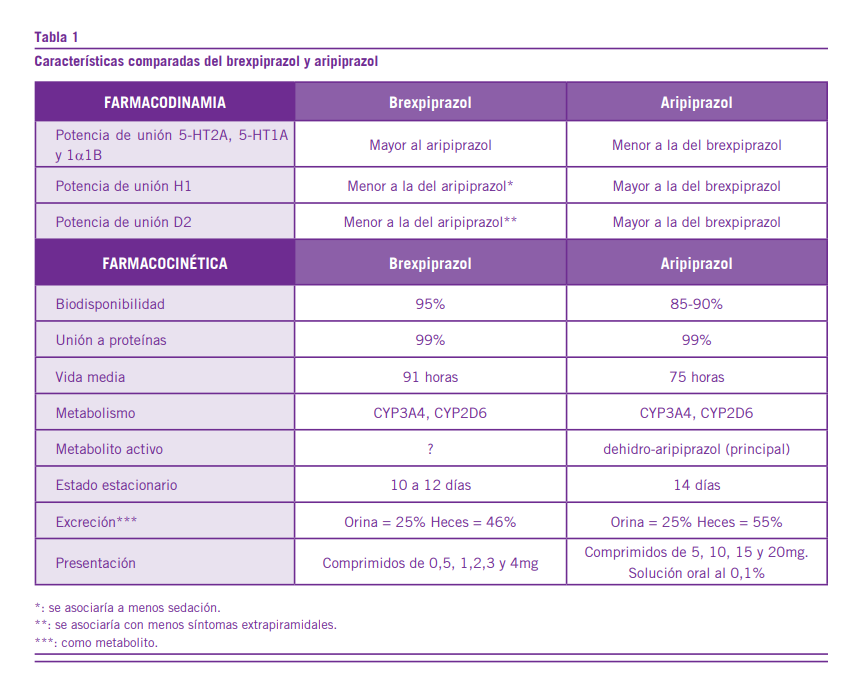
En la tabla 1 se muestras las características comparativas del BREX y el ARI.
Experiencia clínica
Un estudio pionero relacionado con la eficacia y seguridad del BREX en el manejo de la agitación, fue el llevado a cabo por Grossberg y colaboradores en 2020 (8). Se trató de un estudio multicéntrico, aleatorizado, doble ciego y compara- do contra placebo. Se incluyeron pacientes de entre 55 y 90 años con diagnóstico de EA. Los mismos debían mostrar sín- tomas de agitación o agresividad. Los pacientes no debían estar bajo tratamiento con antipsicóticos, anticonvulsivantes o estabilizantes del ánimo al momento de la randomización. Los medicamentos permitidos fueron los destinados a tratar la EA (memantina, inhibidores de colinesterasa, otros), antidepresi- vos y benzodiacepinas. El ensayo se realizó en dos partes ar- bitrariamente llamadas estudio 1 (E1) y estudio 2 (E2). En el E1, los pacientes fueron randomizados en relación 1:1:1 a re- cibir BREX 2 mg, BREX 1mg o placebo, durante 12 semanas. La dosis se tituló del día 1 al 29. En el E2, la randomización se realizó en razón 1:1 a recibir un esquema de dosis flexible de BREX (entre 0,5 y 2 mg) o placebo, por 12 semanas. La medida de eficacia fue el Cohen-Mansfield Agitation Inventory (CMAI) mediante el cual se estable un puntaje de frecuencia
de episodios de agitación con un valor mínimo de 29 y un máximo de 203. A menor valor de CMAI, menos frecuentes son los episodios de agitación.
Se incluyeron 433 pacientes en el E1. De ellos 135 fueron a la rama placebo, 137 a la BREX 1mg y 140 a la rama BREX 2mg. Los 20 pacientes restantes correspondían a una cuarta rama, BREX 0,5mg, que fue desestimada por considerarse di- cha dosis como inefectiva. Se observó descenso significativo (p<0,04) del CMAI en la rama BREX 2mg, únicamente. Con excepción de los 20 pacientes antes mencionados, la princi- pal causa de abandono del estudio fueron los eventos adver- sos. Entre los mismos destacan (con incidencia superior al 5%): cefalea, insomnio, mareos e infección urinaria.
En cuanto al E2, 270 fueron aleatorizados, correspondien- do 137 a la rama de titulación del BREX. Aunque no se ob- servaron beneficios significativos respecto del placebo, un análisis post hoc reveló que los pacientes que recibieron la dosis de 2mg tendrían una reducción significativa del CMAI. En este estudio los eventos adversos predominantes fueron cefalea y somnolencia.
A la luz de estos resultados, los autores concluyeron que BREX a la dosis de 2mg una vez al día por vía oral, podría ofrecer beneficios en el tratamiento de la agitación por EA.
En 2023, Lee y colaboradores (9) realizaron un estudio de confirmación sobre la eficacia y tolerabilidad del BREX. Uti- lizaron un diseño aleatorizado, doble ciego y controlado. Se consideraron 2 ramas principales: BREX y placebo en razón 2:1. La rama BREX fue nuevamente aleatorizada (razón 1:2) a recibir dosis fijas de BREX 2mg o 3mg, durante 12 semanas. Al igual que el estudio de Grossberg (8), la medida de eficacia fue la reducción del CMAI en pacientes adultos con agitación por EA. Se incluyeron 345 pacientes, de los cuales 228 se asignaron a la rama BREX. Los autores observaron reducción significativa del CMAI, respecto del placebo, en la rama de pacientes que recibieron una u otra dosis de BREX. No se detectaron diferencias significativas en cuanto a eventos ad- versos entre las 3 ramas. Los eventos predominantes en las ramas BREX fueron somnolencia, mareo, diarrea e infección urinaria.
¿Brexpiprazol o Aripiprazol?
Generar un verdadero aporte al arsenal terapéutico disponi- ble para el tratamiento de una patología determinada es ex- tremadamente difícil. Esto es debido a que el medicamento “innovador” debe presentar una ventaja clínicamente signifi- cativa en cuanto a eficacia y/o seguridad. En segundo plano,
la ventaja podría ser económica, pero sin resignar eficacia ni seguridad en comparación con el medicamento estándar dis- ponible en el mercado.
La organización sin fines de lucro, Prescrire, emite todos los años un documento llamado Drugs to avoid. En esta revisión se emiten juicios, basados en evidencia, sobre los medica- mentos más novedosos (y no tanto) acerca del aporte que rea- lizan individualmente a la terapéutica. Notará el lector, que la publicación de un “bravo” (es decir, un fármaco con beneficio potencial probable) no es frecuente (10). Estas iniciativas son muy importantes para evitar que los médicos prescriban me- dicamentos conocidos como me too. Estos corresponden a fár- macos que poseen una pequeña diferencia estructural respecto de un medicamento “líder”, pero que no ofrece ninguna ventaja clínica apreciable en ensayos clínicos o ni siquiera los posee. Aún no está claro si este podría ser el caso del BREX respecto del ARI. La ausencia de estudios clínicos aleatorizados “cabeza a cabeza” entre estos dos fármacos dificulta esta diferencia- ción. Hasta ahora, la evidencia sugiere beneficios asociados al BREX en pacientes con agitación en el contexto de la EA, gracias a ciertas diferencias farmacodinámicas (antes mencio- nadas) en favor de este. Se deberá esperar evidencia confiable para el ARI en este grupo de pacientes para poder definir si existe superioridad del BREX y descartar la posibilidad de me too. Por el momento, solo se cuenta con evidencia para éste último en un número reducido de pacientes.
Referencias bibliográficas
• 1. Prince, Martin, et al. World Alzheimer Report 2015. The Global Impact of Demen- tia: An analysis of prevalence, incidence, cost and trends. Diss. Alzheimer’s Disease Inter- national, 2015.
• 2. Antonsdottir IM, Smith J, Keltz M, Pors- teinsson AP. Advancements in the treatment of agitation in Alzheimer’s disease. Expert Opin Pharmacother. 2015;16(11): 1649-56. doi: 10.1517/14656566.2015.1059422. PMID: 26159445.
• 3. Porsteinsson AP, Drye LT, Pollock BG, Deva- nand DP, Frangakis C, Ismail Z, Marano C, Mei- nert CL, Mintzer JE, Munro CA, Pelton G, Rabins PV, Rosenberg PB, Schneider LS, Shade DM, Weintraub D, Yesavage J, Lyketsos CG; CitAD Research Group. Effect of citalopram on agita- tion in Alzheimer disease: the CitAD randomized clinical trial. JAMA. 2014 Feb 19;311(7):682-
- doi: 10.1001/jama.2014.93. PMID:
24549548; PMCID: PMC4086818.
• 4. Kales HC, Gitlin LN, Lyketsos CG; Detroit Expert Panel on Assessment and Management of Neuropsychiatric Symptoms of Dementia. Management of neuropsychiatric symptoms
of dementia in clinical settings: recommenda- tions from a multidisciplinary expert panel. J Am Geriatr Soc. 2014 Apr;62(4):762-9. doi: 10.1111/jgs.12730. Epub 2014 Mar 17. PMID: 24635665; PMCID: PMC4146407.
• 5. Maher AR, Maglione M, Bagley S, Suttorp M, Hu JH, Ewing B, Wang Z, Timmer M, Sult- zer D, Shekelle PG. Efficacy and comparative effectiveness of atypical antipsychotic medi- cations for off-label uses in adults: a syste- matic review and meta-analysis. JAMA. 2011 Sep 28;306(12):1359-69. doi: 10.1001/
jama.2011.1360. Erratum in: JAMA. 2012 Jan 11;307(2):147. PMID: 21954480.
• 6. Drye LT, Ismail Z, Porsteinsson AP, Ro- senberg PB, Weintraub D, Marano C, Pelton G, Frangakis C, Rabins PV, Munro CA, Meinert CL, Devanand DP, Yesavage J, Mintzer JE, Schneider LS, Pollock BG, Lyketsos CG; Ci- tAD Research Group. Citalopram for agitation in Alzheimer’s disease: design and methods. Alzheimers Dement. 2012;8(2):121-30. doi: 10.1016/j.jalz.2011.01.007. Epub 2012 Feb
- PMID: 22301195; PMCID: PMC3333484.
• 7. Stahl SM. Mechanism of action of brex- piprazole: comparison with aripiprazole. CNS
Spectr. 2016 Feb;21(1):1-6. doi: 10.1017/ S1092852915000954. PMID: 26899451.
• 8. Grossberg GT, Kohegyi E, Mergel V, Jo- siassen MK, Meulien D, Hobart M, Slomkows- ki M, Baker RA, McQuade RD, Cummings JL. Efficacy and Safety of Brexpiprazole for the Treatment of Agitation in Alzheimer’s Demen- tia: Two 12-Week, Randomized, Double-Blind, Placebo-Controlled Trials. Am J Geriatr Psy- chiatry. 2020 Apr;28(4):383-400. doi: 10.1016/j.jagp.2019.09.009. Epub 2019
Oct 1. PMID: 31708380.
• 9. Lee D, Slomkowski M, Hefting N, Chen D, Larsen KG, Kohegyi E, Hobart M, Cum- mings JL, Grossberg GT. Brexpiprazole for the Treatment of Agitation in Alzheimer De- mentia: A Randomized Clinical Trial. JAMA Neurol. 2023 Dec 1;80(12):1307-1316. doi:
10.1001 / jamaneurol.2023.3810. PMID:
37930669; PMCID: PMC10628834
• 10. Prescrire. Drugs to avoid. In the name of better patient care: 2024 update. Disponible en: Prescrire IN ENGLISH – Drugs to avoid : 2024 update – Drugs to avoid : Drugs to avoid: 2024 upda- te Consultado el 25 de marzo de 2024.







No comments! Be the first commenter?